13.1: Контроль росту мікробів
- Page ID
- 3870
Цілі навчання
- Порівняйте дезінфікуючі засоби, антисептики та стерилізатори
- Опишіть принципи контролю присутності мікроорганізмів шляхом стерилізації та дезінфекції
- Диференціюйте мікроорганізми різних рівнів біологічної безпеки та поясніть методи, що використовуються для поводження з мікробами на кожному рівні
Клінічна спрямованість: Частина 1
Роберта - 46-річний агент з нерухомості, який нещодавно переніс холецистектомію (операцію з видалення хворобливих каменів у жовчному міхурі). Операція проводилася лапароскопічно за допомогою дуоденоскопа, спеціалізованого ендоскопа, який дозволяє хірургам бачити всередині тіла за допомогою крихітної камери. Після повернення додому з лікарні у Роберти розвинулися болі в животі і висока температура. Також вона відчувала печіння під час сечовипускання і помітила кров у сечі. Вона повідомила свого хірурга про ці симптоми відповідно до її післяопераційних інструкцій.
Вправа\(\PageIndex{1}\)
Які можливі причини симптомів Роберти?
Щоб запобігти поширенню хвороб людини, необхідно контролювати зростання і велику кількість мікробів в або на різних предметах, часто використовуваних людиною. Неживі предмети, такі як дверні ручки, іграшки або рушники, які можуть містити мікроби та сприяти передачі захворювань, називаються фомітами. Два фактори сильно впливають на рівень чистоти, необхідний для конкретного фоміту, і, отже, протокол, обраний для досягнення цього рівня. Перший фактор - це додаток, для якого буде використовуватися предмет. Наприклад, інвазивні програми, які вимагають введення в організм людини, вимагають набагато більш високого рівня чистоти, ніж додатки, які цього не роблять. Другий фактор - рівень стійкості до протимікробної обробки потенційними збудниками. Наприклад, продукти, збережені консервуванням, часто забруднюються бактерією Clostridium botulinum, яка виробляє нейротоксин, що викликає ботулізм. Оскільки C. botulinum може виробляти ендоспори, які можуть пережити суворі умови, для усунення ендоспор повинні використовуватися екстремальні температури та тиск. Інші організми можуть не вимагати таких крайніх заходів і можуть контролюватися такою процедурою, як прання білизни в пральній машині.
Рівні біологічної безпеки лабораторії
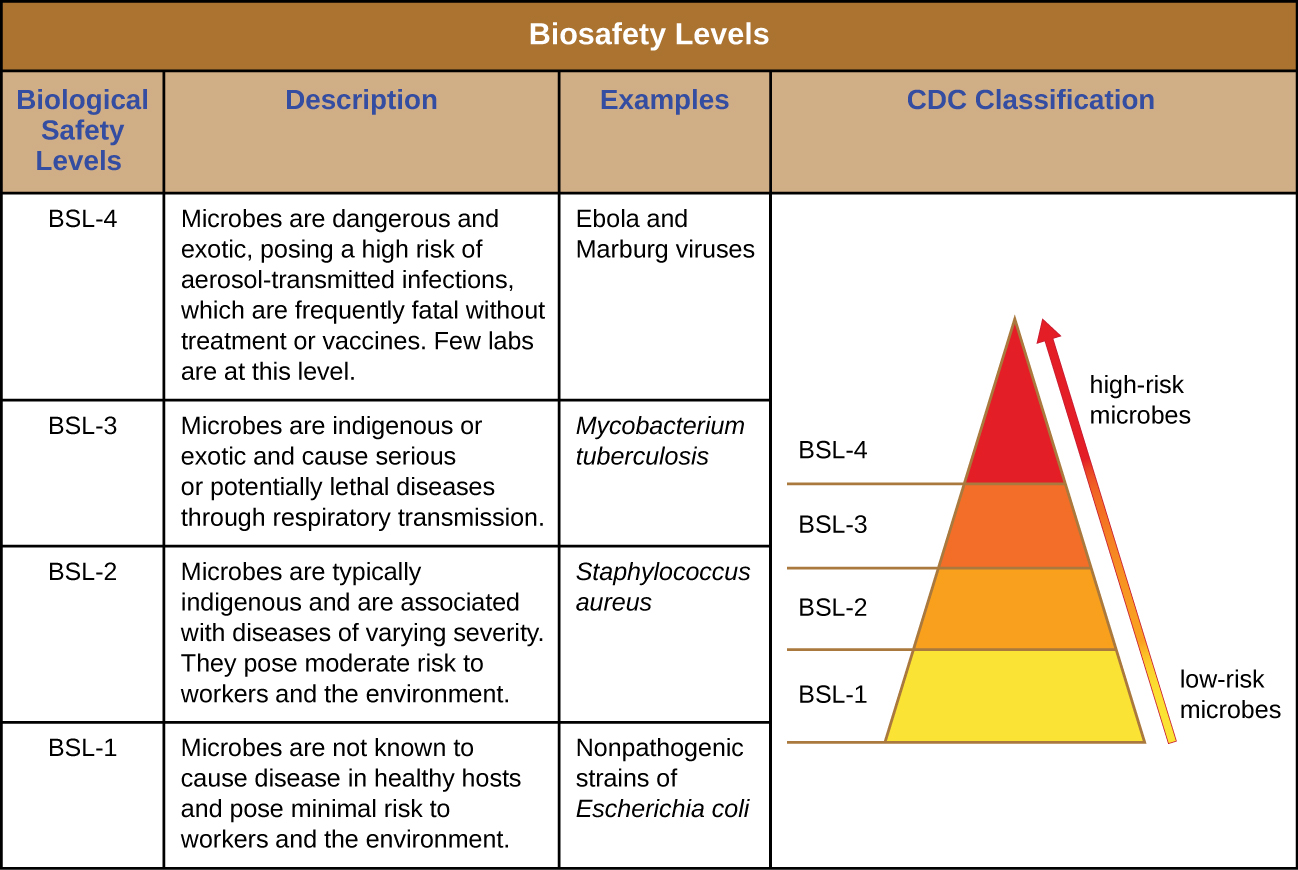
Для дослідників або лабораторного персоналу, що працює з патогенами, ризики, пов'язані з конкретними патогенами, визначають рівень чистоти та необхідного контролю. Центри контролю та профілактики захворювань (CDC) та Національні інститути охорони здоров'я (NIH) встановили чотири класифікаційні рівні, які називаються «рівнями біологічної безпеки» (BSL). Різні організації по всьому світу, включаючи Всесвітню організацію охорони здоров'я (ВООЗ) і Європейський Союз (ЄС), використовують подібну схему класифікації. Згідно CDC, BSL визначається інфекційністю агента, легкістю передачі та потенційною тяжкістю захворювання, а також типом роботи, що виконується з агентом. 1
Кожен BSL вимагає різного рівня біоізоляції, щоб запобігти зараженню та поширенню інфекційних агентів на персонал лабораторій та, зрештою, громаду. Наприклад, найнижчий BSL, BSL-1, вимагає найменшої кількості запобіжних заходів, оскільки це стосується ситуацій з найменшим ризиком мікробної інфекції.
Засоби BSL-1 - це ті, які, як правило, не викликають інфекції у здорових дорослих людей. До них відносяться неінфекційні бактерії, такі як непатогенні штами кишкової палички та Bacillus subtilis, а також віруси, які, як відомо, заражають тварин, відмінних від людей, такі як бакуловіруси (віруси комах). Оскільки робота з агентами BSL-1 становить дуже невеликий ризик, потрібно мало запобіжних заходів. Працівники лабораторії використовують стандартну асептичну техніку і можуть працювати з цими агентами на відкритому лабораторному стенді або столі, одягаючи засоби індивідуального захисту (ЗІЗ), такі як лабораторне пальто, окуляри та рукавички, за необхідності. Крім раковини для миття рук і дверей, щоб відокремити лабораторію від решти будівлі, ніяких додаткових модифікацій не потрібно.
Агенти, класифіковані як BSL-2, включають ті, які становлять помірний ризик для працівників лабораторій та громади, і, як правило, є «корінними», що означає, що вони зазвичай зустрічаються в цьому географічному районі. До них відносяться такі бактерії, як золотистий стафілокок і Salmonella spp., і віруси, такі як гепатит, свинка та віруси кору. Лабораторії BSL-2 вимагають додаткових запобіжних заходів, крім запобіжних заходів BSL-1, включаючи обмежений доступ; необхідні ЗІЗ, включаючи захисний щиток за деяких обставин; і використання шаф біологічної безпеки для процедур, які можуть диспергувати агенти по повітрю (називається «аерозолізацією»). Лабораторії BSL-2 оснащені самозакриваються дверцятами, станцією для промивання очей та автоклавом, який є спеціалізованим пристроєм для стерилізації матеріалів парою під тиском перед використанням або утилізацією. Лабораторії БСЛ-1 також можуть мати автоклав.
Засоби BSL-3 можуть викликати летальні інфекції шляхом вдихання. Вони можуть бути як корінними, так і «екзотичними», що означає, що вони походять з іноземного місця, і включають такі патогени, як Mycobacterium tuberculosis, Bacillus anthracis, вірус Західного Нілу та вірус імунодефіциту людини (ВІЛ). Через серйозний характер інфекцій, викликаних агентами BSL-3, лабораторії, що працюють з ними, вимагають обмеженого доступу. Працівники лабораторії знаходяться під медичним наглядом, можливо, отримують щеплення від мікробів, з якими вони працюють. Крім вже згаданих стандартних ЗІЗ, лабораторний персонал лабораторій в лабораторіях BSL-3 також повинен носити респіратор і постійно працювати з мікробами та інфекційними агентами в кабінеті біологічної безпеки. Лабораторії BSL-3 потребують мийки без рук, станції для промивання очей біля виходу та двох комплектів самозакриваються та замикаються дверей біля входу. Ці лабораторії оснащені спрямованим повітряним потоком, що означає, що чисте повітря витягується через лабораторію з чистих зон до потенційно забруднених районів. Це повітря не можна рециркулювати, тому необхідна постійна подача чистого повітря.
Засоби БСЛ-4 є найбільш небезпечними і часто смертельними. Ці мікроби, як правило, екзотичні, легко передаються при вдиханні і викликають інфекції, для яких немає лікування або щеплень. Приклади включають вірус Ебола та вірус Марбург, обидва з яких викликають геморагічну лихоманку, і вірус віспи. Існує лише невелика кількість лабораторій у Сполучених Штатах та у всьому світі, належним чином обладнаних для роботи з цими агентами. Окрім запобіжних заходів BSL-3, працівники лабораторій у закладах BSL-4 також повинні змінити одяг при вході в лабораторію, приймати душ при виході та знезаражувати весь матеріал при виході. Під час роботи в лабораторії вони повинні або носити захисний костюм для всього тіла з призначеною подачею повітря, або проводити всі роботи в кабінеті біологічної безпеки з високоефективною подачею повітря з фільтром твердих частинок (HEPA) і подвійно фільтрованим вихлопом HEPA. При носінні костюма тиск повітря всередині костюма повинен бути вище, ніж зовні костюма, так що, якщо відбувається витік в костюмі, лабораторне повітря, яке може бути забруднене, не може бути втягнуто в костюм (рис.\(\PageIndex{1}\)). Сама лабораторія повинна розташовуватися або в окремій будівлі, або в ізольованій частині будівлі і мати власну систему припливу і витяжки повітря, а також власну систему знезараження. BSL узагальнені на малюнку\(\PageIndex{2}\).

Щоб дізнатися більше про чотири BSL, відвідайте веб-сайт CDC.
Вправа\(\PageIndex{2}\)
Які деякі фактори використовуються для визначення БСЛ, необхідного для роботи з конкретним збудником?
Стерилізація
Найбільш екстремальні протоколи мікробного контролю спрямовані на досягнення стерилізації: повне видалення або вбивство всіх вегетативних клітин, ендоспор та вірусів з цільового предмета або середовища. Протоколи стерилізації, як правило, зарезервовані для лабораторних, медичних, виробничих та харчової промисловості, де певні предмети можуть бути вкрай необхідними для того, щоб певні предмети були повністю вільними від потенційно інфекційних агентів. Стерилізація може бути здійснена будь-якими фізичними засобами, такими як вплив високої температури, тиску або фільтрації через відповідний фільтр, або хімічними засобами. Хімічні речовини, які можуть бути використані для досягнення стерилізації, називаються стерильними s. Стериліанти ефективно вбивають всі мікроби та віруси, а при відповідному часі впливу також можуть вбивати ендоспори.
Для багатьох клінічних цілей необхідна асептична техніка для запобігання забруднення стерильних поверхонь. Асептична техніка передбачає поєднання протоколів, які в сукупності підтримують стерильність, або асептику, запобігаючи тим самим зараження пацієнта мікробами та інфекційними агентами. Відмова від практики асептичної техніки під час багатьох видів клінічних процедур може ввести мікроби в організм пацієнта і поставити пацієнта під загрозу сепсису, системної запальної реакції на інфекцію, що призводить до високої температури, почастішання серцевих і дихальних скорочень, шоку і, можливо, смерті. Медичні процедури, які несуть ризик зараження, повинні проводитися в стерильному полі, відведеному місці, де зберігаються всі вегетативні мікроби, ендоспори та віруси. Стерильні поля створюються відповідно до протоколів, що вимагають використання стерилізованих матеріалів, таких як упаковка та драпірування, а також суворі процедури миття та застосування стерилістів. Інші протоколи дотримуються для підтримки стерильного поля під час проведення медичної процедури.
Один протокол стерилізації харчових продуктів, комерційна стерилізація, використовує тепло при досить низькій температурі, щоб зберегти якість їжі, але досить високу, щоб знищити загальні патогени, відповідальні за харчові отруєння, такі як C. botulinum. Оскільки C. botulinum та його ендоспори зазвичай знаходяться в ґрунті, вони можуть легко забруднювати культури під час збирання врожаю, і ці ендоспори можуть згодом прорости в анаеробному середовищі після консервування продуктів. Металеві банки з їжею, забруднені C. botulinum, будуть випирати через вироблення мікробів газів; забруднені банки з їжею зазвичай випирають на металеву кришку. Щоб виключити ризик зараження C. botulinum, комерційні протоколи консервування харчових продуктів розроблені з великою похибкою. Вони припускають неймовірно велику популяцію ендоспор (10 12 на банку) і мають на меті скоротити цю популяцію до 1 ендоспор на банку для забезпечення безпеки консервів. Наприклад, продукти з низьким і середнім вмістом кислот нагрівають до 121° C протягом мінімум 2,52 хвилин, це час, який знадобиться для зменшення популяції 10 12 ендоспор на банку до 1 ендоспор при цій температурі. Незважаючи на це, комерційна стерилізація не усуває присутності всіх мікробів; скоріше, вона спрямована на ті збудники, які викликають псування та харчові захворювання, дозволяючи при цьому вижити багатьом непатогенним організмам. Тому «стерилізація» є дещо неправильною в цьому контексті, і комерційна стерилізація може бути більш точно описана як «квазістерилізація».
Вправа\(\PageIndex{3}\)
У чому різниця між стерилізацією і асептичною технікою?
Асоціація хірургічних технологів публікує стандарти асептичної техніки, включаючи створення і підтримку стерильного поля.
Інші методи контролю
Протоколи стерилізації вимагають процедур, які не є практичними або необхідними у багатьох умовах. Різні інші методи використовуються в клінічних і неклінічних умовах для зниження мікробного навантаження на предмети. Хоча терміни для цих методів часто використовуються взаємозамінно, існують важливі відмінності (рис.\(\PageIndex{3}\)).
Процес дезінфекції інактивує більшість мікробів на поверхні фоміта за допомогою антимікробних хімікатів або тепла. Оскільки деякі мікроби залишаються, дезінфікований предмет не вважається стерильним. В ідеалі дезінфікуючі засоби повинні бути швидкодіючими, стабільними, легкими в приготуванні, недорогими та простими у використанні. Прикладом природного дезінфікуючого засобу є оцет, його кислотність вбиває більшість мікробів. Хімічні дезінфікуючі засоби, такі як хлорний відбілювач або продукти, що містять хлор, використовуються для очищення неживих поверхонь, таких як лабораторні лавки, клінічні поверхні та раковини для ванної кімнати. Типова дезінфекція не призводить до стерилізації, оскільки ендоспори, як правило, виживають навіть тоді, коли всі вегетативні клітини були вбиті.
На відміну від дезінфікуючих засобів, антисептики - протимікробні хімічні речовини, безпечні для використання на живій шкірі або тканині. Приклади антисептиків включають перекис водню і ізопропіловий спирт. Процес нанесення антисептика називається антисептиком. Крім характеристик хорошого дезінфікуючого засобу, антисептики також повинні бути вибірково ефективними проти мікроорганізмів і здатними глибоко проникати в тканини, не викликаючи пошкодження тканин.
Тип протоколу, необхідного для досягнення бажаного рівня чистоти, залежить від конкретного елемента, що підлягає очищенню. Наприклад, ті, що використовуються клінічно, класифікуються як критичні, напівкритичні та некритичні. Важливі предмети повинні бути стерильними, оскільки вони будуть використовуватися всередині організму, часто проникаючи в стерильні тканини або кров; приклади критичних предметів включають хірургічні інструменти, катетери та внутрішньовенні рідини. Шлунково-кишкові ендоскопи та різні види обладнання для респіраторної терапії є прикладами напівкритичних предметів; вони можуть контактувати зі слизовими оболонками або неінтактною шкірою, але не проникати в тканини. Напівкритичні предмети, як правило, не потрібно стерилізувати, але вимагають високого рівня дезінфекції. Предмети, які можуть контактувати, але не проникати в неушкоджену шкіру, є некритичними предметами; прикладами є постільна білизна, меблі, милиці, стетоскопи та манжети артеріального тиску. Ці вироби повинні бути чистими, але не сильно дезінфікованими.
Акт миття рук є прикладом дегермінгу, при якому кількість мікробів значно зменшується шляхом м'якого очищення живої тканини, найчастіше шкіри, м'якою хімічною речовиною (наприклад, милом), щоб уникнути передачі патогенних мікробів. Протирання шкіри спиртовим тампоном в місці ін'єкції - ще один приклад дегермінга. Ці методи дегермінга видаляють більшість (але не всіх) мікробів з поверхні шкіри.
Термін санітарна обробка відноситься до очищення фомітів для видалення достатньої кількості мікробів для досягнення рівнів, які вважаються безпечними для здоров'я населення. Наприклад, комерційні посудомийні машини, що використовуються в галузі громадського харчування, зазвичай використовують дуже гарячу воду та повітря для миття та сушіння; високі температури вбивають більшість мікробів, дезінфікуючи посуд. Поверхні в лікарняних палатах зазвичай дезінфікуються за допомогою хімічного дезінфікуючого засобу для запобігання передачі захворювання між пацієнтами. \(\PageIndex{3}\)Рисунок узагальнює загальні протоколи, визначення, програми та агенти, що використовуються для контролю росту мікробів.

Вправа\(\PageIndex{4}\)
- Чим відрізняється дезінфікуючий засіб від антисептика?
- Що найефективніше при видаленні мікробів з продукту: санітарна обробка, дегермінг або стерилізація? Поясніть.
Клінічна спрямованість: Частина 2
Лікар Роберти підозрював, що бактеріальна інфекція є причиною її раптової високої температури, болю в животі та кров'янистої сечі. На підставі цих симптомів лікар діагностував інфекцію сечовивідних шляхів (ІМП). Найрізноманітніші бактерії можуть викликати ІМП, які зазвичай виникають, коли бактерії з нижніх відділів шлунково-кишкового тракту потрапляють в сечовивідні шляхи. Однак нещодавня операція Роберти на жовчному міхурі змусила лікаря підозрювати, що під час операції вона заразилася внутрішньолікарняною (придбаною лікарнею) інфекцією. Лікар взяв зразок сечі і замовив посів сечі, щоб перевірити наявність лейкоцитів, еритроцитів та бактерій. Результати цього тесту допомогли б визначити причину зараження. Лікар також призначив курс антибіотика ципрофлоксацин, впевнений, що він дозволить очистити інфекцію Роберта.
Вправа\(\PageIndex{5}\)
Які можливі способи введення бактерій у сечовивідні шляхи Роберти під час операції?
Вимірювання мікробного контролю
Фізико-хімічні методи мікробного контролю, що вбивають цільовий мікроорганізм, ідентифікуються суфіксом -цидом (або -цидним). Приставка вказує на тип мікроба або інфекційного агента, вбитого методом лікування: бактерициди вбивають бактерії, віруциди вбивають або інактивують віруси, а фунгіциди вбивають гриби. Інші методи не вбивають організми, а, натомість, зупиняють їх ріст, роблячи їх популяцію статичною; такі методи ідентифікуються суфіксом -стат (або -статичний). Наприклад, бактеріостатичні процедури пригнічують ріст бактерій, тоді як фунгістатичні процедури пригнічують ріст грибків. Фактори, що визначають, чи є конкретне лікування -цидним або -статичним, включають типи мікроорганізмів, спрямованих, концентрацію використовуваного хімічного речовини та характер застосовуваного лікування.
Хоча -статичні методи лікування насправді не вбивають інфекційних агентів, вони часто менш токсичні для людей та інших тварин, а також можуть краще зберегти цілісність оброблюваного предмета. Такі методи лікування, як правило, достатні, щоб тримати мікробну популяцію предмета під контролем. Знижена токсичність деяких з цих -статичних хімічних речовин також дозволяє їх безпечно просочувати в пластмаси, щоб запобігти зростанню мікробів на цих поверхнях. Такі пластмаси використовуються в таких продуктах, як іграшки для дітей і обробні дошки для приготування їжі. Коли використовується для лікування інфекції, статичні методи лікування, як правило, достатні в іншому випадку здорової людини, запобігаючи розмноженню збудника, тим самим дозволяючи імунній системі людини очистити інфекцію.
Ступінь мікробного контролю можна оцінити за допомогою мікробної кривої смерті для опису прогресу та ефективності конкретного протоколу. При впливі певного протоколу контролю мікробів фіксований відсоток мікробів всередині популяції загине. Оскільки швидкість вбивств залишається постійною навіть тоді, коли чисельність популяції змінюється, відсоток вбитих є більш корисною інформацією, ніж абсолютна кількість вбитих мікробів. Криві смерті часто будуються як semilog-графіки так само, як і криві росту мікробів, оскільки зменшення мікроорганізмів, як правило, логарифмічне (рис.\(\PageIndex{4}\)). Кількість часу, необхідного для того, щоб конкретний протокол виробляв зменшення кількості організмів на один порядок, або загибель 90% популяції, називається десятковим часом скорочення (ДРТ) або D-значенням.
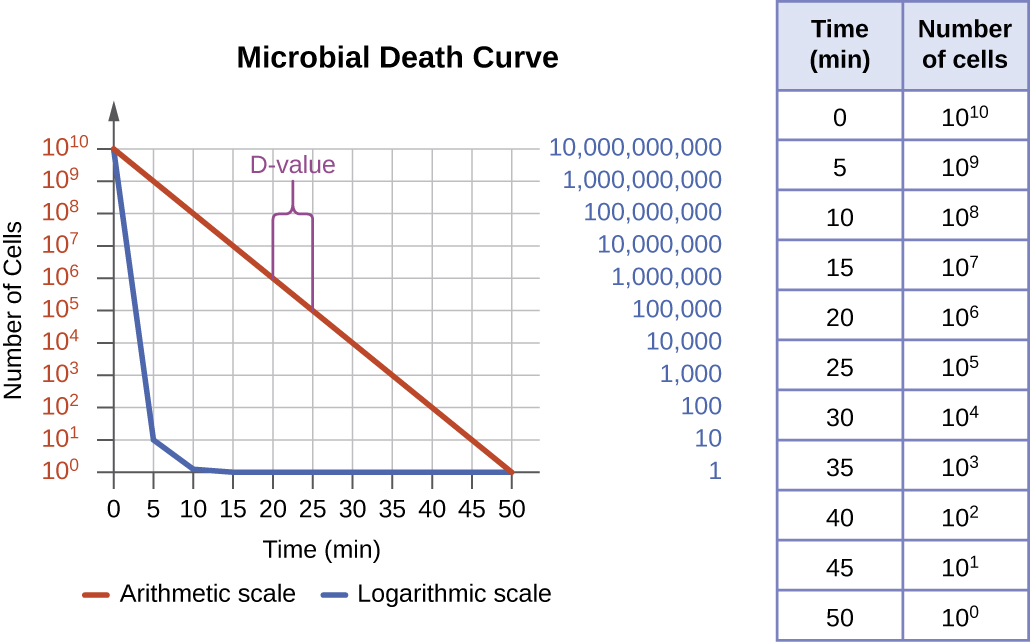
Ефективності дезінфікуючого засобу або протоколу мікробного контролю сприяють кілька факторів. По-перше, як показано на малюнку\(\PageIndex{4}\), важлива тривалість часу впливу. Більш тривалий час впливу вбиває більше мікробів. Оскільки мікробна смерть населення, що піддається певному протоколу, є логарифмічною, для знищення високого навантаження населення потрібно більше часу, ніж навантаження з низькою популяцією, що піддається тому ж протоколу. Більш короткий час лікування (вимірюється в кратних значенню D) потрібен при запуску з меншої кількості організмів. Ефективність також залежить від сприйнятливості засобу до цього дезінфікуючого засобу або протоколу. Важлива також концентрація дезінфікуючого засобу або інтенсивність впливу. Наприклад, більш високі температури і більш високі концентрації дезінфікуючих засобів вбивають мікроби швидше і ефективніше. Умови, що обмежують контакт між агентом і клітинами-цільовими клітинами - наприклад, наявність тілесних рідин, тканин, органічного сміття (наприклад, бруду або калу) або біоплівок на поверхнях - збільшують час очищення або інтенсивність протоколу мікробного контролю, необхідного для досягнення бажаного рівня чистоти . Всі ці фактори необхідно враховувати при виборі відповідного протоколу для контролю росту мікробів в тій чи іншій ситуації.
Вправа\(\PageIndex{6}\)
- Які дві можливі причини вибору бактеріостатичного лікування перед бактерицидною?
- Назвіть як мінімум два фактори, які можуть поставити під загрозу ефективність дезінфікуючого засобу.
Ключові поняття та резюме
- Неживі предмети, які можуть містити мікроби та сприяти їх передачі, називаються фомітами. Рівень чистоти, необхідний для фоміту, залежить як від використання предмета, так і від інфекційного агента, яким предмет може бути заражений.
- CDC та NIH встановили чотири рівні біологічної безпеки (BSL) для лабораторій, що виконують дослідження інфекційних агентів. Кожен рівень призначений для захисту персоналу лабораторії та громади. Ці БСЛ визначаються інфекційністю агента, легкістю передачі та потенційною тяжкістю захворювання, а також типом роботи, що виконується з агентом.
- Дезінфекція видаляє потенційних патогенів з фоміту, тоді як антисептик використовує антимікробні хімічні речовини, досить безпечні для тканин; в обох випадках мікробне навантаження знижується, але мікроби можуть залишатися, якщо використовувана хімічна речовина не буде достатньо сильною, щоб бути стерилістом.
- Кількість чистоти (стерилізація проти дезінфекції високого рівня проти загальної чистоти), необхідна для предметів, що використовуються клінічно, залежить від того, чи буде предмет контактувати зі стерильними тканинами (критичним предметом), слизовими оболонками (напівкритичним предметом) або неушкодженими шкіра (некритичний предмет).
- Медичні процедури з ризиком зараження повинні проводитися в стерильному полі, підтримуваному належною асептичною технікою для запобігання сепсису.
- Стерилізація необхідна для деяких медичних застосувань, а також у харчовій промисловості, де ендоспори Clostridium botulinum гинуть через комерційні протоколи стерилізації.
- Фізичні або хімічні методи контролю росту мікробів, що призводять до загибелі мікроба, позначаються суфіксами -цидом або -цидним (наприклад, як у випадку з бактерицидами, вірицидами та фунгіцидами), тоді як ті, що гальмують ріст мікробів, є позначаються суфіксами -стат або -статичні (наприклад, бактеріостатичні, фунгістатичні).
- Криві мікробної загибелі відображають логарифмічний спад живих мікробів, що піддаються впливу методу мікробного контролю. Час, необхідний для протоколу для отримання 1-log (90%) скорочення мікробної популяції, - це десятковий час скорочення, або D-значення.
- При виборі протоколу контролю мікробів фактори, які слід враховувати, включають тривалість часу впливу, тип мікроба, орієнтований, його сприйнятливість до протоколу, інтенсивність обробки, наявність органічних речовин, які можуть перешкоджати протоколу, та умови навколишнього середовища, які можуть змінити ефективність протоколу.
Виноски
- 1 Центри США з контролю та профілактики захворювань. «Визнання рівнів біобезпеки». http://www.cdc.gov/training/quicklearns/biosafety/. Доступ до 7 червня 2016 року.
