4.2: В'язкість полімерів
- Page ID
- 19939
Полімери займають дуже важливу нішу в матеріалах, які ми використовуємо щодня. Що робить їх унікальними? Чому вони мають властивості, які не легко відтворюються іншими матеріалами?
Почнемо з властивості, з яким ви напевно знайомі. В'язкість - це термін, який ми використовуємо для опису «товщини» різних рідин. Наприклад, ми говоримо, що мед більш в'язкий, ніж вода. Моторне масло більш в'язке, ніж бензинове. Коли ми говоримо про це, ми маємо на увазі, що воду набагато легше помішувати або наливати, ніж мед. Мед рухається повільніше. Він чинить опір руху ложки, коли ми її перемішуємо. В'язкість часто описується в дуже загальних рисах як «опір потоку». Мед тече не дуже легко, особливо в порівнянні з чимось на зразок води.

Тепер мед - це не полімер. Це дуже концентрований розчин. Він містить трохи води і багато цукрів, а також інші невеликі молекули, вироблені рослинами, з яких бджоли збирали нектар, щоб зробити мед. Цукор також не є полімерами; це прості моносахариди, такі як глюкоза та фруктоза. Тим не менш, ця висока в'язкість - це щось спільне меду з полімерними розчинами, а також з деякими олігомерами, які є коротколанцюговими полімерами, які можуть бути рідинами замість твердих речовин.
Чому мед такий в'язкий? Частково це просто те, що молекули цукру у воді набагато більші, ніж молекули води, тому вони відчувають набагато більше тяги, коли вони рухаються через розчин порівняно з простою водою.
Сильні міжмолекулярні атракціони між окремими молекулами цукру також є основним фактором. Цукор покриті OH або гідроксильними групами, які здатні до міцних водневих зв'язків. Оскільки ці молекули рухаються повз один одного в самому концентрованому розчині, вони чіпляються один за одного, сповільнюючи потік рідини.

Приклад моторного масла працює аналогічним чином. Моторне масло і бензин складаються з одного класу сполук, вуглеводнів, що складаються з вуглецевих ланцюгів, покритих атомами водню. Вони дуже схожі один на одного. Міжмолекулярні атракціони між молекулами набагато слабкіші, ніж між молекулами цукру; вони просто лондонські сили дисперсії. Основна відмінність моторного масла від бензину полягає в тому, що моторне масло містить набагато довші вуглеводневі ланцюги. Молекули більші, і тому вони відчувають більше тяги, коли вони рухаються через рідину. Кількість міжмолекулярних взаємодій також має вирішальне значення для визначення того, наскільки міцно дві молекули тримаються один за одним, і цей фактор особливо важливий у дуже слабких лондонських силах дисперсії, де невелика перевага проходить довгий шлях. Ті довші вуглеводневі ланцюги в моторному маслі чіпляються один за одного набагато сильніше, ніж більш короткі в бензині, тому бензин тече набагато легше, ніж моторне масло.
З аналогічних причин олігомери і полімери, якщо вони є рідинами, також проявляють високу в'язкість. Розширений контакт між їх довгими молекулярними ланцюгами призводить до посилених міжмолекулярних атракціонів, які сприяють опору потоку. Збільшення опору також є фактором; навіть у розчині ці дуже великі молекули стикаються з більшою стійкістю, оскільки вони рухаються повз молекул розчинника порівняно з опором менших молекул.
Фактично вимірювання в'язкості полімерних розчинів є ще одним способом визначення розміру полімеру — приводячи до довжини ланцюга і молекулярної маси. Чим більше полімер, тим більше опір, а також більше міжмолекулярного тяжіння, і тим вище в'язкість.

Так, в'язкість збільшується з молекулярною масою, але не обов'язково лінійним способом. Це може ускладнити використання подібного графіка для прогнозування молекулярної маси за допомогою вимірювання в'язкості. Одна поширена річ, яку потрібно зробити в цій ситуації, - взяти журнал значень. Такий підхід часто дасть пряму лінію, коли дві речі пов'язані.
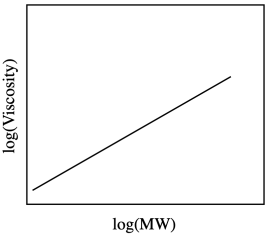
Часто в природі одне фізичне властивість, яке залежить від іншого, буде слідувати «закону влади». Це означає, що одна величина залежить від іншої, піднятої до якогось показника. В даному випадку зв'язок описується рівнянням Марка-Хоувінка:
\[ [η] = KM^α\]
У цьому рівнянні [η] - це внутрішня в'язкість; це в'язкість, що приписується розчиненому речовині, а не в'язкість самого розчинника. М - молекулярна маса. K і α - константи для конкретного полімеру.
Якщо взяти журнал обох сторін рівняння - це нормально, щоб зробити математично, так само, як ви могли б помножити обидві сторони рівняння на чотири або відняти три з обох сторін і все ще мати еквівалентний вираз - ви отримаєте:
\[\log[η] = log(KM^a)\]
Якщо взяти журнал двох речей, помножених разом, це те ж саме, що додавання окремих журналів обох речей.
\[\log[η] = \log K + \log(M^a)\]
І якщо взяти журнал щось підняв до експоненти, показник просто зводиться, щоб стати коефіцієнтом.
\[\log[η] = \log K + α\log M\]
або
\[\log[η] = α \log M + \log K\]
Це виглядає як рівняння для прямої лінії:
\[y = mx + b.\]
Тут ви намалюєте\(\log[η]\) на осі y,\(\log M\) на осі x, і ви отримаєте пряму лінію з цими константами,\(α\) і\(K\), як нахил і перехоплення y-відповідно.
Такий підхід не дає абсолютного виміру. Ви не могли взяти два абсолютно різні полімери, провести вимірювання в'язкості і зробити висновки про те, який з них має більш високу середню молекулярну масу. Однак, якби ви взяли серію полімерів того ж виду і виміряли їх в'язкість у розчині, ви зможете вивести, які з них довші, а які - коротші.
Насправді залежність в'язкості від молекулярної маси полімерів є більш складною, ніж припускає цей графік. Якщо ви маєте справу з досить великими полімерами, графік починає виглядати так:

Чому він прогинається? Пам'ятайте, полімери в розчині згортаються в кульки. Довший ланцюг якраз відповідає більшій котушці. У якийсь момент ці ланцюги стають досить великими, що вони, швидше за все, не залишаться згорнутими незалежно один від одного. Вони стають все частіше і частіше взаємодіяти один з одним. Вони заплутуються один з одним.

Є багато інших факторів, які вам доведеться враховувати при використанні в'язкості для оцінки молекулярної маси. Одним з них є концентрація, наприклад. Чим більше концентрований полімерний розчин, тим більше великих молекул у вас виявляють тягу і взаємодіють один з одним. Більш висока концентрація призводить до більш високого вимірювання в'язкості. Отже, вам доведеться переконатися, що ви враховували концентрації полімерів, якщо ви використовували цей метод.
Проблема ПП2.1.
Оцініть значення α і К для полімеру, які надали на графіку нижче.
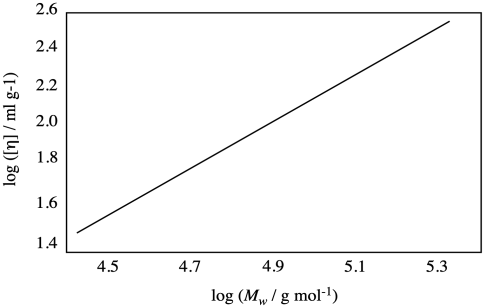
Проблема ПП2.2.
Припустимо, у вас полімер, описаний нижче сюжетом. Якщо ваш зразок має молекулярну масу 1 мільйон г/моль, що б ви очікували на внутрішню в'язкість в умовах цього експерименту?
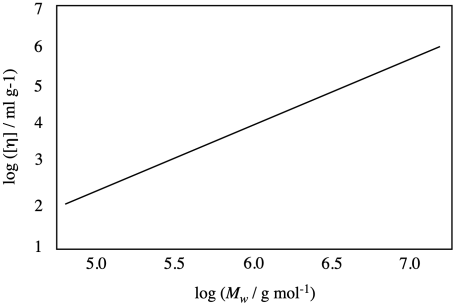
Проблема ПП2.3.
Припустимо, у вас є калібрувальний графік, нижче, для конкретного полімеру. Якщо виміряти внутрішню в'язкість зразка і виявити, що значення становить 800 мл/г, яка молекулярна маса зразка?

Проблема РР2.4.
Етанол (CH 3 CH 2 OH) має «абсолютну в'язкість» 1,095 сантипуаза, тоді як етиленгліколь (HOCH 2 CH 2 OH) має абсолютну в'язкість 16,2 сантипуази. Поясніть, чому ці два значення настільки різні.