16.2: Вуглеводні
- Page ID
- 22646
- Визначте алкани, алкени, алкіни та ароматичні сполуки.
- Перерахуйте деякі властивості вуглеводнів.
Найпростіші органічні сполуки - це ті, що складаються лише з двох елементів: вуглецю та водню. Ці сполуки називаються вуглеводнями. Самі вуглеводні поділяються на два типи: аліфатичні вуглеводні і ароматичні вуглеводні.
Аліфатичні вуглеводні - це вуглеводні на основі ланцюгів атомів С. Існує три види аліфатичних вуглеводнів. Алкани - це аліфатичні вуглеводні з тільки поодинокими ковалентними зв'язками. Алкени - це вуглеводні, які містять принаймні один подвійний зв'язок С—С, а алкіни - вуглеводні, які містять потрійний зв'язок C-C. Іноді ми знаходимо аліфатичний вуглеводень з кільцем атомів С; ці вуглеводні називаються циклоалканами (або циклоалкенами або циклоалкінами).
Ароматичні вуглеводні мають спеціальне шестивуглецеве кільце, яке називається бензольним кільцем. Електрони в бензольному кільці мають особливі енергетичні властивості, які надають бензолу фізико-хімічні властивості, які помітно відрізняються від алканів. Спочатку термін ароматичний використовувався для опису цього класу сполук, оскільки вони були особливо ароматними. Однак в сучасній хімії термін ароматичний позначає наявність шестичленного кільця, яке надає молекулі різні і унікальні властивості.
Найпростіші алкани мають свої атоми С, з'єднані прямим ланцюгом; вони називаються нормальними алканами. Названі вони відповідно до кількості атомів С в ланцюжку. Найменший алкан - метан:
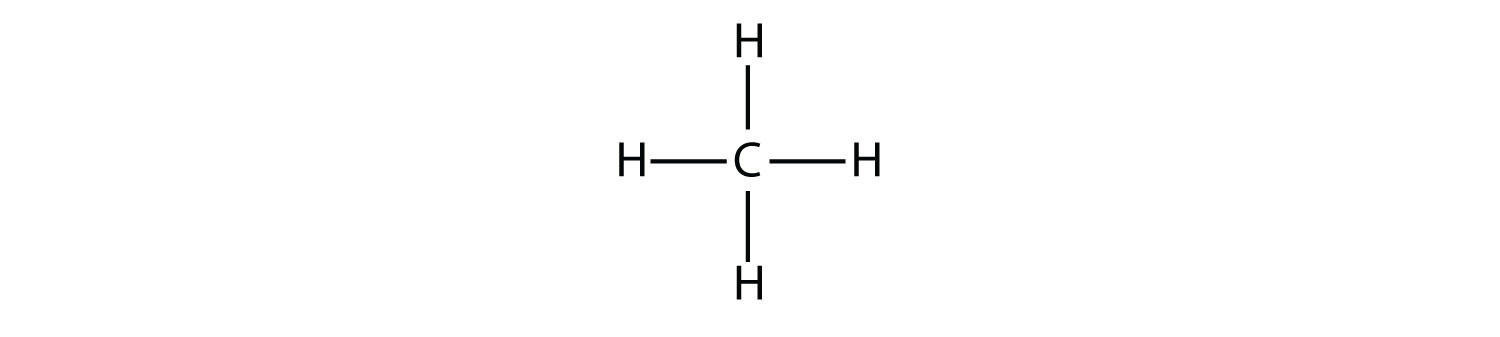
Наступний за величиною алкан має два атоми С, які ковалентно пов'язані один з одним. Щоб кожен атом С утворив чотири ковалентні зв'язки, кожен атом С повинен бути пов'язаний з трьома атомами Н. Отримана молекула, формула якої - С 2 Н 6, є етан:
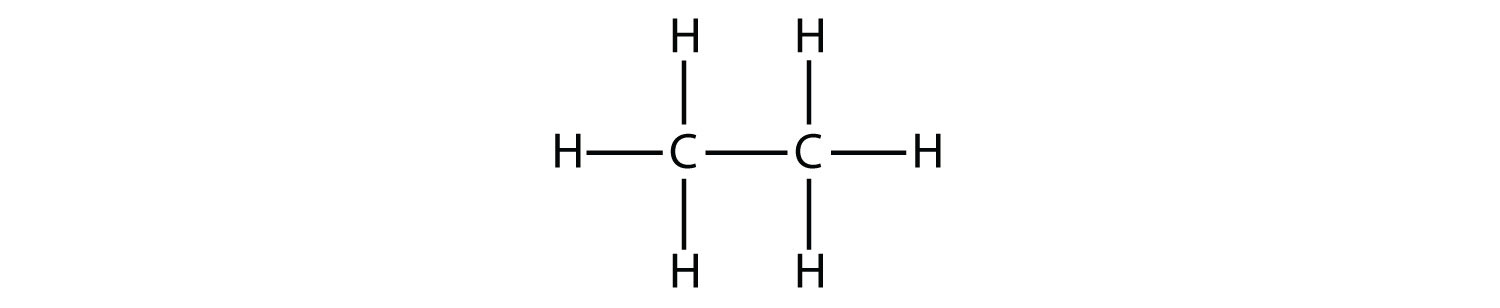
Пропан має кістяк з трьох атомів С, оточених атомами Н. Ви повинні бути в змозі переконатися, що молекулярна формула пропану становить C 3 H 8:
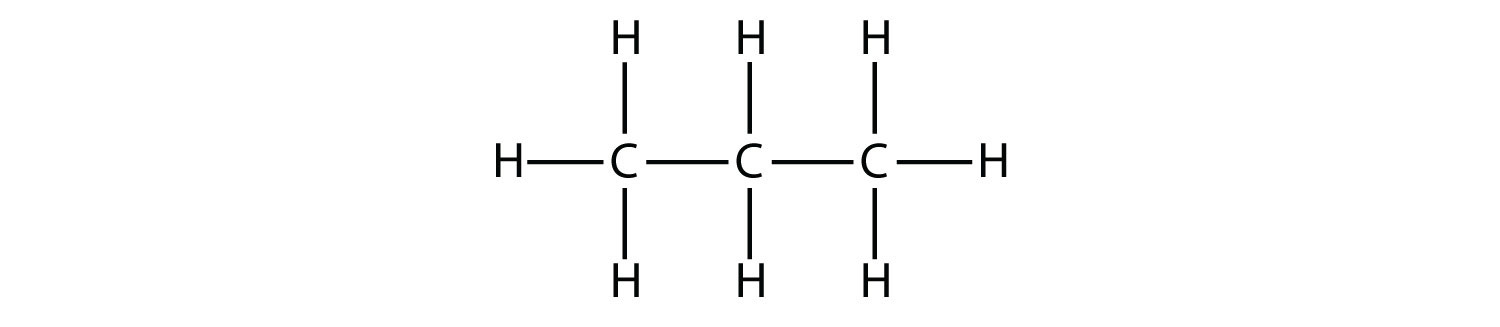
Діаграми, що представляють алкани, називаються структурними формулами, оскільки вони показують структуру молекули. У міру збільшення молекул структурні формули стають все більш складними. Один із способів цього полягає у використанні конденсованої структурної формули, яка перераховує формулу кожного атома С в кістці молекули. Наприклад, конденсована структурна формула для етану - СН 3 СН 3, тоді як для пропану - СН 3 СН 2 СН 3. Таблиця\(\PageIndex{1}\) - Перші 10 алканів, наводяться молекулярні формули, конденсовані структурні формули, а також назви перших 10 алканів.
| Молекулярна формула | Конденсована структурна формула | Ім'я |
|---|---|---|
| СН 4 | СН 4 | метан |
| С 2 Ч 6 | СН 3 СН 3 | етану |
| С 3 Ч 8 | СН 3 СН 2 СН 3 | пропан |
| З 4 Ч 10 | СН 3 СН 2 СН 2 СН 3 | бутан |
| З 5 Ч 12 | СН 3 СН 2 СН 2 СН 2 СН 3 | пентан |
| С 6 Ч 14 | СН 3 (СН 2) 4 СН 3 | гексан |
| С 7 Ч 16 | СН 3 (СН 2) 5 СН 3 | гептан |
| З 8 Ч 18 | СН 3 (СН 2) 6 СН 3 | октан |
| З 9 Ч 20 | СН 3 (СН 2) 7 СН 3 | нонан |
| С 10 Ч 22 | СН 3 (СН 2) 8 СН 3 | декан |
Оскільки алкани мають максимальну кількість атомів Н, можливих за правилами ковалентних зв'язків, алкани також називають насиченими вуглеводнями.
Алкени мають подвійний зв'язок C - C. Оскільки вони мають менше, ніж максимальна кількість можливих атомів Н, вони є ненасиченими вуглеводнями. Найменший алкен - етен - має два атоми С і також відомий своєю загальною назвою етилен:
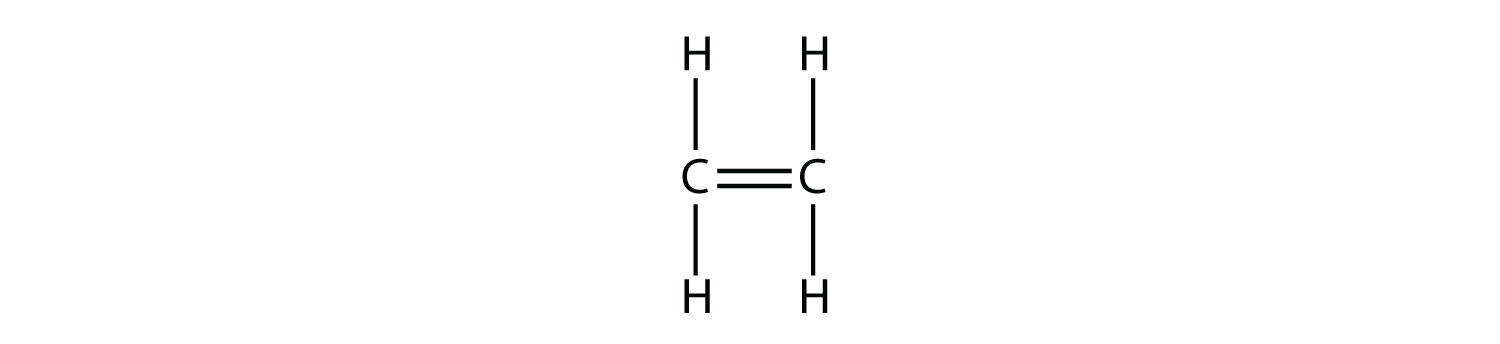
Наступний найбільший алкен - пропен - має три атоми С з подвійним зв'язком C - C між двома атомами С. Він також відомий як пропілен:
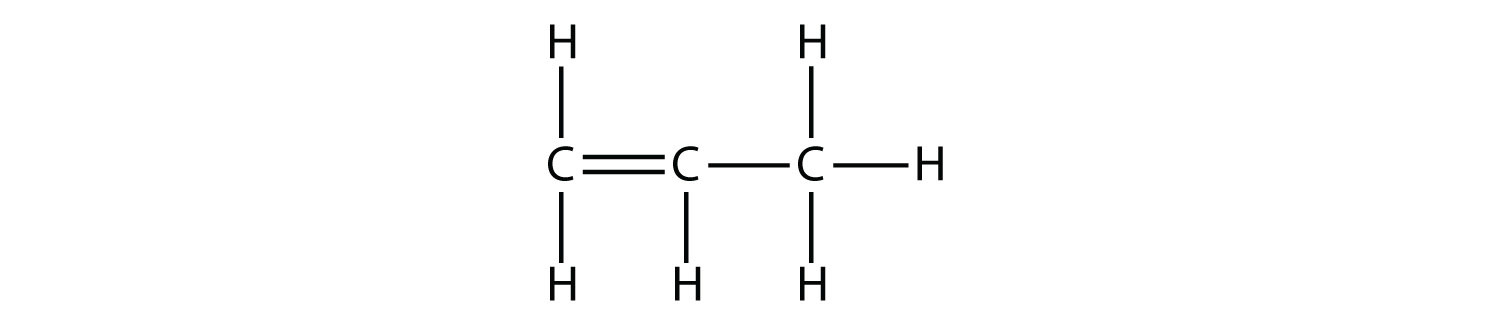
Що ви помічаєте з приводу назв алканів і алкенів? Назви алкенів такі ж, як і їх відповідні алкани, за винятком того, що закінчення - ene, а не - ane. Використання стебла для позначення кількості атомів С у молекулі та закінчення для представлення типу органічної сполуки є загальним явищем в органічній хімії, як ми побачимо.
З введенням наступного алкену, бутену, ми починаємо бачити основну проблему з органічними молекулами: вибір. З чотирма атомами C подвійний зв'язок C—C може переходити між першим і другим атомами С або між другим і третім атомами С:
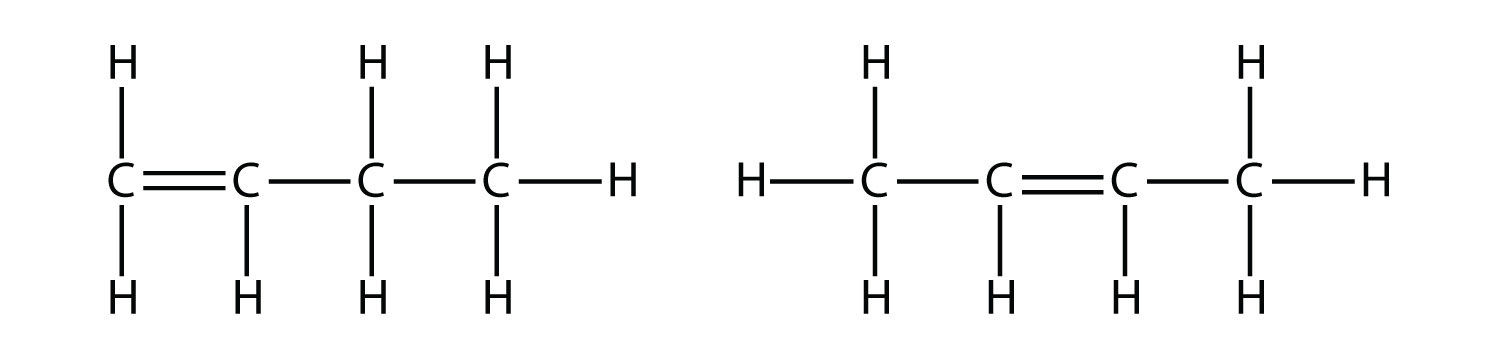
2 структурні формули для бутену, причому перший бутен має подвійний зв'язок на першому та другому вуглеці зліва, а останній має подвійний зв'язок на другому та третьому вуглеці зліва.
(Подвійний зв'язок між третім і четвертим атомами С такий же, як наявність його між першим і другим атомами С, тільки перевернутий.) Правила неймінга в органічній хімії вимагають, щоб ці дві речовини мали різні назви. Перша молекула називається 1-бутеном, а друга - 2-бутеном. Число на початку назви вказує, звідки бере початок подвійний зв'язок. Найменше можливе число використовується для нумерації ознаки в молекулі; отже, виклик другої молекули 3-бутену було б неправильним. Числа є загальними частинами органічних хімічних назв, оскільки вони вказують, який атом С в ланцюжку містить відмінну рису.
Сполуки 1-бутен і 2-бутен мають різні фізико-хімічні властивості, хоча вони мають однакову молекулярну формулу—C 4 H 8. Різні молекули з однаковою молекулярною формулою називаються ізомерами. Ізомери поширені в органічній хімії і сприяють її складності.
Виходячи з назв молекул бутену, запропонуйте назву цієї молекули.
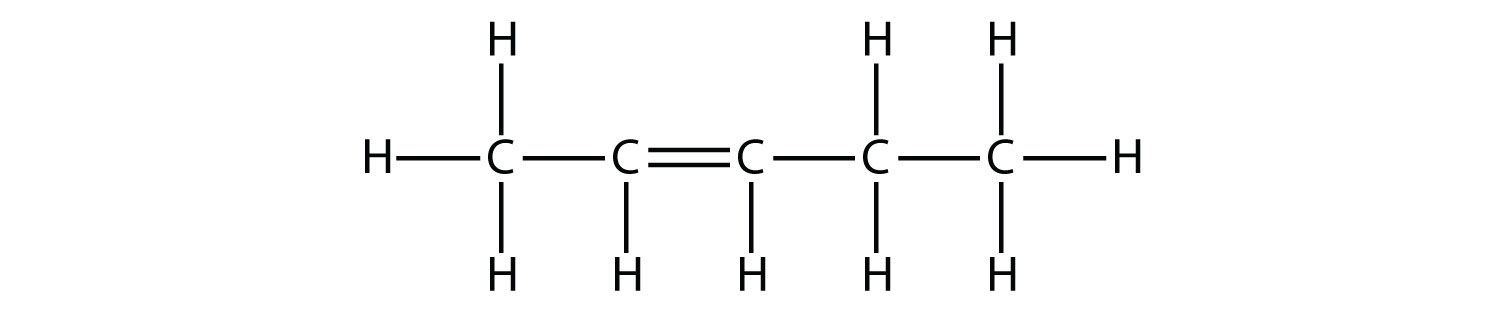
Рішення
З п'ятьма атомами С ми будемо використовувати пент - стовбур, а з подвійним зв'язком С—С це алкен, тому ця молекула є пентеном. При нумерації атомів С ми використовуємо число 2, оскільки це нижня можлива мітка. Так ця молекула називається 2-пентеном.
Виходячи з назв молекул бутену, запропонуйте назву цієї молекули.
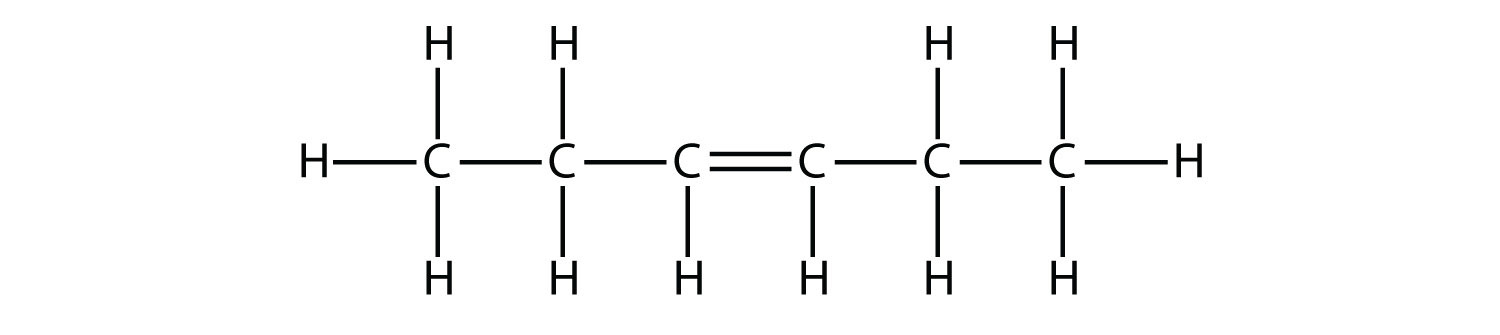
Структурна формула шести молекул вуглецю з подвійним зв'язком на третьому і четвертому вуглеці зліва. Всього існує дванадцять атомів водню.
- Відповідь
-
3-гексен
Алкіни, з потрійним зв'язком С—С, називаються аналогічно алкенам, за винятком того, що їх назви закінчуються на - yne. Найменшим алкіном є етин, який також відомий як ацетилен:
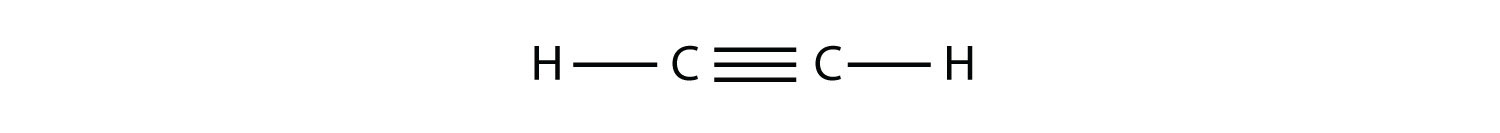
Пропін має будову
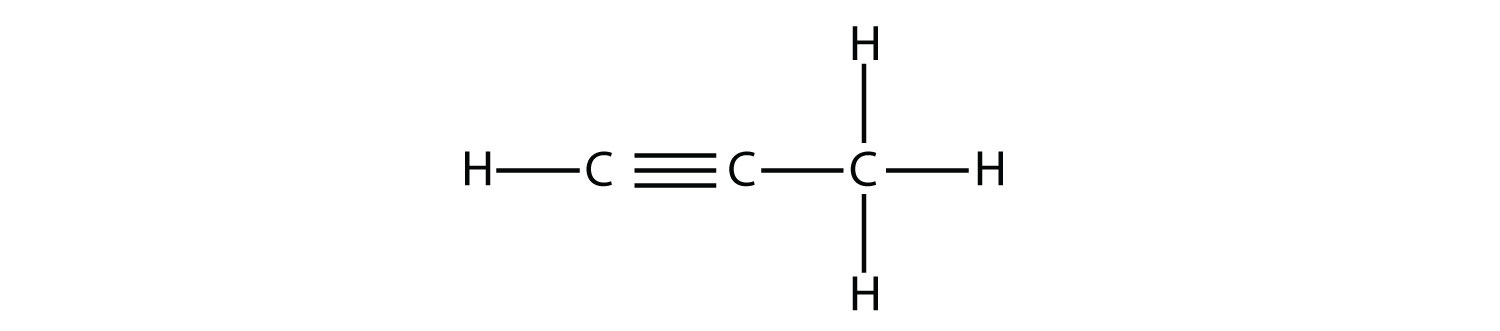
Структурна формула, що показує три молекули вуглецю з потрійним зв'язком, присутнім між першим і другим атомом вуглецю. Відповідна кількість атомів водню прикріплюється до кожного атома вуглецю.
З бутином нам потрібно почати нумерацію позиції потрійного зв'язку, так само, як ми це робили з алкенами:
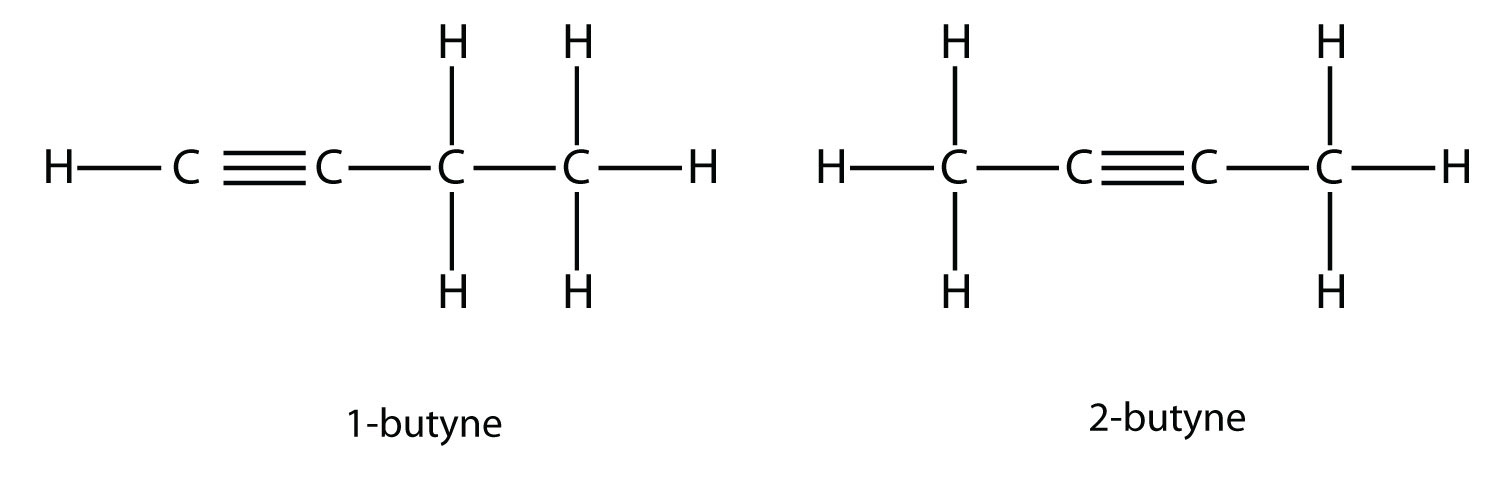
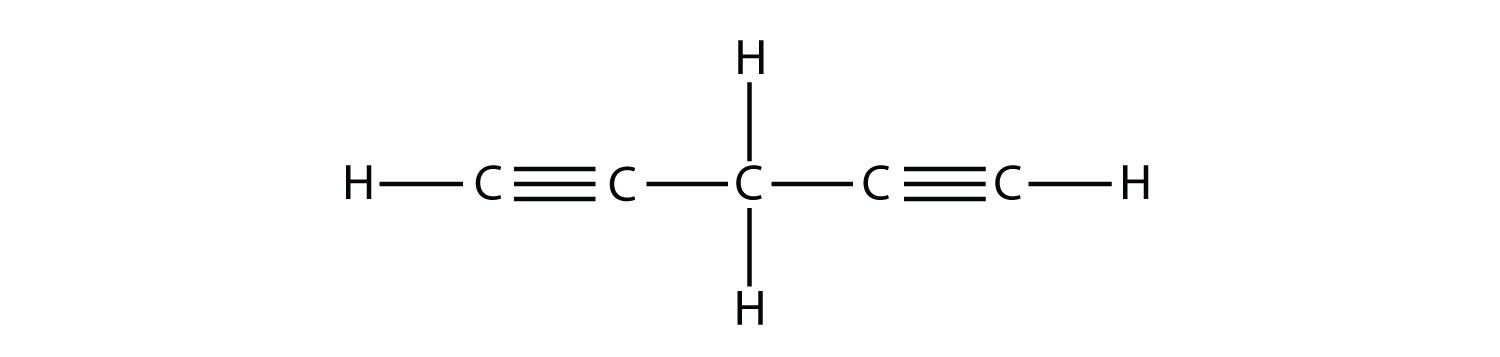
Дві структурні формули бутину. Один бутин має потрійний зв'язок між першим і другим атомом вуглецю, тоді як два бутина мають потрійний зв'язок між другим і третім атомом вуглецю.
Ароматичні сполуки містять бензольний агрегат. Сам бензол складається з шести атомів С в кільці, з чергуванням одинарних і подвійних зв'язків С—С:
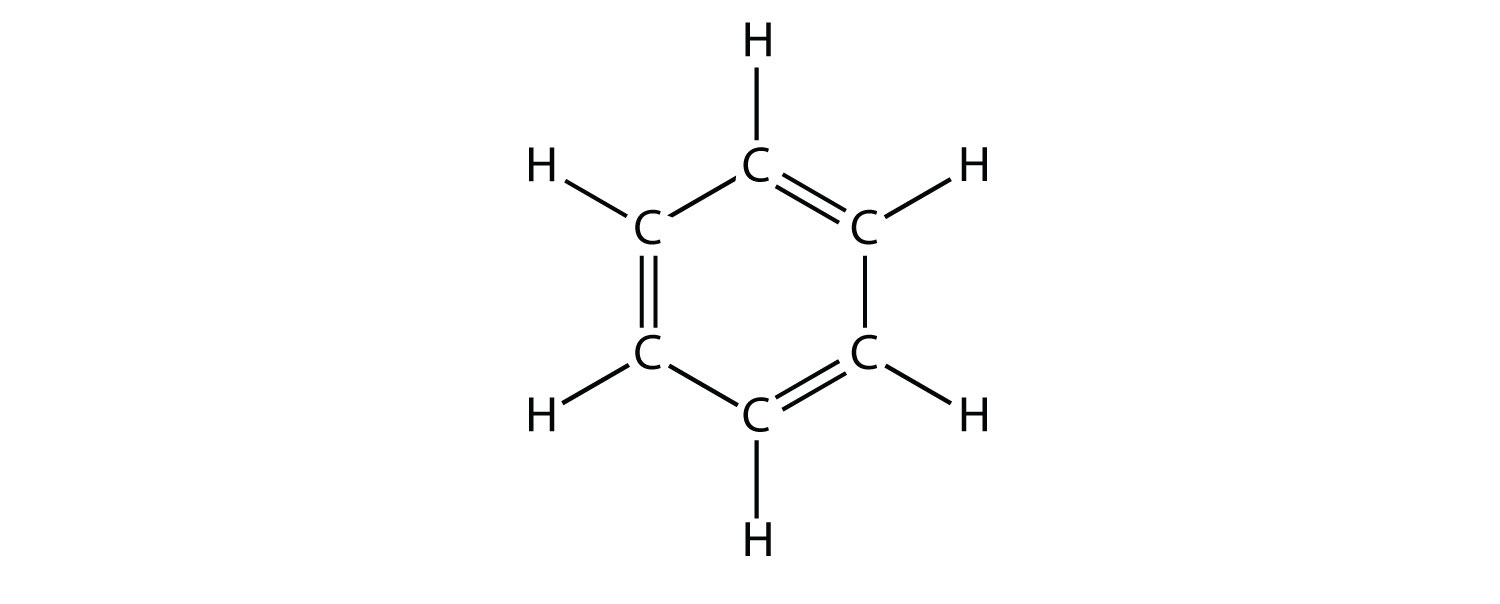
Шість вуглеців розташовані за схемою шестикутника з одним атомом водню, що виходить назовні від кожного атома вуглецю. Наявність подвійного зв'язку чергується між кожним іншим атомом вуглецю.
Чергуються одинарні та подвійні зв'язки С—С надають бензольному кільцю особливу стабільність, і воно не реагує як алкен, як можна підозрювати. Бензол має молекулярну формулу C 6 H 6; в більших ароматичних сполуках інший атом замінює один або кілька атомів Н.
Наскільки фундаментальними є вуглеводні для органічної хімії, їх властивості та хімічні реакції досить приземлені. Більшість вуглеводнів неполярні через близьку електронегативність атомів С і Н. Таким чином, вони розчиняються лише економно в Н 2 О та інших полярних розчинниках. Дрібні вуглеводні, такі як метан і етан, є газами кімнатної температури, тоді як більші вуглеводні, такі як гексан і октан, є рідинами. Ще більші вуглеводні є твердими речовинами при кімнатній температурі і мають м'яку воскоподібну консистенцію.
Вуглеводні досить нереактивні, але вони беруть участь у деяких класичних хімічних реакціях. Однією з поширених реакцій є заміщення атомом галогену шляхом об'єднання вуглеводню з елементарним галогеном. Світло іноді використовується для сприяння реакції, наприклад, ця між метаном та хлором:
\[CH_{4}+Cl_{2}\overset{light}{\rightarrow} CH_{3}Cl+HCl\nonumber \]
Галогени також можуть вступати в реакцію з алкенами і алкінами, але реакція інша. У цих випадках галоген реагує з подвійним або потрійним зв'язком C-C і вставляє себе на кожен атом С, що бере участь у множинних зв'язках. Ця реакція називається реакцією приєднання. Одним із прикладів є
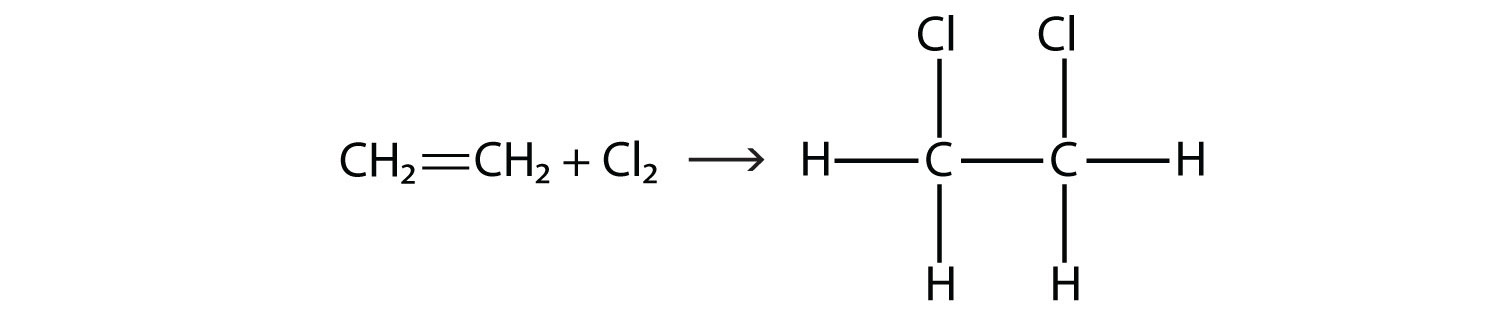
Умови реакції зазвичай м'які; у багатьох випадках галоген спонтанно реагує з алкеном або алкіном.
Водень також може бути доданий через множинний зв'язок; ця реакція називається реакцією гідрування. Однак у цьому випадку умови реакції можуть бути не м'якими; може знадобитися високий тиск газу Н 2. Платиновий або паладієвий каталізатор зазвичай використовується для того, щоб реакція протікала розумними темпами:
\[CH_{2}=CH_{2}+H_{2}\overset{metal\: catalyst}{\rightarrow} CH_{3}CH_{3}\nonumber \]
На сьогоднішній день найпоширенішою реакцією вуглеводнів є горіння, яке являє собою поєднання вуглеводню з O 2 для отримання СО 2 і Н 2 О. Згоряння вуглеводнів супроводжується виділенням енергії і є первинним джерелом виробництво енергії в нашому суспільстві (рис.\(\PageIndex{2}\) - Горіння). Реакція горіння для бензину, наприклад, яку можна представити С 8 Н 18, наступна:
\[2C^{8}H_{18}+25O_{2}\rightarrow 16CO_{2}+18H_{2}O+\sim 5060kJ\nonumber \]

Ключові винос
- Найпростіші органічні сполуки є вуглеводнями і складаються з вуглецю і водню.
- Вуглеводні можуть бути аліфатичними або ароматичними; аліфатичні вуглеводні діляться на алкани, алкени та алкіни.
- Спалювання вуглеводнів є первинним джерелом енергії для нашого суспільства.
- Визначте вуглеводневий. Які два загальних типи вуглеводнів?
- Які три різні типи аліфатичних вуглеводнів? Як вони визначаються?
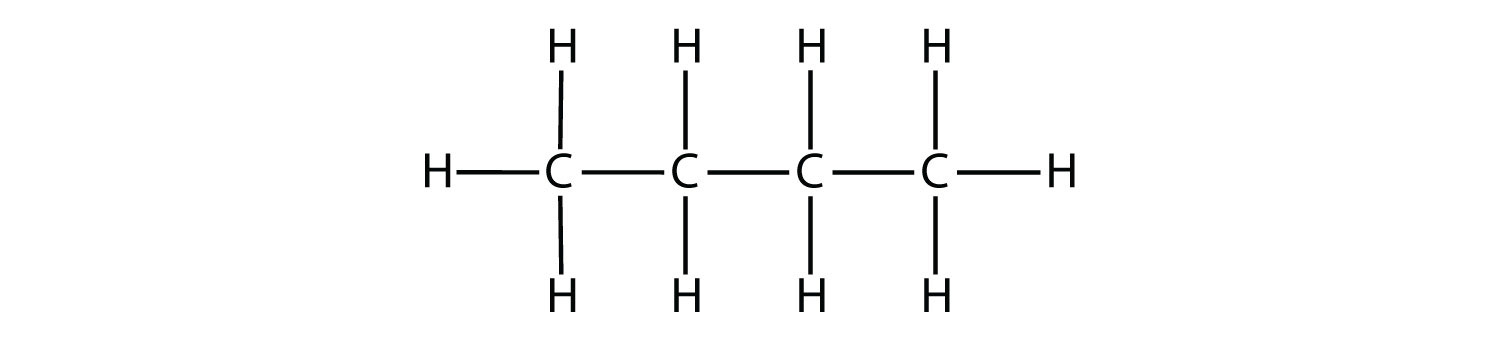
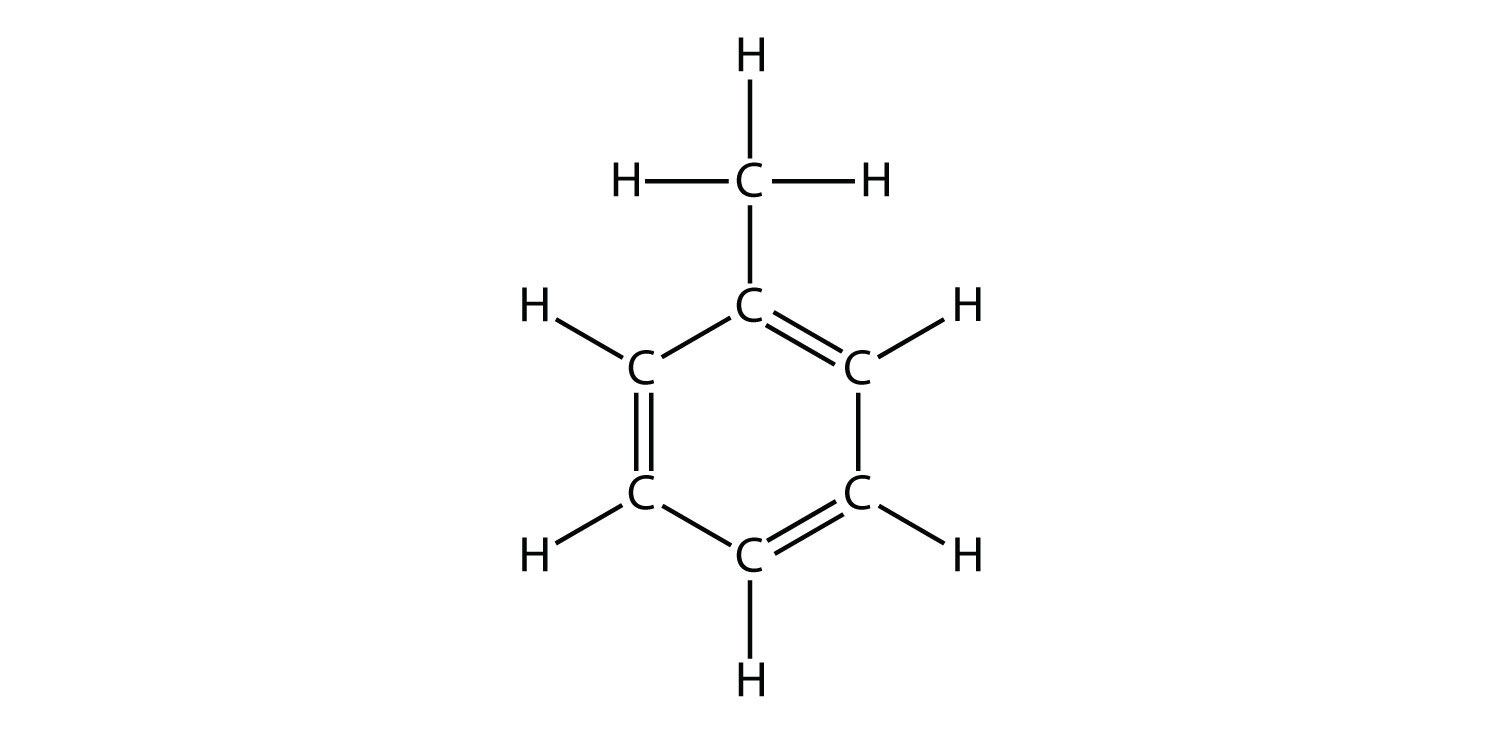
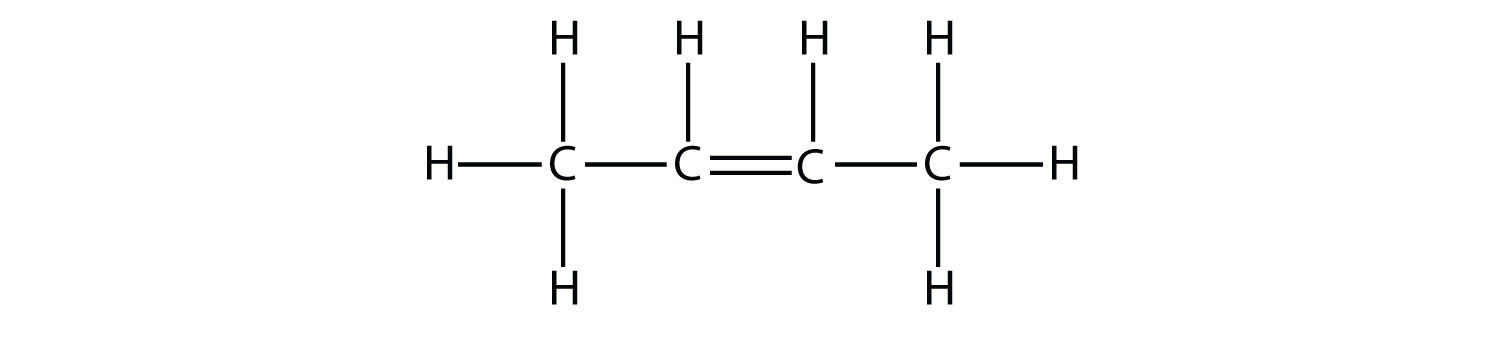
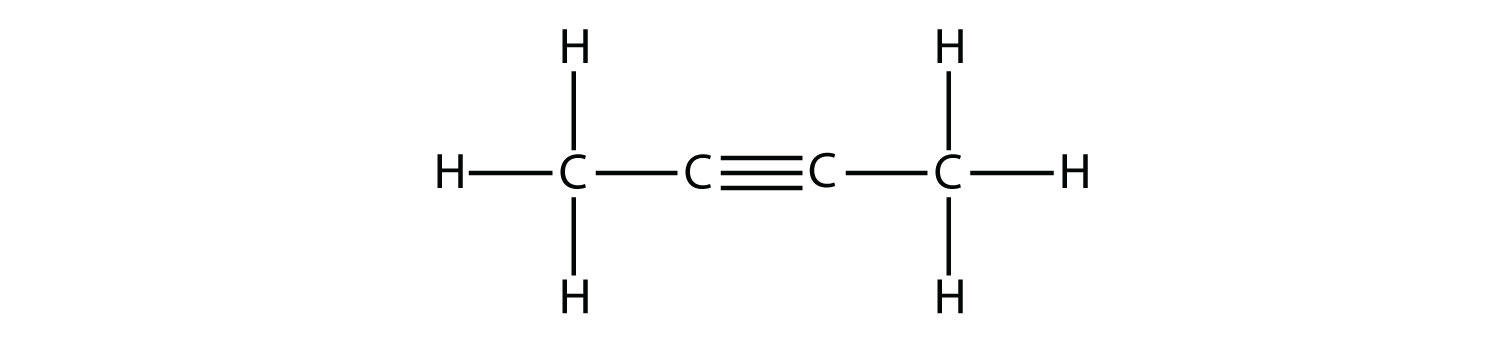
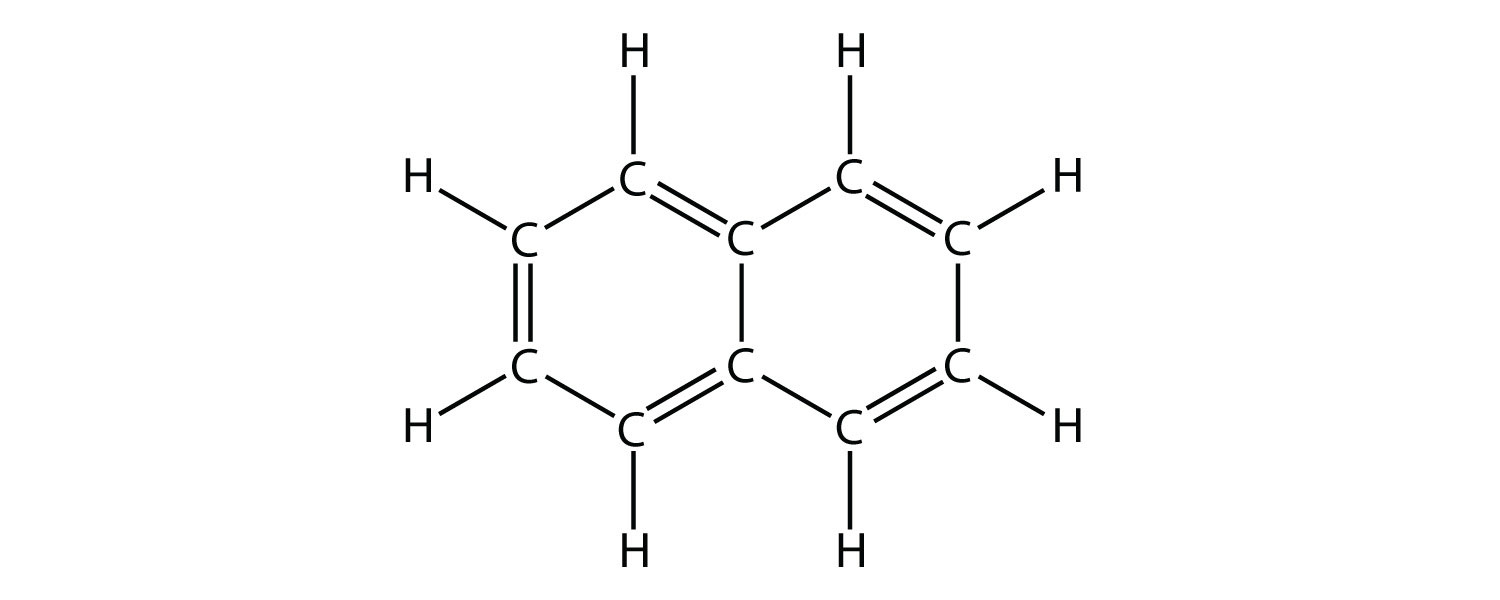
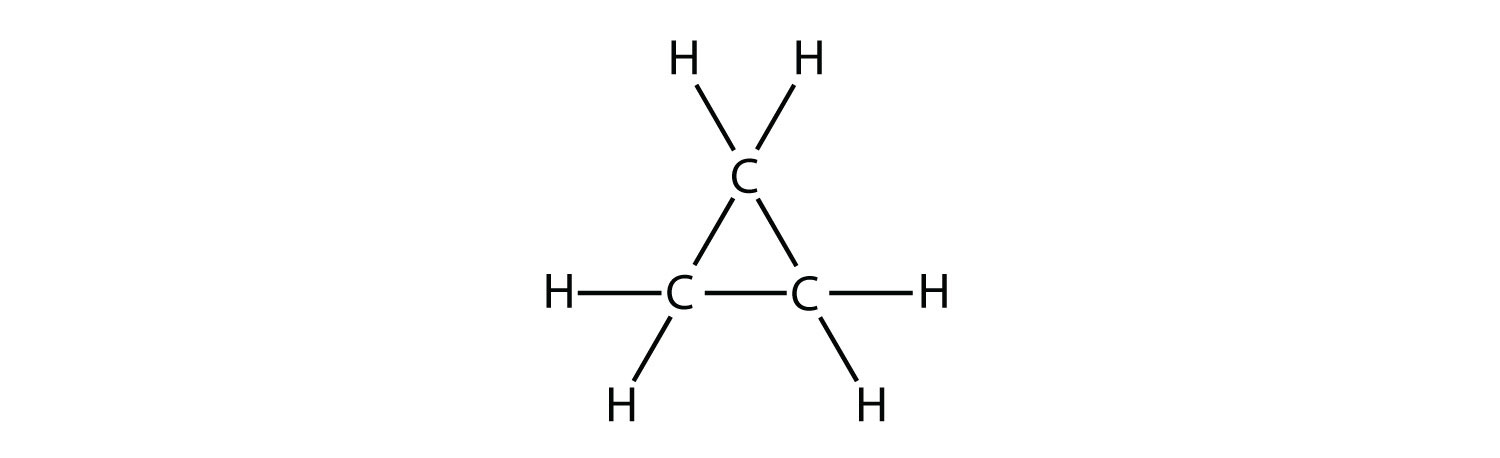
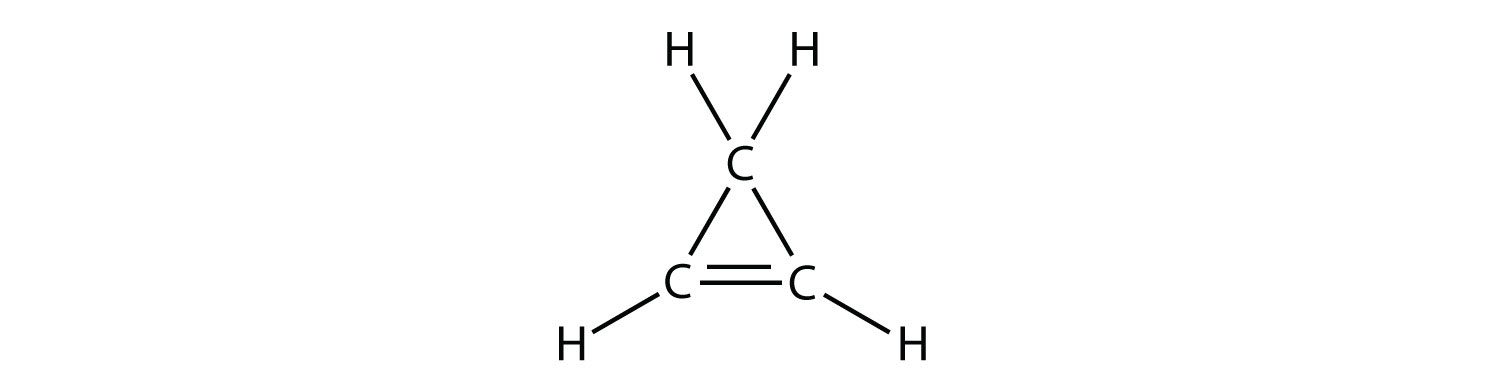
- Вкажіть, чи є кожна молекула аліфатичним або ароматичним вуглеводнем; якщо аліфатична, ідентифікуйте молекулу як алкан, алкен або алкін.
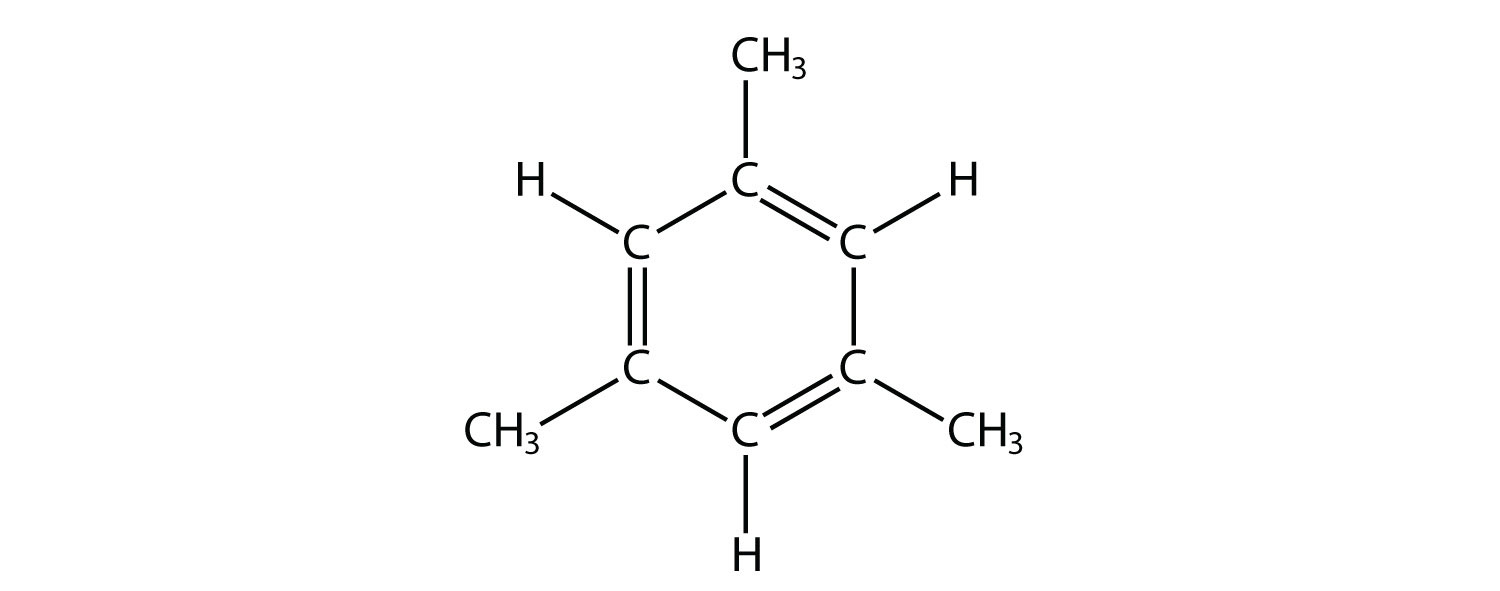
- Вкажіть, чи є кожна молекула аліфатичним або ароматичним вуглеводнем; якщо аліфатична, ідентифікуйте молекулу як алкан, алкен або алкін.
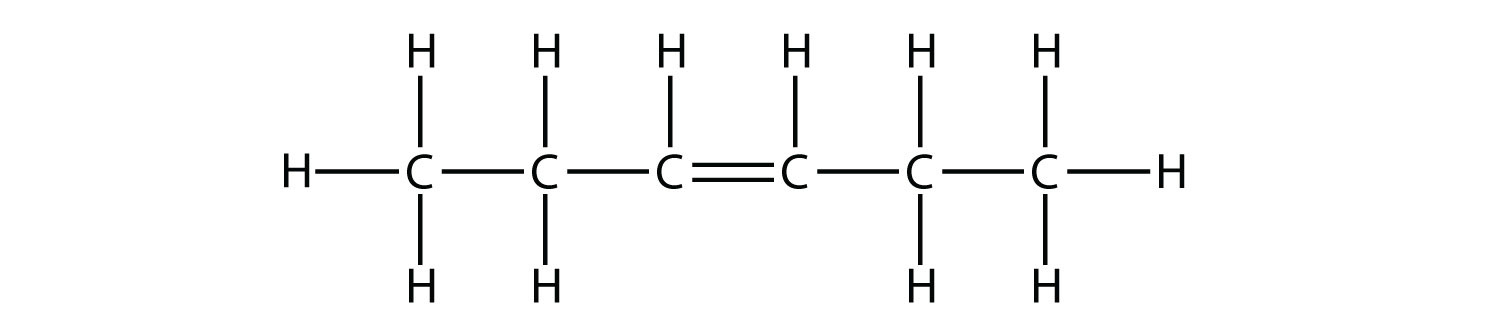
- Вкажіть, чи є кожна молекула аліфатичним або ароматичним вуглеводнем; якщо аліфатична, ідентифікуйте молекулу як алкан, алкен або алкін.
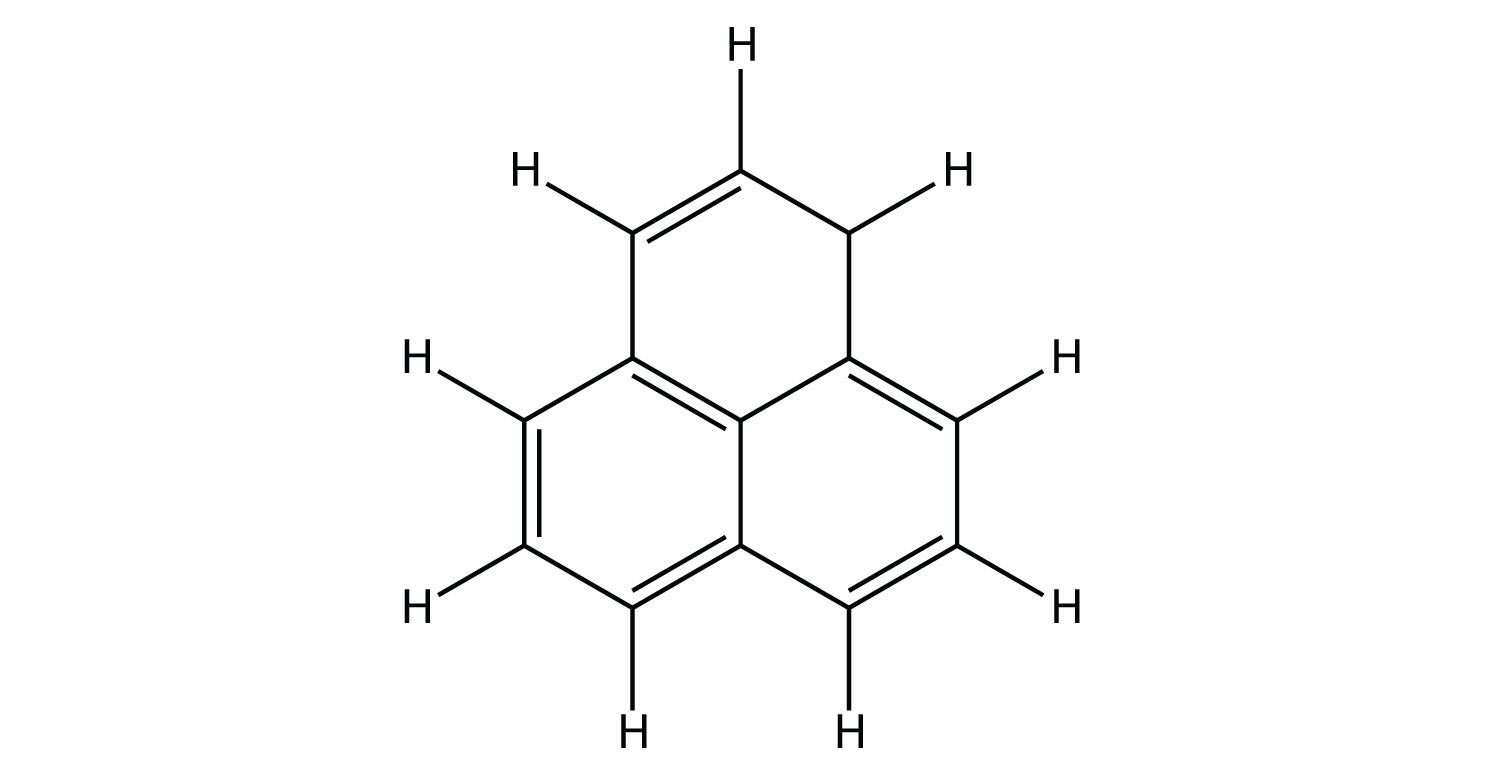
- Вкажіть, чи є кожна молекула аліфатичним або ароматичним вуглеводнем; якщо аліфатична, ідентифікуйте молекулу як алкан, алкен або алкін.
- Назвіть і намалюйте структурні формули для чотирьох найменших алканів.
- Назвіть і намалюйте структурні формули для чотирьох найменших алкенів.
- Що означає термін ароматичний про органічну молекулу?
- Що означає термін нормальний, коли використовується для алканів?
- Поясніть, чому назва 1-пропен невірно. Яке власне назва цієї молекули?
- Поясніть, чому назва 3-бутен невірно. Яке власне назва цієї молекули?
- Назвіть і намалюйте структурну формулу кожного ізомеру пентена.
- Назвіть і намалюйте структурну формулу кожного ізомеру гексину.
- Напишіть хімічне рівняння для реакції між метаном і бромом.
- Напишіть хімічне рівняння реакції між етаном і хлором.
- Намалюйте структуру продукту реакції брому з пропеном.
- Намалюйте структуру продукту реакції хлору з 2-бутеном.
- Намалюйте структуру продукту реакції водню з 1-бутеном.
- Намалюйте структуру продукту реакції водню з 1-бутеном.
- Напишіть збалансоване хімічне рівняння для згоряння гептану.
- Напишіть збалансоване хімічне рівняння для згоряння нонана.

Відповіді