6.3: Зв'язування ліганду
- Page ID
- 7412
Молекулярне розпізнавання є ключовим аспектом практично всієї біохімії і передбачає:
- Реплікація ДНК
- Генна регуляція
- Транскрипція ДНК в мРНК
- Переклад мРНК в білки
- Функція ферменту
- Молекулярна збірка
- Трансдукція сигналу
- Клітинно-клітинний зв'язок
- Імунологія
Міжмолекулярні взаємодії, в найпростішому прикладі, включають дві молекули, які розпізнають і зв'язуються один з одним:
- ліганд
- рецептор
Це широкі терміни, але загальні властивості рецептора і ліганду такі:
- Ліганд, як правило, є невеликою молекулою, і він дифундує по всьому навколишньому середовищу, поки не зв'язується з певним рецептором
- Рецептор, як правило, являє собою велику, відносно стаціонарну молекулу, яка містить специфічне місце зв'язування ліганду. При зв'язуванні ліганду структурні та/або хімічні властивості рецептора зазвичай змінюються
Взаємодія між рецептором і лігандом, як правило, не ковалентна
- Існує загальна молекулярна комплементарність між рецептором і лігандом.
- Часто, але не завжди, існує ентропна вартість, пов'язана з зв'язуванням ліганду з рецептором, але це з лишком компенсується сприятливою ентальпією (тобто молекулярною компліментарністю)
- Енергія зв'язування, як правило, використовується, щоб викликати структурні зміни, пов'язані з подією молекулярного зв'язку.
Існує два загальні методи дослідження взаємодій рецепторів/лігандів:
-
- Рівноважна термодинаміка, і
- Кінетика асоціації та дисоціації
Аналіз рівноважного зв'язування ліган/рецепторів
Два можливих стану взаємодії ліга/рецепторів та константи швидкості, пов'язані з їх утворенням, наведені як:
Константа рівноваги асоціації (освіти), K f, задається як:
- [RL] - концентрація комплексу, [R] - концентрація вільного R при рівновазі, а [L] - концентрація вільного L при рівновазі
- K f має одиниці М -1
- Велике значення для K f означає, що рівновага сприяє комплексу - спостерігається висока спорідненість рецептора до ліганду
- Невелике значення для K f означає, що рівновага сприяє поділу рецептора і ліганду, а рецептор має низьку спорідненість до ліганду.
Просто для того, щоб ускладнити життя, типовою рамкою відліку при описі спорідненості рецепторів до ліганду є посилання на константу дисоціації, K d:
- K d має одиниці М
- Невелике значення для K d означає, що рівновага сприяє комплексу - спостерігається висока спорідненість рецептора до ліганду
- Велике значення для K d означає, що рівновага сприяє поділу рецептора і ліганду, а рецептор має низьку спорідненість до ліганду
При рівновазі швидкість утворення комплексу RL дорівнює швидкості дисоціації:
Лівий вираз - це визначення константи дисоціації, K d, отже:
Вираз вільної енергії і K f і K d
З початкового вираження складного освіти:
Стандартна зміна вільної енергії стану, Δ G 0, для процесу (тобто починаючи з 1M все) буде дано як:
Оскільки K d - обернене K f:
У цьому випадку від'ємне значення для DG 0 (що вказує на спонтанність) виникне, коли K d < 1,0. Це станеться, коли є висока спорідненість і рівновага сприяє складному утворенню.
Практичні зв'язки між [R], [L], K d і [RL]
При однаковій концентрації доданого ліганду і рецептора буде відбуватися більш складне утворення при меншому значенні K d
Приклад 6.3.1
Рецептор і ліганд додають до загальної концентрації 1,0 х 10 -4 М. K d для комплексу RL становить 1,0 х 10 -4 М. Яка концентрація [R], [L] і [RL] при рівновазі?
.png)
Доданий ліганд, L, буде розділений між вільною та зв'язаною формами:
L всього = Л + РЛ = 1,0 х 10 -4 М
Д = 1,0 х 10 -4 М - РЛ
Аналогічно, доданий рецептор, R, буде розділений між вільною та пов'язаною формами:
R всього = R + RL = 1,0 х 10 -4 М
R = 1,0 х 10 -4 М - РЛ
Підстановка цих значень L і R у вираз для K d дає:
.png)
Це квадратика зі значеннями a = 1, b = -3,0 х 10 -4 і c = 1,0 х 10 -8. Це дає два можливі значення для RL:
RL = 2,62 Х 10 -4 М або
РЛ = 3,82 Х 10 -5
Оскільки максимально можливе значення для [RL] становить 1,0 х 10 -4 (тобто, враховуючи початкові концентрації R і L, це найбільша кількість RL, яка може бути сформована), перший результат неможливий і [RL] = 3,82 X 10 -5 M
Так, 38,2% доданого рецептора знаходиться в комплексоутворенні (тобто 3,82 Х 10 -5 М/1,0 х 10 -4) х 100%
Приклад 6.3.2
Така ж кількість доданих R і L, але на цей раз K d для комплексу RL становить 1,0 х 10 -6 М. Яка концентрація [R], [L] і [RL] при рівновазі?
.png)
це квадратика зі значеннями a = 1, b = -2,01 х 10 -4 і c = 1,0 х 10 -8. Це дає два можливі значення для RL:
RL = 1,11 Х 10 -4 М або
РЛ = 9,05 Х 10 -5
Оскільки максимально можливе значення для [RL] становить 1,0 х 10 -4 (тобто, враховуючи початкові концентрації R і L, це найбільша кількість RL, яка може бути сформована), перший результат неможливий і [RL] = 9,05 X 10 -5 M
Так, 90,5% доданого рецептора знаходиться в комплексоутворенні (тобто 9,05 Х 10 -5 М/1,0 х 10 -4) х 100%
При однаковій концентрації доданого ліганду і рецептора буде відбуватися більш складне утворення при меншому значенні K d
Визначення констант дисоціації (K d) або зв'язування (K f)
Співвідношення між K d, [R], [L] і [RL] задається:
- Це рівняння з чотирма змінними, якщо ви знаєте три з них, ви можете вирішити для четвертої
- В принципі, ви можете вирішити для K d, якщо ви знаєте концентрацію вільного рецептора [R], вільного ліганду [L] і рецептора/лігандного комплексу [RL] при рівновазі
Щоб мати можливість вирішити для K d, вам потрібен аналіз, який забезпечить молярні концентрації для кожного компонента. Однак цього, як правило, важко досягти. Набагато частіше є аналіз, який надасть вам інформацію щодо частки доданого рецептора (або ліганду), який присутній у вільній або складній формі.
- Якщо [R t] - загальна концентрація рецептора в зразку, ми знаємо, що він буде розділений на дві популяції - зв'язані і вільні:
- Фракція пов'язаних рецепторних сайтів задається співвідношенням:
- Фракція зв'язаних рецепторів відома змінною a, а має значення від 0 до 1
- Підставляючи значення на [R t] в терміні [R] та [RL], наведених вище, дає:
- Зв'язок між [RL] і K d задається виразом для Kd:
- Цей вираз для [RL] можна підставити у вираз для a to yield:
- Спростіть, попередньо розділивши через [R]:
- Потім множимо на K d:
Це рівняння має три змінні:
- Концентрація вільного ліганду при рівновазі [L]
- Константа дисоціації, K d, для комплексу RL
- Фракція рецептора, яка знаходиться в зв'язаній формі при рівновазі, а
Якщо ви знаєте дві з цих змінних, ви можете вирішити для третьої (тобто якщо експериментальний аналіз кількісно [L] і a, ви можете вирішити для K d)
Вищевказаним рівнянням можна маніпулювати далі шляхом підстановки значення a через [RL] і [R t]:
Це рівняння має чотири змінні:
- Концентрація вільного ліганду при рівновазі [L]
- Константа дисоціації, K d, для комплексу RL
- Концентрація рецептора, що знаходиться в зв'язаній формі при рівновазі [RL]
- Загальна концентрація рецептора в зразку
Зазвичай експеримент з зв'язування лігандів налаштований таким чином, що [Rt] тримається постійною, а [RL] контролюється як функція [L]
Це рівняння дуже схоже на рівняння Міхаеліса-Ментена:
Побудова V проти [S] в рівнянні М-М дає прямокутну гіперболу. Таким чином, побудова графіка [RL] проти [L] також дасть прямокутну гіперболу
- Асимптота кривої дасть значення [R t]
- Концентрація вільного ліганду [L], що призводить до половини максимального значення [RL], дорівнює значенню K d
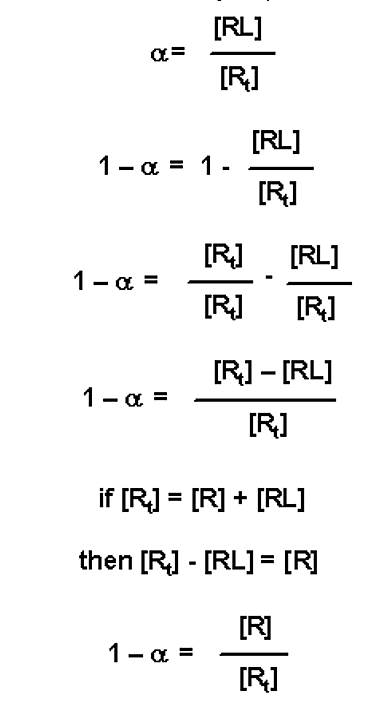
Ще одна модифікація полягає в тому, щоб зрозуміти, що якщо a дорівнює частці рецептора, пов'язаного в комплексі (зі значенням 0 ≤ α ≤ 1,0), то (1 - α) є часткою вільного рецептора (тобто фракції незв'язаного рецептора)
.png)
Це значення можна підставити в три змінні вирази вище:
.png)
Це рівняння має чотири змінні:
- Концентрація вільного ліганду при рівновазі [L]
- Константа дисоціації, K d, для комплексу RL
- Концентрація рецептора, що знаходиться у вільній формі при рівновазі [R]
- Загальна концентрація рецептора в зразку [R t]
Зазвичай експеримент з зв'язування лігандів налаштований таким чином, що [Rt] тримається постійною, а [R] контролюється як функція [L]
(Примітка: Хоча це виглядає як рівняння М-М, K d є постійною.)
Наведені вище похідні називаються "зв'язуючими ізотермами" у зв'язку з їх здатністю вирішувати для Kd в умовах рівноваги (і вихідне рівноважне термодинамічне рівняння використовується постійна температура)
.png)
Побудова даних для різних значень [L], [R t], і або [RL] або [R], і підгонка до відповідної функції вище, дозволяє більш точно визначити K d (хоча один експеримент дасть відповідь).
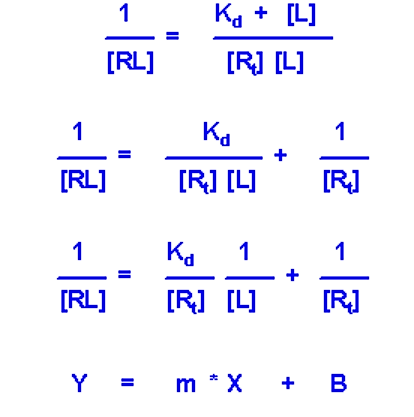
Через схожість графіка [RL] проти [L] з графіком М-М, це часто є більш бажаною експериментальною установкою. Зокрема, для більш точного визначення K d може бути використаний подвійно-зворотний графік (так само, як і двозворотний М-М графік)
.png)
- Якщо ви намалюєте 1/ [RL] проти 1/ [L], ви отримаєте пряму лінію, нахил якої дорівнює K d/[R t]
- Перехоплення Y буде дорівнює 1/ [R t]. Оскільки це значення фіксоване і відоме, значення перехоплення y може служити перевіркою, щоб переконатися, що експеримент відповідає моделі
Експеримент рівноважного діалізу
Напівпроникна мембрана може бути використана в експерименті з рівноваги на основі діалізу для визначення Kd для пари ліганд-рецепторів.
- Мембрана повинна бути вільно проникною, що стосується ліганду (зазвичай це невелика молекула), але представляти бар'єр для рецептора
- Експеримент встановлюється з відомою концентрацією рецептора з одного боку, а відомою концентрацією ліганду - з іншого
- Системі дозволено прийти до рівноваги
- Експеримент вимагає проведення аналізу на ліганд
.png)
Малюнок 6.3.1: Напівпроникний бар'єр
Після досягнення рівноваги оцінюють концентрацію ліганду по обидва боки напівпроникної мембрани:
.png)
Малюнок 6.3.2: Концентрація рівнова
- Оскільки ліганд не впливає на мембрану, концентрація ліганду на стороні без рецептора дорівнює концентрації вільного ліганду [L] скрізь у зразку (тобто по обидва боки мембрани)
- Концентрація ліганду буде дорівнює концентрації вільного ліганду [L] плюс ліганд, присутній в рецепторному комплексі [RL] (іншими словами, повинна бути більша концентрація ліганду на стороні з рецептором, якщо рецептор має спорідненість до ліганду)
- Концентрацію рецептор/лігандного комплексу [RL] можна визначити за різницею між цими двома значеннями
- Загальна концентрація рецепторів - відома величина (експериментатор визначається на початку експерименту, і не змінюється)
- Будь-яка ізотерма зв'язування може бути використана для вирішення для K d (оскільки [R] також може бути визначено)
