4.3: Використання видобутку
- Page ID
- 21346
Є кілька причин використовувати екстракцію в хімічній лабораторії. Це основний метод виділення сполук з рослинної сировини. Екстракція переміщує сполуки з однієї рідини в іншу, так що ними можна легше маніпулювати або концентрувати. Це також дозволяє вибірково видаляти компоненти в суміші.
Витяг природних сполук
Плоди та листя рослин в основному складаються з целюлози та води, але також містять «ефірні олії». жирна суміш сполук, які захоплюють «сутність» запаху та смаку рослинного матеріалу. Апельсинова олія - це приблизно\(95\%\) лімонен (рис. 4.3b), і завдяки своїй неполярній структурі його можна витягти з шкірки в органічний розчинник, такий як гексани або дихлорметан (рис. 4.3а). Потім масло можна концентрувати і використовувати для ароматизації або аромату продуктів, засобів для чищення та свічок.
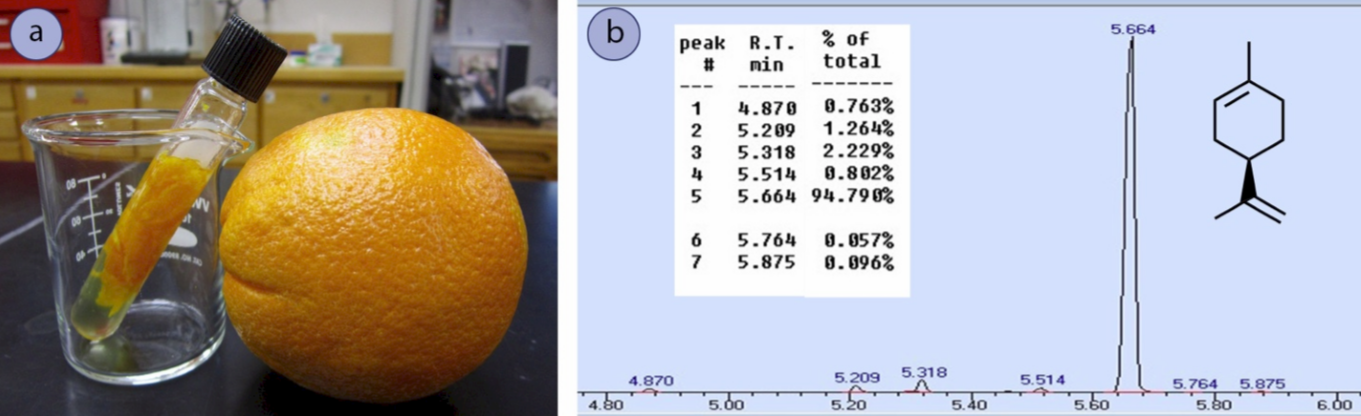
Малюнок 4.3: а) Помаранчева шкірка, витягнута в дихлорметан, б) спектр GC апельсинової олії.
У хімічній лабораторії ефірні олії часто витягуються з їх джерела за допомогою розчинників та аналізуються за допомогою газової хроматографії або спектроскопії.
Перенесення сполук з шарів
Ще один спосіб вилучення ефірних масел з запашних рослинних матеріалів - за допомогою парової дистиляції (рис. 4.4б). Цей процес часто призводить до прекрасних пахнуть сполук, підвішених у водному дистиляті (рис. 4.4c). Для того, щоб сконцентрувати масло, водну суспензію часто екстрагують низькокиплячим органічним розчинником (рис. 4.4d), який потім можна легко видалити з масла.
.png)
Малюнок 4.4: а) Цільна гвоздика, б) Парова перегонка гвоздики, в) Молочний дистилят, що складається з олії та води, г) Використання екстракції для відділення масла від води.
Вибіркове видалення компонентів
При проведенні експерименту, який синтезує хімічний продукт, реакція часто завершується всякий раз, коли припиняється перемішування або нагрівання. І все ж, етапів у процедурі завжди більше! Те, що зазвичай відбувається безпосередньо після цього, - це «пропрацювати» реакцію певним чином. Обробка відноситься до методів, спрямованих на виділення продукту з реакційної суміші, і часто починається з використання сепараторної воронки і екстракцій.

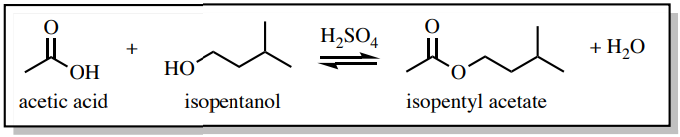
Наприклад, уявіть, що оцтова кислота і ізопентанол нагрівали в присутності кислотного каталізатора протягом однієї години (рис. 4.5), щоб зробити ізопентилацетат - складний ефір, який пахне бананами (див. Схему реакції на рис. 4.6). Після одногодинного періоду часу, на жаль, є не тільки банановий запах ефіру в колбі. Колба також буде містити побічні продукти (вода в даному випадку), залишки вихідних матеріалів, якщо реакція неповна, а також будь-які використовувані каталізатори (\(\ce{H_2SO_4}\)в даному випадку). У цьому прикладі може бути п'ять з'єднань в реакційній колбі після припинення нагрівання (рис. 4.7)!
При «відпрацюванні» цієї реакції отриману суміш часто виливають в сепараторну воронку разом з деякою кількістю води і органічного розчинника. При цьому утворюється два шари в сепараторній воронці: водний шар і органічний шар.
Після струшування цієї неоднорідної суміші сполуки розподіляються самостійно виходячи з їх розчинності. Сполуки, які мають високу розчинність у воді, сприяють водному шару, тоді як менш полярні сполуки сприяють органічному шару. У цьому прикладі кислотний каталізатор та залишкова карбонова кислота або спирт, швидше за все, будуть втягнуті у водний шар. Ефір мав би більшу спорідненість до органічного шару, ніж водний шар, викликаючи його виділення від інших компонентів в реакційній суміші (рис. 4.7).
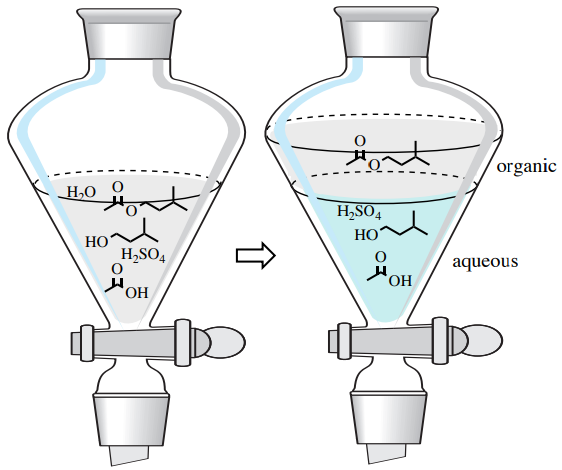
У цьому прикладі можливо, що невеликі кількості спирту також втягуються в органічний шар, але їх, швидше за все, можна було б видалити водою «змити». Під час промивання бажана сполука (наприклад, ізопентилацетат) залишається у своєму поточному шарі сепараторної воронки (в даному прикладі органічного шару), і небажані сполуки видаляються або «змиваються» в інший шар (наприклад, водний шар). Промивання відрізняється від екстракції, оскільки при екстракції бажана сполука рухається від свого поточного місця (тобто рухається від водного шару до органічного шару), тоді як при промиванні бажана сполука залишається у своєму поточному шарі.
