8: Стратегії синтезу Cedrene
- Page ID
- 24267
Cedrene являє собою дуже складний трициклічний сесквітерпен. Така складність вимагала геніальних підходів до тотального синтезу кільцевої системи. Для цієї кільцевої системи повідомляється кілька синтезів. Ми б обговорили кілька підходів. Деякі стратегічні розщеплення зв'язків показані у вигляді ламаних ліній на малюнку 8.1.
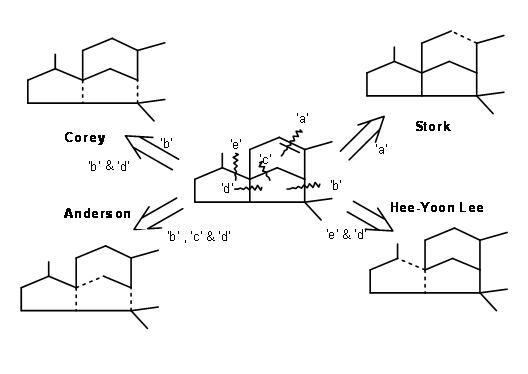
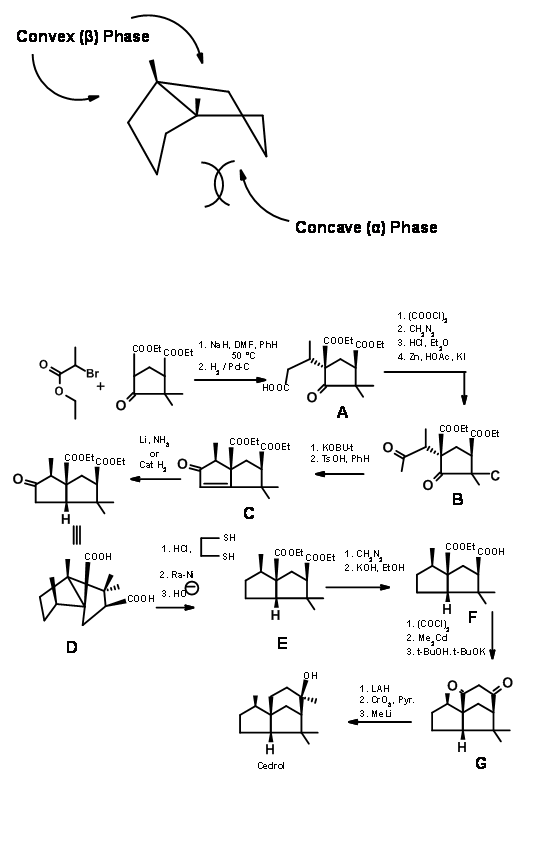
Відключення на 'a': Г.Лелека та ін., (J. Am. Хім. Soc., 77, 1078 (1955); там же, 83, 3114 (1961)) скористався тим, що сплавлені п'ять членів кільця будуть цис-сплавлені. Така система мала б переповнену «увігнуту фазу». Ці дві особливості лягли в основу синтезу Лелеки Кедрену. Їх синтетична схема показана на малюнку 8.2. Перше алкілування приводить в рух, стерик виходить з решти ступенів.
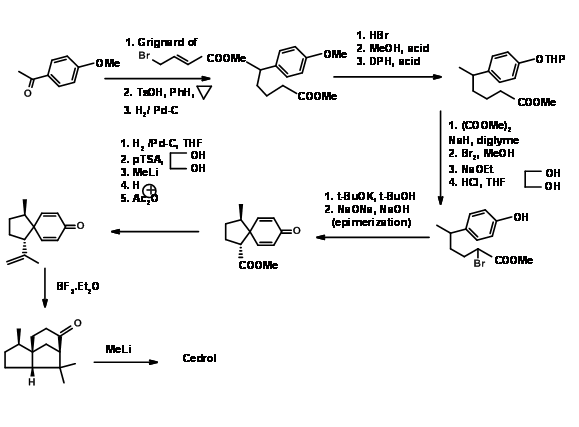
Відключення на 'b': За його синтез Седрене 1969 (J. Am. Хім. Соц., 91, 1557 (1969)), Корі створив спіро-кільцеву систему (розщеплення зв'язку 'b'). А р- алкілування фенолату дало спіро-кільце (J. Am. Хім. Соц., 84, 788 (1962)). Льюїс каталізував цилізацію енолату завершив скелет (рис. 8.3).
Відключення на 'b' і 'd': На основі концепції біогенетичної циклізації Корі досяг одноетапної циклізації кілець A і B (рис. 8.4) на попередньо сформованому кільці С (Tet. Летт., 2455 (1972). Ключем до успіху в цій схемі є попереднє формування облігації 'd' з подальшим утворенням облігації 'b'. Зверніть увагу на роль циклопропілкетону, який організував розвиток іона карбонію з подальшим початковим карбонієм для завершення кілець A і B в такому порядку.
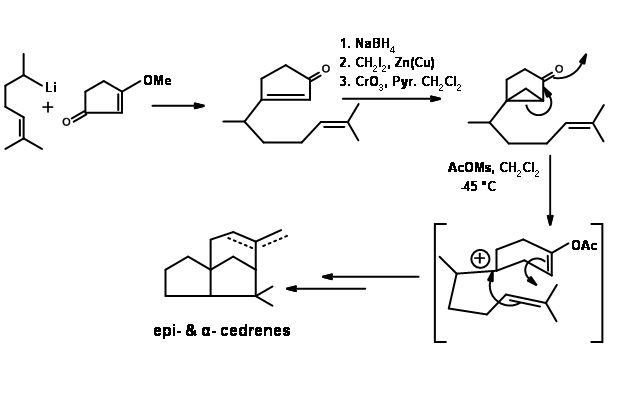
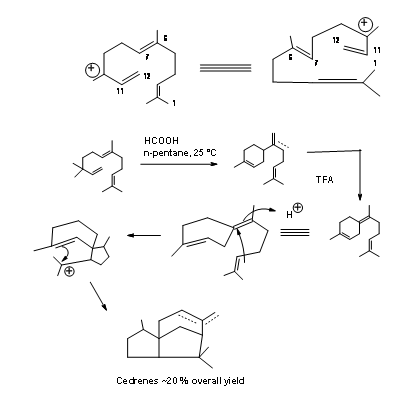
Циклізація біогенетичного типу: Чудова циклізація біогенетичного типу Nerolidol до Cedrene повідомила Андерсон et.al. , (Тет. Летт., 2455 (1972). Циклізація може бути здійснена в два етапи. З мурашиною кислотою спочатку утворюється шестичленне кільце. Подальші обробки трифлурооцтової кислотою завершили синтез. Загальна врожайність була дуже помірною (рис. 8.5).
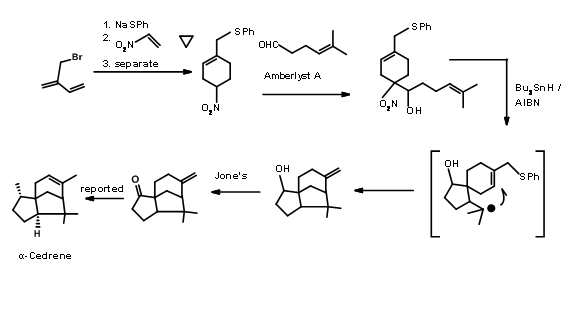
Відключення у зв'язках 'e' та 'd': У циклізації біогенетичного типу Андерсона вперше було реалізовано формування шестичленного кільця С. Шестичленна кільцева система також послужила ключовим кроком для вільної радикальної циклізації, про яку повідомив Хі-Юн Лі. Тандем радикальної циклізації була їх центральною темою. Повідомлялося про такі радикальні циклізації для синтезу натуральних продуктів. Хі-Юн Лі повідомив про застосування цієї стратегії до синтезу α-кедрену (Ter. Летт., 7713 (1998). Успіх цієї схеми залежать від двох факторів.
- Селективне формування радикала для формування зв'язку 'd' для виконання В-кільця
- Акцептор вуглецю повинен генерувати новий вільний радикал в процесі завершення кільця А. Перше завдання було досягнуто шляхом включення ксантанового блоку, а друге важливе завдання було виконано через., N-азиридиніліміну групи. Синтетична схема показана на малюнку 8.6.

Відключення на 'b' і 'd': підхід Чень і т.д., (Тет. Lett., 2961 (1993)) спирався на реакцію циклізації вільних радикалів на відповідним чином фукціоналізоване кільце С (рис. 8.7). Синтез кільця С досягається за допомогою., реакція DA. Новенагальная реакція поміщала необхідний ланцюжок для комплектації кілець А і В. Зниження гідриду олова породило вільний радикал на місці нітрогрупи, який зазнав тандемної циклізації для завершення кілець A і B в такому порядку.
Про підхід Дільса-Альдера до трициклічного кедрену скелет повідомили Breitholle et.al., (Кан. Хім., 54, 1991 (1976) (рис. 8.8). Алкілування циклобутадієну до необхідного ланцюга дало 8,8А після рівноваги. Реакція DA протікала з виходом 36% з отриманням суміші ізомерів. Кетон 8.8B не зазнав кільцевого розширення діазометаном. Розширення кільця було нарешті досягнуто за допомогою метиленового аміну 8.8C за допомогою діазотизації. Той факт, що два продукти розширення кільця 8.8D та 8.8E були сформовані з 8.8D як основний продукт, свідчить про те, що амін 8.8F був основним ізомером.
