1.5: Правило октету - іонне та ковалентне склеювання (огляд)
- Page ID
- 22832
Мета навчання
Малюйте, інтерпретуйте та перетворюйте між структурами Льюїса (Kekule), конденсованих та ліній зв'язку
Примітка: Огляд загальної хімії в розділах 1.3 - 1.6 інтегрований у вищезазначену ціль навчання з органічної хімії в розділах 1.7 та 1.8.
Для органічної хімії акцент робиться на хімії вуглецю. Хімія вуглецю стає більш цікавою, коли вуглець пов'язаний з киснем та/або азотом або іншими гетероатомами, атомами, які НЕ є вуглецем або воднем. Тому правило октету є сильним фактором органічної хімії і порушується лише невуглецевими елементами, такими як водень, бор, алюміній, сірка та фосфор.
Чому одні речовини хімічно пов'язані молекули, а інші є асоціацією іонів? Відповідь на це питання залежить від електронних структур атомів і природи хімічних сил всередині сполук. Хоча різко визначених меж немає, хімічні зв'язки, як правило, класифікуються на три основні типи: іонні зв'язки, ковалентні зв'язки та металеві зв'язки. У цьому розділі буде розглянуто кожен тип зв'язку та загальні властивості, виявлені у типових речовин, в яких зустрічається тип зв'язку
- Іонні зв'язки виникають в результаті електростатичних сил, які існують між іонами протилежного заряду. Ці зв'язки, як правило, включає в себе метал з неметалевим
- Ковалентні зв'язки виникають внаслідок спільного використання електронів між двома атомами. Облігації, як правило, включають один неметалічний елемент з іншим.
- Металеві зв'язки Ці зв'язки знаходяться в твердих металах (мідь, залізо, алюміній) з кожним металом, пов'язаним з декількома сусідніми групами і зв'язуючи електрони вільно переміщатися по всій тривимірній структурі.
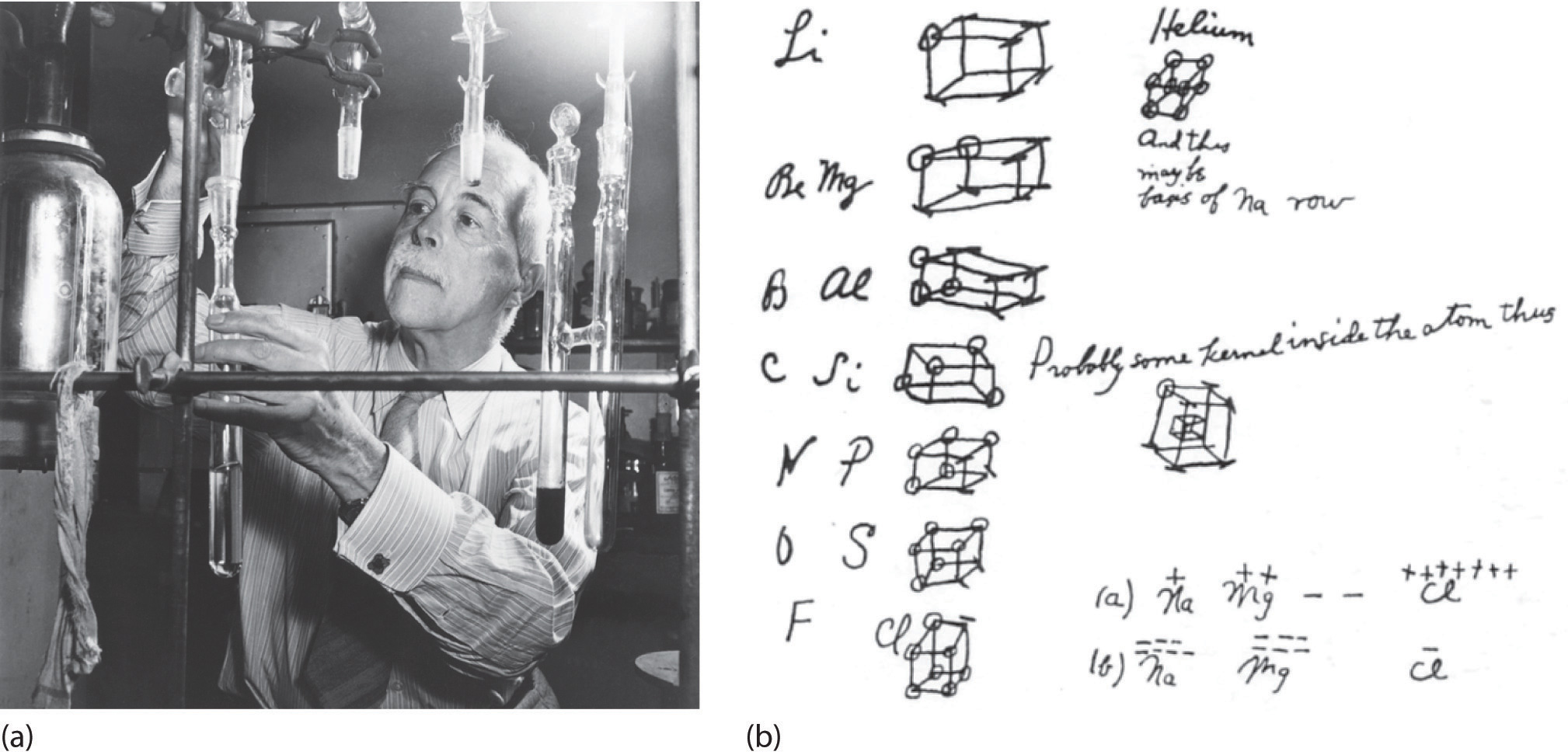
Правило октету
У 1904 році Річард Абегг сформулював те, що зараз відомо як правило Абегга, яке стверджує, що різниця між максимальною позитивною та негативною валентністю елемента часто становить вісім. Це правило було використано пізніше в 1916 році, коли Гілберт Н. Льюїс сформулював «правило октета» у своїй теорії кубічних атомів. Правило октету посилається на тенденцію атомів віддавати перевагу мати вісім електронів у валентній оболонці. Коли атоми мають менше восьми електронів, вони, як правило, реагують і утворюють більш стійкі сполуки. Атоми будуть реагувати, щоб потрапити в максимально стійкий стан з можливих. Повний октет дуже стабільний, тому що всі орбіталі будуть заповнені. Атоми з більшою стабільністю мають меншу енергію, тому реакція, що збільшує стабільність атомів, вивільнить енергію у вигляді тепла або світла; реакції, що знижують стабільність, повинні поглинати енергію, стаючи холодніше.
Правило октету: Атоми часто набирають, втрачають або ділять електрони, щоб досягти такої ж кількості електронів, як благородний газ, найближчий до них у періодичній таблиці.
При обговоренні правила октету ми не розглядаємо d або f електронів. У правилі октета беруть участь тільки електрони s і p, що робить його корисним правилом для елементів основної групи (елементів не в перехідному металі або внутрішньо-перехідних металевих блоках); октет в цих атомах відповідає електронна конфігурація, що закінчується s 2 p 6.
Приклад іонних облігацій
Символи точки Льюїса також можуть бути використані для представлення іонів в іонних сполуках. Реакцію цезію з фтором, наприклад, на отримання іонної сполуки CsF можна записати наступним чином:

На Cs + немає крапок у продукті, оскільки цезій втратив свій єдиний валентний електрон до фтору. Перенесення цього електрона виробляє іон Cs +, який має валентну електронну конфігурацію Xe, і F − іон, який має загалом вісім валентних електронів (октет) та електронну конфігурацію Ne. Цей опис узгоджується з твердженням, що серед основних елементів групи іони в простих бінарних іонних сполуках зазвичай мають електронні конфігурації найближчого благородного газу. Заряд кожного іона записується в твір, а аніон і його електрони укладені в дужки. Це позначення підкреслює, що іони пов'язані електростатично; ніякі електрони не поділяються між двома елементами.