Тиск пари
- Page ID
- 24685
Навички для розвитку
- Визначте тиск пари
Всякий раз, коли у нас є рідина з деяким простором над нею, деякі молекули на поверхні рідини можуть вийти у простір і стати газоподібними, якщо у них достатньо кінетичної енергії. Якщо рідина знаходиться в закритій пляшці, то молекули в газовій фазі не можуть повністю піти. Там буде рідина, а над нею газ тієї ж молекули. Частинки газу іноді натикають рідину, і якщо вони мають досить малу кінетичну енергію, вони можуть залишитися в ній. Таким чином, молекули можуть йти взад-вперед між рідиною і газом. Зі збільшенням кількості газу він частіше вдариться на поверхню і застряє, тому темпи стають газовими і рідинними стають однаковими. Буде встановлено рівновагу. Парціальний тиск цього газу над рідиною при рівновазі буде залежати від типу молекули та температури. Якщо температура рідини підвищиться, більшій кількості молекул буде достатньо кінетичної енергії, щоб вийти з рідини і бути газом. Якщо молекула має сильні міжмолекулярні сили, для виходу рідини знадобиться більше кінетичної енергії.
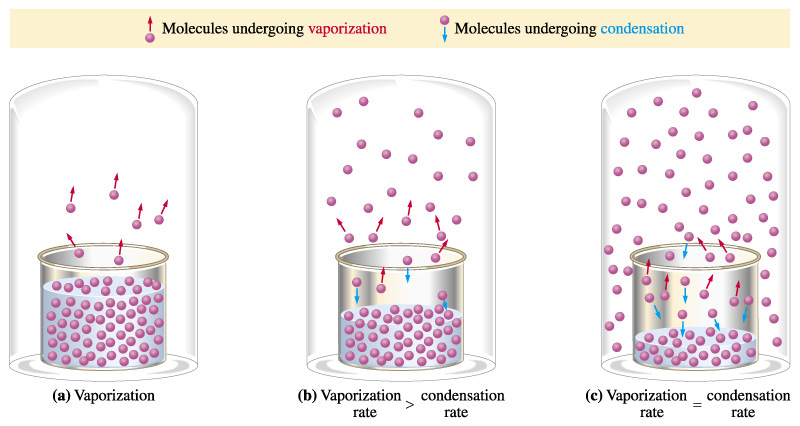
У відкритій ємності така рідина, як вода, з часом повністю випаровується, навіть при низьких температурах (навіть лід з часом зникне, тому що тверді речовини також мають тиск пари). Це відбувається тому, що коли молекули стають газом, вони можуть розсіюватися, замість того, щоб залишатися біля поверхні, і, можливо, натикаючись на неї і знову застрягати.
Тиск пари рідини не залежить від тиску в цілому (принаймні не сильно). Наявність інших молекул газу насправді не вплине на швидкість молекул рідини, що виходять з поверхні або повертаються до неї, оскільки їх зіткнення з рідиною не мають значення. Коли ми збираємо гази над рідиною, як у методі Хейлса, ми повинні включити корекцію тиску пари рідини. Ми можемо знайти це в таблиці, якщо знаємо температуру.
Деякі рідини мають високий тиск пари, а інші мають низький тиск пари. Це залежить від міжмолекулярних сил, таких як лондонські сили дисперсії, диполь-дипольні сили та водневі зв'язки. Якщо міжмолекулярні сили сильні, тиск пари буде низьким. Якщо вони слабкі, то вона буде високою. Летючі рідини мають високий тиск пари.