25.10: Ефіри
- Page ID
- 19462
Водії гоночних автомобілів завжди шукають той «край», який зробить їх автомобіль (легально) швидше, ніж автомобілі своїх конкурентів. Один із способів отримати більшу швидкість - більш ефективно спалювати бензин в двигуні автомобіля. З цією метою був використаний метил-т-бутиловий ефір (MTBE), але припиняється через побоювання щодо забруднення питної води витіканням паливних баків, що містять цю сполуку.
Ефіри
Ефір - це органічна сполука, в якій дві вуглеводневі групи пов'язані з одним і тим же атомом кисню. Ефір представлений загальною формулою\(\ce{R-O-R'}\). \(\ce{R'}\)У формулі означає, що вуглеводнева група може бути такою ж\(\ce{R}\), як, а може бути різною. Етапи для іменування ефірів наведені нижче.
- Батьківське з'єднання дається словом ефір, яке з'являється в кінці назви.
- Назви кожної алкільної групи походять перед словом ефір. Якщо дві алкільні групи однакові, використовується префікс di-. Якщо дві алкільні групи різні, вони перераховуються в алфавітному порядку.
- Прогалини залишаються між назвами алкільних груп (якщо вони різні) і перед словом ефір.
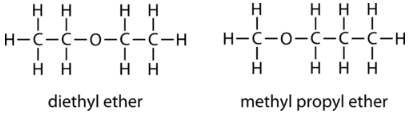
Нижче наведено два приклади ефірів з їх назвами IUPAC.
властивості ефірів
Як і спирти, ефіри також досить розчинні у воді. Однопарні електрони на атомі кисню ефіру можуть утворювати водневий зв'язок з атомами водню молекул води. Як і у спиртів, розчинність більша для ефірів, які мають більш короткі\(\ce{R}\) групи довжини. Точки кипіння ефірів набагато нижче, ніж температури кипіння спиртів. Молекули ефіру не мають атомів водню, які ковалентно пов'язані з високоелектронегативним атомом, і тому молекули ефіру не можуть утворювати водневі зв'язки один з одним. Більш слабка міжмолекулярна сила, що діє між молекулами ефіру, призводить до температури кипіння, які набагато ближче до алканів подібної молярної маси, ніж до спиртів.
Знеболюючі ефекти ефірів вперше були виявлені в 1840-х роках. Діетиловий ефір використовувався як загальний анестетик для пацієнтів, які перенесли операцію протягом багатьох років. Однак ефіри дуже легкозаймисті і мають небажані побічні ефекти, такі як нудота і блювота. Більш безпечні альтернативи ефірам зараз використовуються в анестезії, а основне застосування ефірів сьогодні - як розчинник для інших органічних сполук.
Резюме
- Ефір - це органічна сполука, в якій дві вуглеводневі групи пов'язані з одним і тим же атомом кисню.
- Правила іменування IUPAC для ефірів продиктовані.
- Ефіри досить розчинні у воді.
- Первинне застосування ефірів сьогодні полягає в якості розчинника для інших органічних сполук.