25.5: Ізомери
- Page ID
- 19435
Коли ми заглиблюємось у складнощі органічної хімії, ми побачимо, як молекулярна форма впливає на реакції. Однією з поширених реакцій для алкенів є додавання водню через подвійний зв'язок з утворенням відповідного алкану. Через геометрію реакції різні форми 2-бутену мають різну теплоту реакції. Ці відмінності важливі, як з теоретичної точки зору, так і з точки зору промислового застосування. Більші потреби в енергії означають більш високу вартість і більш дорогий продукт.
Ізомери
Одним з цікавих аспектів органічної хімії є те, що вона тривимірна. Молекула може мати форму в просторі, яка може сприяти її властивостям. Молекули можуть відрізнятися за способом розташування атомів - одна і та ж комбінація атомів може бути зібрана більш ніж одним способом. Ці сполуки відомі як ізомери. Ізомери - це молекули з однаковими молекулярними формулами, але різним розташуванням атомів. Ми розглянемо деякі можливості ізомерів для алканів і алкенів.
Структурні ізомери
Структурний ізомер - це той, в якому два або більше органічних сполук мають однакові молекулярні формули, але різну структуру. Дві молекули пентану нижче відрізняються лише розташуванням метильної групи.
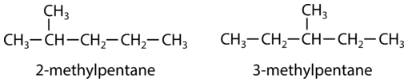
Алкени також можуть демонструвати структурну ізомерію. В алкенах існує безліч структурних ізомерів, заснованих на тому, де в ланцюзі відбувається подвійний зв'язок. Про це свідчать конденсовані структурні формули 1-бутену та 2-бутену.

Число в назві алкена відноситься до найнижчого пронумерованого вуглецю в ланцюжку, який є частиною подвійного зв'язку.
Геометричні ізомери
З такою молекулою, як 2-бутен, можна спостерігати інший тип ізомерії, званий геометричною ізомерією. Геометричні ізомери - це ізомери, в яких порядок зв'язку атомів однаковий, але розташування атомів в просторі різне. Подвійний зв'язок в алкені не може вільно обертатися через характер зв'язків пі. Тому існує два різних способи побудови молекули 2-бутену. На зображенні нижче показані два геометричні ізомери, звані цис-2-бутен і транс-2-бутен.
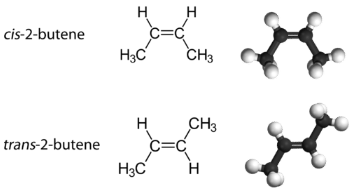
Ізомер цис має два одиничних атома водню на одній стороні молекули, тоді як транс-ізомер має їх на протилежних сторонам молекули. В обох молекулах порядок зв'язку атомів однаковий. Для того, щоб геометричні ізомери існували, в молекулі повинна бути жорстка структура, щоб запобігти вільному обертанню навколо зв'язку. Якби подвійний зв'язок в алкені був здатний обертатися, двох геометричних ізомерів вище не існувало б. Крім того, два атоми вуглецю повинні мати дві різні групи, прикріплені для того, щоб там були геометричні ізомери. Пропен не має геометричних ізомерів, оскільки один з атомів вуглецю має два одиночних водню, пов'язані з ним.
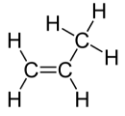
Фізико-хімічні властивості геометричних ізомерів, як правило, різні. У той час як цис-2-бутен є полярною молекулою, транс-2-бутен неполярний. Тепло або опромінення світлом можуть бути використані для перетворення одного геометричного ізомеру в інший. Вхід енергії повинен бути досить великим, щоб розірвати pi зв'язок між двома атомами вуглецю, який слабший, ніж сигма-зв'язок. У цей момент тепер єдиний зв'язок може вільно обертатися, і ізомери можуть взаємоконвертувати.
Як і у алкенів, алкіни проявляють структурну ізомерію, починаючи з 1-бутину та 2-бутину. Однак геометричних ізомерів з алкінами немає, оскільки існує лише одна інша група, пов'язана з атомами вуглецю, які беруть участь у потрійному зв'язку.
Резюме
- Ізомери - це молекули з однаковими молекулярними формулами, але різним розташуванням атомів.
- Структурний ізомер - це той, в якому два або більше органічних сполук мають однакові молекулярні формули, але різну структуру.
- Геометричні ізомери - це ізомери, в яких порядок зв'язку атомів однаковий, але розташування атомів в просторі різне.
- Наведено приклади ізомерів алкану та алкену.