14.4: Клінічні міркування
- Page ID
- 4076
Цілі навчання
- Поясніть відмінності між способами дії препаратів, які націлені на гриби, найпростіші, гельмінти та віруси
Оскільки гриби, найпростіші та гельмінти є еукаріотичними, їх клітини дуже схожі на клітини людини, що ускладнює розробку препаратів з селективною токсичністю. Крім того, віруси реплікуються в клітинах-господарях людини, що ускладнює розробку препаратів, вибірково токсичних для вірусів або заражених вірусом клітин. Незважаючи на ці проблеми, існують протимікробні препарати, які спрямовані на гриби, найпростіші, гельмінти та віруси, а деякі навіть націлені на більш ніж один тип мікробів. У таблиці\(\PageIndex{1}\), таблиці\(\PageIndex{2}\)\(\PageIndex{3}\), таблиці та таблиці наведені\(\PageIndex{4}\) приклади антимікробних препаратів цих різних класів.
протигрибкові препарати
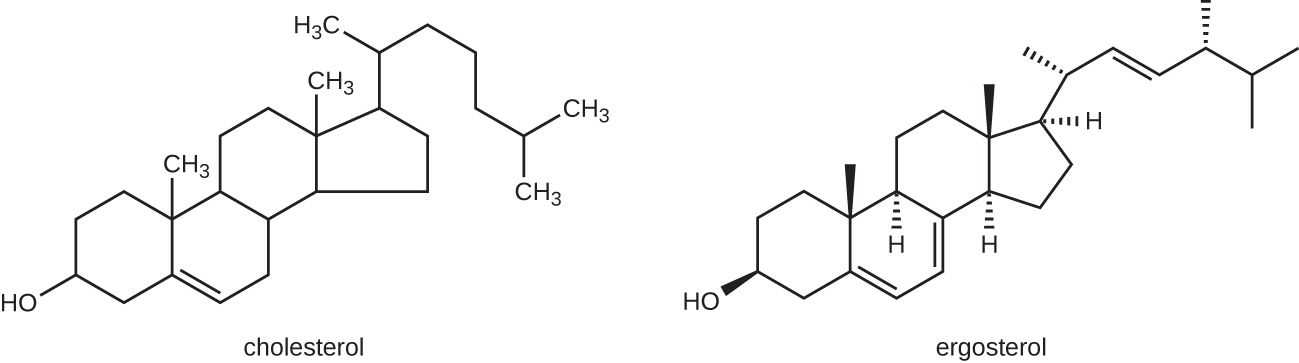
Найбільш поширеним способом дії протигрибкових препаратів є порушення клітинної мембрани. Протигрибкові препарати використовують невеликі відмінності між грибами та людиною в біохімічних шляхах, що синтезують стерини. Стерини мають важливе значення для підтримки належної плинності мембрани і, отже, правильної функції клітинної мембрани. Для більшості грибів переважаючим мембранним стерином є ергостерол. Оскільки мембрани клітин людини використовують холестерин, замість ергостерину протигрибкові препарати, спрямовані на синтез ергостерину, вибірково токсичні (рис.\(\PageIndex{1}\)).
Імідазоли - це синтетичні фунгіциди, які порушують біосинтез ергостерину; вони зазвичай використовуються в медичних цілях, а також у сільському господарстві, щоб зберегти насіння та зібрані врожаї від формування. Приклади включають міконазол, кетоконазол та клотримазол, які використовуються для лікування грибкових шкірних інфекцій, таких як стригучий лишай, зокрема tinea pedis (стопа спортсмена), tinea cruris (свербіж спортсмена) та tinea corporis. Ці інфекції зазвичай викликаються дерматофітами пологів Trichophyton, Epidermophyton і Microsporum. Міконазол також використовується переважно для лікування вагінальних дріжджових інфекцій, викликаних грибком Candida, а кетоконазол використовується для лікування лишаю та лупи, які обидва можуть бути викликані грибком Malassezia.
Препарати триазолу, включаючи флуконазол, також пригнічують біосинтез ергостерину. Однак їх можна вводити перорально або внутрішньовенно для лікування декількох типів системних дріжджових інфекцій, включаючи пероральну молочницю та криптококовий менінгіт, обидва з яких поширені у хворих на СНІД. Триазоли також виявляють більш селективну токсичність, порівняно з імідазолами, і пов'язані з меншою кількістю побічних ефектів.
Алліламіни, структурно інший клас синтетичних протигрибкових препаратів, інгібують більш ранню стадію біосинтезу ергостерину. Найбільш часто використовуваним алліламіном є тербінафін (продається під торговою маркою Lamisil), який використовується місцево для лікування дерматофітних шкірних інфекцій, таких як стопа спортсмена, стригучий лишай та свербіж спортсмена. Пероральне лікування тербінафіном також використовується для лікування грибка нігтів і нігтів на ногах, але це може бути пов'язано з рідкісним побічним ефектом гепатотоксичності.
Полієни - це клас протигрибкових засобів, які природним чином виробляються певними бактеріями грунту актиноміцетів і структурно пов'язані з макролідами. Ці великі ліпофільні молекули зв'язуються з ергостеролом в грибкових цитоплазматичних мембранах, створюючи таким чином пори. Поширені приклади включають ністатин і амфотерицин Б. ністатин зазвичай використовується як місцеве лікування дріжджових інфекцій шкіри, рота та піхви, але також може бути використаний для кишкових грибкових інфекцій. Препарат амфотерицин В застосовується при системних грибкових інфекціях, таких як аспергільоз, криптококовий менінгіт, гістоплазмоз, бластомікоз і кандидоз. Амфотерицин В був єдиним протигрибковим препаратом, доступним протягом декількох десятиліть, але його застосування пов'язане з деякими серйозними побічними ефектами, включаючи нефротоксичність (токсичність нирок).
Амфотерицин В часто використовується в комбінації з флуцитозином, фторованим аналогом піримідину, який перетворюється грибковим специфічним ферментом в токсичний продукт, який перешкоджає як реплікації ДНК, так і синтезу білка у грибів. Флуцитозин також пов'язаний з гепатотоксичністю (токсичність печінки) і пригніченням кісткового мозку.
Крім таргетингу ергостеролу в мембранах грибкових клітин, існує кілька протигрибкових препаратів, які націлені на інші грибкові структури (рис.\(\PageIndex{2}\)). Ехінокандини, включаючи каспофунгін, - це група природним чином вироблених протигрибкових сполук, які блокують синтез β (1 → 3) глюкану, знайденого в грибкових клітинних стінках, але не виявлених у клітині людини. Цей клас ліків має прізвисько «пеніцилін для грибів». Каспофунгін використовується для лікування аспергільозу, а також системних дріжджових інфекцій.
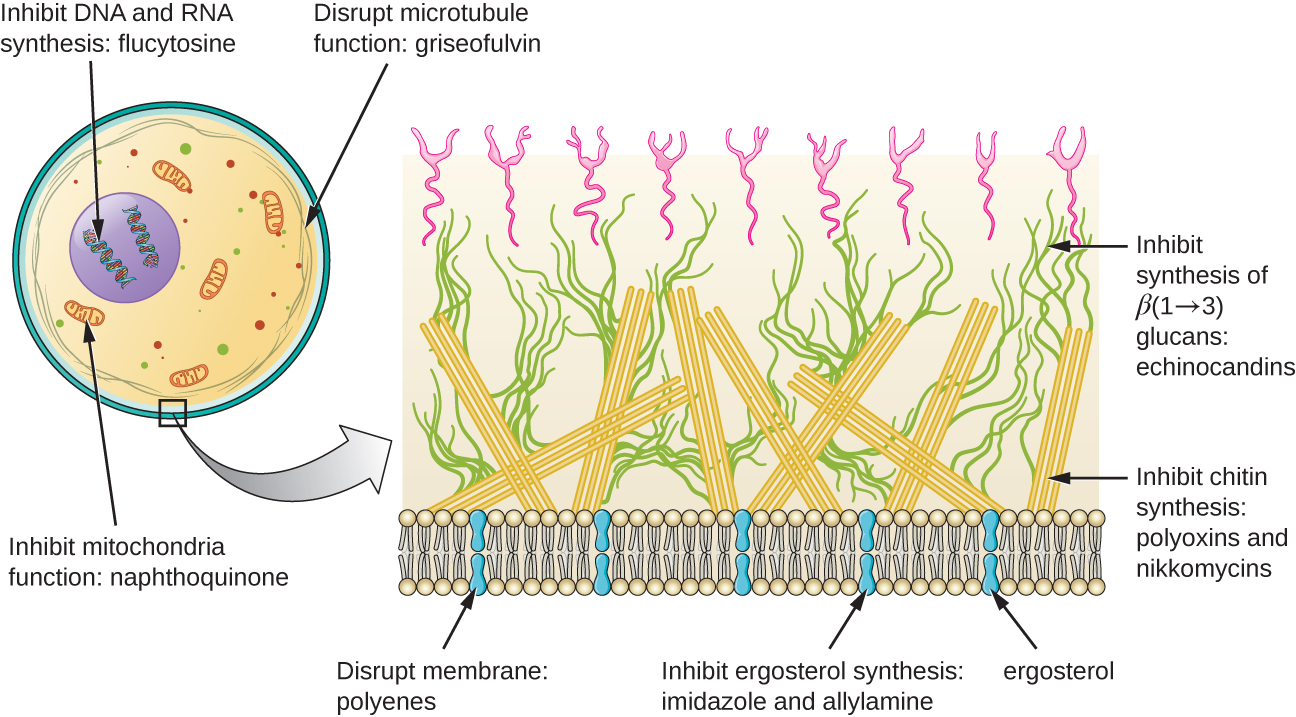
Хоча хітин є лише незначною складовою грибкових клітинних стінок, він також відсутній в клітині людини, що робить його селективною мішенню. Поліоксини та ніккоміцини природним чином виробляються протигрибковими препаратами, які націлені на синтез хітину. Поліоксини використовуються для боротьби з грибами в сільськогосподарських цілях, і ніккоміцин Z в даний час розробляється для використання у людей для лікування дріжджових інфекцій та лихоманки Долини (кокцидіоідомікоз), грибкового захворювання, поширеного на південному заході США. 1
Вважається, що природний протигрибковий гризеофульвін спеціально порушує поділ грибкових клітин, втручаючись у мікротрубочки, що беруть участь у формуванні веретена під час мітозу. Це було одне з перших протигрибкових препаратів, але його застосування пов'язане з гепатотоксичністю. Зазвичай його застосовують перорально для лікування різних типів дерматофітних шкірних інфекцій, коли інші місцеві протигрибкові методи лікування неефективні.
Існує кілька препаратів, які діють як антиметаболіти проти грибкових процесів. Наприклад, атовакуон, представник класу препаратів нафтохінону, є напівсинтетичним антиметаболітом для грибкових і найпростіших версій мітохондріального цитохрому, важливого в електронному транспорті. Структурно він є аналогом коферменту Q, з яким конкурує за електронне зв'язування. Це особливо корисно для лікування пневмоцистної пневмонії, спричиненої Pneumocystis jirovecii. Антибактеріальна комбінація сульфаметоксазол-триметоприм також діє як антиметаболіт проти P. jirovecii.
У таблиці\(\PageIndex{1}\) наведені різні терапевтичні класи протигрибкових препаратів, класифікованих за способом дії, з прикладами кожного.
| Механізм дії | Клас наркотиків | специфічні препарати | Клінічне використання |
|---|---|---|---|
| Пригнічують синтез ергостерину | імідазоли | Міконазол, кетоконазол, клотримазол | Грибкові інфекції шкіри та вагінальні дріжджові інфекції |
| Триазоли | Флуконазол | Системні дріжджові інфекції, молочниця порожнини рота та криптококовий менінгіт | |
| Аліламіни | Тербінафін | Дерматофітні шкірні інфекції (стопа спортсмена, кільцевий черв'як, свербіж спортсмена) та інфекції нігтів і нігтів | |
| Зв'язують ергостерол в клітинній мембрані і створюють пори, що порушують мембрану | Полієни | Ністатин | Використовується місцево для дріжджових інфекцій шкіри, рота, і піхви; також використовується для грибкових інфекцій кишечника |
| Амфотерицин В | Різновиди системних грибкових інфекцій | ||
| Пригнічують синтез клітинної стінки | ехінокандини | Каспофунгін | Аспергільоз і системні дріжджові інфекції |
| Не застосовується | Ніккоміцин Z | Кокцидіоідомікоз (лихоманка Долини) та дріжджові інфекції | |
| Пригнічують мікротрубочки і поділ клітин | Не застосовується | Гризеофульвін | Дерматофітні інфекції шкіри |
Вправа\(\PageIndex{1}\)
Як порушення біосинтезу ергостерину ефективним способом дії протигрибкових препаратів?
Лікування грибкової інфекції легенів
Джек, 48-річний інженер, є ВІЛ-позитивним, але загалом здоровим завдяки антиретровірусній терапії (АРТ). Однак після особливо інтенсивного тижня на роботі у нього розвинулася температура і сухий кашель. Він припустив, що у нього просто застуда або легкий грип через перенапруження і не думав багато про це. Однак приблизно через тиждень у нього почалася втома, зниження ваги, задишка. Він вирішив відвідати свого лікаря, який виявив, що у Джека низький рівень оксигенації крові. Лікар замовив аналіз крові, рентген грудної клітки та збір індукованого зразка мокротиння для аналізу. Його рентген показав дрібну помутніння і кілька пневматоцеле (тонкостінні кишені повітря), що вказувало на пневмоцистну пневмонію (PCP), тип пневмонії, викликаної грибком Pneumocystis jirovecii. Лікар Джека прийняв його до лікарні і призначив Бактрім, комбінацію сульфаметоксазолу і триметоприму, для введення внутрішньовенно.
P. jirovecii - це дріжджоподібний гриб з життєвим циклом, подібним до циклу найпростіших. Таким чином, він був класифікований як найпростіший до 1980-х років. Він живе тільки в легеневій тканині інфікованих осіб і передається від людини до людини, причому багато людей піддаються як діти. Як правило, P. jirovecii викликає пневмонію лише у осіб з ослабленим імунітетом. Здорові люди можуть переносити грибок у легенях без симптомів захворювання. ПХФ особливо проблемний серед хворих на ВІЛ з порушеною імунною системою.
PCP зазвичай лікують пероральним або внутрішньовенним Bactrim, але альтернативою є атовакуон або пентамідин (інший протипаразитарний препарат). Якщо не лікувати, ПХФ може прогресувати, що призводить до згорнутої легені та майже 100% смертності. Навіть при антимікробній медикаментозній терапії PCP все ще несе відповідальність за 10% смертей, пов'язаних з ВІЛ.
Цитологічне дослідження з використанням прямого імунофлюоресцентного аналізу (ДФА) мазка з зразка мокротиння Джека підтвердило наявність P. jirovecii (рис.\(\PageIndex{3}\)). Крім того, результати аналізів крові Джека показали, що його кількість лейкоцитів знизилася, що робить його більш сприйнятливим до грибка. Його лікар переглянув його режим АРТ і вніс корективи. Через кілька днів госпіталізації Джека відпустили, щоб продовжити антимікробну терапію вдома. З коригуваннями в його АРТ-терапії кількість CD4 Джека почала збільшуватися, і він зміг повернутися до роботи.
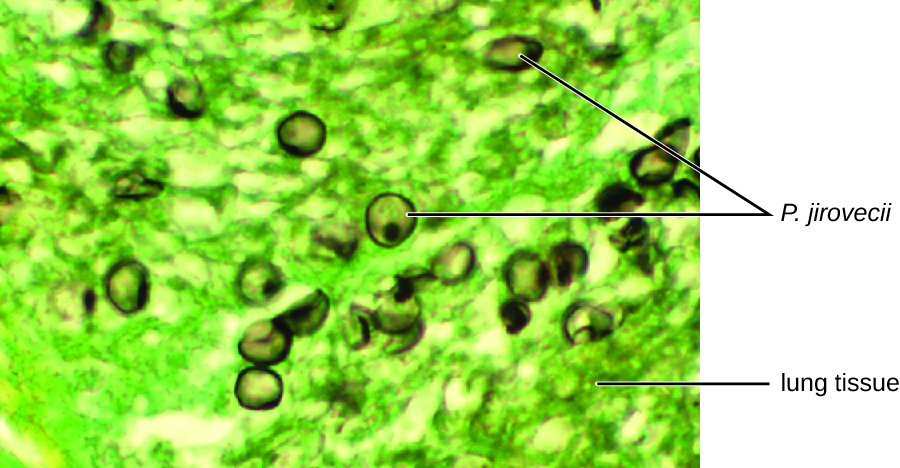
Антипротозойні препарати
Існує кілька механізмів, за допомогою яких протипротозойні препарати націлені на інфекційних найпростіших (табл.\(\PageIndex{3}\)). Деякі з них є антиметаболітами, такими як атовакуон, прогуаніл та артемізиніни. Атовакуон, крім того, що є протигрибковим, блокує електронний транспорт у найпростіших і використовується для лікування найпростіших інфекцій, включаючи малярію, бабезіоз та токсоплазмоз. Прогуаніл - ще один синтетичний антиметаболіт, який переробляється в клітинах-паразитах в його активну форму, що пригнічує синтез найпростіших фолієвої кислоти. Він часто використовується в поєднанні з атоваквоном, і комбінація продається як Маларон як для лікування малярії і профілактики.
Артемізинін, рослинний протигрибковий засіб, вперше виявлений китайськими вченими в 1970-х роках, досить ефективний проти малярії. Напівсинтетичні похідні артемізиніну більш водорозчинні, ніж натуральний варіант, що робить їх більш біодоступними. Хоча точний механізм дії неясний, артемізиніни, здається, діють як пропрепарати, які метаболізуються клітинами-мішенями для вироблення активних форм кисню (ROS), які пошкоджують клітини-мішені. Через підвищення резистентності до протималярійних препаратів артемізиніни також зазвичай використовуються в комбінації з іншими протималярійними сполуками в комбінованій терапії на основі артемізиніну (АКТ).
Кілька антиметаболітів використовуються для лікування токсоплазмозу, викликаного паразитом Toxoplasma gondii. Синтетичний сульфатний препарат сульфадіазин конкурентно пригнічує фермент у виробництві фолієвої кислоти у паразитів і може бути використаний для лікування малярії та токсоплазмозу. Піриметамін - це синтетичний препарат, який пригнічує інший фермент у шляху вироблення фолієвої кислоти і часто використовується в комбінації з сульфадоксином (іншим сульфатним препаратом) для лікування малярії або в поєднанні з сульфадіазином для лікування токсоплазмозу. Побічні ефекти піриметаміну включають зниження активності кісткового мозку, що може спричинити посилення синців та низький вміст еритроцитів. Коли токсичність викликає занепокоєння, спіраміцин, інгібітор синтезу макролідів білка, зазвичай призначається для лікування токсоплазмозу.
Два класи антипротозойних препаратів перешкоджають синтезу нуклеїнових кислот: нітроїмідазоли і хіноліни. Нітроїмідазоли, включаючи напівсинтетичний метронідазол, який раніше обговорювався як антибактеріальний препарат, і синтетичний тинідазол, корисні для боротьби з найрізноманітнішими збудниками найпростіших, таких як лямблії, Entamoeba histolytica та Trichomonas vaginalis . При введенні в ці клітини в середовищах з низьким вмістом кисню нітроімідазоли активізуються і вводять обрив ланцюга ДНК, перешкоджаючи реплікації ДНК в клітинах-мішенях. На жаль, метронідазол пов'язаний з канцерогенезом (розвитком раку) у людини.
Інший тип синтетичного антипротозойного препарату, який, як давно вважалося, спеціально втручається в реплікацію ДНК у певних патогенів, - це пентамідин. Історично він використовувався для лікування африканської сонної хвороби (спричиненої найпростішим Trypanosoma brucei) та лейшманіозу (спричиненого найпростішими роду Leishmania), але це також альтернативне лікування грибка Pneumocystis. Деякі дослідження показують, що він спеціально зв'язується з ДНК, знайденої в кінетопластах (кДНК; довгі мітохондріоподібні структури, унікальні для трипаносом), що призводить до розщеплення кДНК. Однак ядерна ДНК як паразита, так і господаря залишається незмінною. Він також, як видається, зв'язується з тРНК, пригнічуючи додавання амінокислот до тРНК, тим самим запобігаючи синтезу білка. Можливі побічні ефекти застосування пентамідину включають дисфункцію підшлункової залози та ураження печінки.
Хіноліни - це клас синтетичних сполук, що відносяться до хініну, який має довгу історію використання проти малярії. Вважається, що хіноліни перешкоджають детоксикації гема, що необхідно для ефективного розщеплення паразита гемоглобіну на амінокислоти всередині еритроцитів. Синтетичні похідні хлорохін, хінакрин (також званий мепакрин) та мефлохін зазвичай використовуються як протималярійні препарати, а хлорохін також використовується для лікування амебіазу, як правило, спричиненого Entamoeba histolytica. Тривале профілактичне застосування хлорохіну або мефлохіну може призвести до серйозних побічних ефектів, включаючи галюцинації або серцеві проблеми. Пацієнти з дефіцитом глюкозо-6-фосфатдегідрогенази відчувають важку анемію при лікуванні хлорохіном.
| Механізм дії | Клас наркотиків | специфічні препарати | Клінічне використання |
|---|---|---|---|
| Пригнічують транспорт електронів у мітохондріях | Нафтохінон | Атовакуоне | Малярія, бабезіоз та токсоплазмоз |
| Пригнічують синтез фолієвої кислоти | Не застосовується | Проканіл | Комбінована терапія атоваквоном для лікування та профілактики малярії |
| Сульфаніламід | сульфадіазин | Малярія і токсоплазмоз | |
| Не застосовується | піриметамін | Комбінована терапія сульфадоксином (сульфадоксином) при малярії | |
| Виробляє шкідливі активні форми кисню | Не застосовується | Артемізинін | Комбінована терапія для лікування малярії |
| Пригнічують синтез ДНК | нітроїмідазоли | Метронідазол, тинідазол | Інфекції, спричинені лямбліями лямбліями, ентамоеба гістолітіка та вагінальна трихомонада |
| Не застосовується | Пентамідин | Африканська сонна хвороба і лейшманіоз | |
| Пригнічують детоксикацію гема | хіноліни | хлорохін | Малярія та інфекції з E. histolytica |
| Мепакрин, мефлохін | Малярія |
Вправа\(\PageIndex{2}\)
Перерахуйте два режими дії протипротозойних препаратів.
Протигельмінтні препарати
Оскільки гельмінти є багатоклітинними еукаріотами, як і люди, розробка препаратів з селективною токсичністю проти них є надзвичайно складною справою. Незважаючи на це, розроблено кілька ефективних занять (табл.\(\PageIndex{3}\)). Синтетичні бензимідазоли, як мебендазол і альбендазол, зв'язуються з глистовим β-тубуліном, перешкоджаючи утворенню мікротрубочок. Мікротрубочки в клітині кишечника глистів, здається, особливо уражаються, що призводить до зниження поглинання глюкози. Крім їх активності проти широкого спектру гельмінтів, бензимідазоли також активні проти багатьох найпростіших, грибків та вірусів, і вивчається їх застосування для інгібування мітозу та прогресування клітинного циклу в ракових клітині. 2 Можливі побічні ефекти від їх застосування включають пошкодження печінки і придушення кісткового мозку.
Авермектини є членами сімейства макролідів, які були вперше виявлені з японського ґрунтового ізоляту Streptomyces avermectinius. Більш потужним напівсинтетичним похідним авермектину є івермектин, який зв'язується з глутаматовими хлоридними каналами, специфічними для безхребетних, включаючи гельмінтів, блокуючи нейронну передачу і викликаючи голод, параліч і смерть глистів. Івермектин використовується для лікування захворювань аскариди, включаючи онхоцеркоз (також називається річкова сліпота, викликана хробаком Onchocerca volvulus) та стронгілоїдоз (викликаний хробаком Strongyloides stercoralis або S. fuelleborni). Івермектин також може лікувати паразитичних комах, таких як кліщі, воші та постільні клопи, і нетоксичний для людини.
Ніклозамід - це синтетичний препарат, який використовується більше 50 років для лікування інфекцій солітера. Хоча його спосіб дії не зовсім зрозумілий, ніклозамід, як видається, пригнічує утворення АТФ в анаеробних умовах і пригнічує окислювальне фосфорилювання в мітохондріях його цільових збудників. Ніклозамід не всмоктується з шлунково-кишкового тракту, таким чином він може досягти високих локалізованих кишкових концентрацій у пацієнтів. Останнім часом було показано, що він також має антибактеріальну, противірусну та протипухлинну активність. 3 4 5
Іншим синтетичним протиглистовим препаратом є празиквантел, який використовується для лікування паразитарних стрічкових черв'яків і печінкових сосальщиков, і особливо корисний для лікування шистосомозу (викликаного кровотопиками з трьох пологів шистосоми). Його спосіб дії залишається неясним, але він, як видається, викликає приплив кальцію в глист, в результаті чого виникає інтенсивний спазм і параліч хробака. Він часто використовується як краща альтернатива ніклозаміду при лікуванні стрічкових черв'яків, коли шлунково-кишковий дискомфорт обмежує використання ніклозаміду.
Тіоксантенони, інший клас синтетичних препаратів, структурно пов'язаних з хініну, проявляють антишистосомальну активність шляхом інгібування синтезу РНК. Тіоксантенон лукантон та його метаболіт гікантон були першими клінічно, але серйозні неврологічні, шлунково-кишкові, серцево-судинні та печінкові побічні ефекти призвели до їх припинення. Оксамніхін, менш токсичне похідне гікантону, ефективний лише проти S. mansoni, одного з трьох видів, які, як відомо, викликають шистосомоз у людини. Празиквантел був розроблений для націлювання на інші два види шистосом, але занепокоєння щодо підвищення стійкості відновили інтерес до розробки додаткових похідних оксамніхіну для націлення всіх трьох клінічно важливих видів шистосом.
| Механізм дії | Клас наркотиків | специфічні препарати | Клінічне використання |
|---|---|---|---|
| Пригнічують утворення мікротрубочок, зменшуючи поглинання глюкози | Бензимідазоли | Мебендазол, альбендазол | Різноманітність гельмінтозів |
| Блокують нейронну передачу, викликаючи параліч і голодування | авермектини | івермектин | Захворювання аскариди, включаючи річкову сліпоту та стронгілоїдоз, лікування паразитичних комах |
| Пригнічують виробництво АТФ | Не застосовується | Ніклозамід | Інфекції кишкового солітера |
| Індукція припливу кальцію | Не застосовується | Празиквантел | Шистосомоз (кровоносні сосальці) |
| Пригнічують синтез РНК | Тіоксантенони | Лукантон, гікантон, оксамніхін | Шистосомоз (кровоносні сосальці) |
Вправа\(\PageIndex{3}\)
Чому протигельмінтні препарати важко розробляються?
противірусні препарати
На відміну від складної будови грибів, найпростіших і гельмінтів, вірусна структура проста, що складається з нуклеїнової кислоти, білкової оболонки, вірусних ферментів, а іноді і ліпідної оболонки. Крім того, віруси є облігатними внутрішньоклітинними патогенами, які використовують клітинний механізм господаря для реплікації. Ці характеристики ускладнюють розробку препаратів з селективною токсичністю проти вірусів.
Багато противірусні препарати є нуклеозидними аналогами і функціонують шляхом інгібування біосинтезу нуклеїнових кислот. Наприклад, ацикловір (продається як Зовіракс) є синтетичним аналогом нуклеозида гуанозина (рис.\(\PageIndex{4}\)). Він активується вірусним ферментом простого герпесу тимідинкіназою і при додаванні до зростаючої ланцюга ДНК під час реплікації викликає припинення ланцюга. Його специфічність для заражених вірусом клітин походить як від необхідності вірусного ферменту для його активації, так і від підвищеної спорідненості активованої форми до вірусної ДНК-полімерази порівняно з ДНК-полімеразою клітини-господаря. Ацикловір та його похідні часто використовуються для лікування герпес-вірусних інфекцій, включаючи генітальний герпес, вітрянку, оперізуючий лишай, вірусні інфекції Епштейна-Барр та цитомегаловірусні інфекції. Ацикловір можна вводити як місцево, так і системно, в залежності від інфекції. Один з можливих побічних ефектів від його застосування включає нефротоксичність. Препарат аденін-арабінозид, що продається як видарабін, є синтетичним аналогом дезоксиаденозину, який має механізм дії, подібний до механізму дії ацикловіру. Він також ефективний для лікування різних вірусів герпесу людини. Однак через можливі побічні ефекти, що включають низький вміст лейкоцитів та нейротоксичність, лікування ацикловіром зараз є кращим.
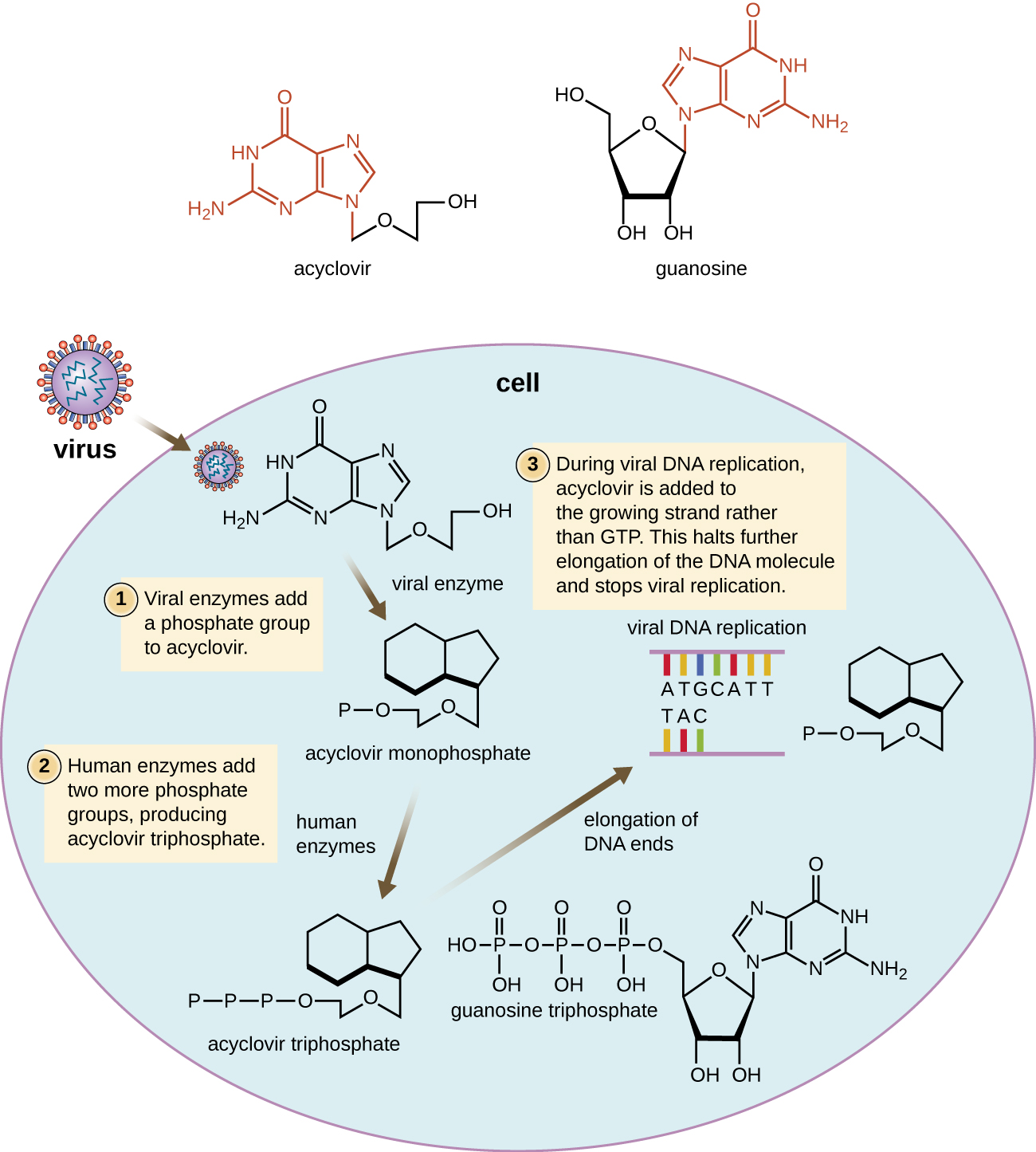
Рибавірин, ще один синтетичний аналог гуанозина, працює за не зовсім зрозумілим механізмом дії. Здається, це заважає як синтезу ДНК, так і РНК, можливо, шляхом зменшення внутрішньоклітинних пулів гуанозинтрифосфату (GTP). Рибаварін також, як видається, інгібує РНК-полімеразу вірусу гепатиту С. Він в основному використовується для лікування РНК вірусів, таких як гепатит С (в комбінованій терапії з інтерфероном) і респіраторно-синцитіальний вірус. Можливі побічні ефекти застосування рибавірину включають анемію та вплив на розвиток майбутніх дітей у вагітних пацієнтів. В останні роки для лікування гепатиту С. Софосбувір - софосбувір (Solvaldi) також був розроблений для лікування гепатиту С. Софосбувір - аналог уридину, який перешкоджає активності вірусної полімерази. Зазвичай його застосовують спільно з рибавірином, з інтерфероном і без нього.
Пригнічення синтезу нуклеїнових кислот - не єдина мішень синтетичних противірусних препаратів. Хоча спосіб дії амантадину і його родича ремантадину не зовсім зрозумілий, ці препарати, здається, зв'язуються з трансмембранним білком, який бере участь у втечі вірусу грипу з ендосом. Блокування втечі вірусу також запобігає викиду вірусної РНК в клітини-господаря і подальшу реплікацію вірусів. Підвищення резистентності обмежило застосування амантадину та ремантадину при лікуванні грипу А. використання амантадину може призвести до неврологічних побічних ефектів, але побічні ефекти ремантадину здаються менш важкими. Цікаво, що через їх вплив на хімічні речовини мозку, такі як дофамін і NMDA (N-метил D-аспартат), амантадин і ремантадин також використовуються для лікування хвороби Паркінсона.
Інгібітори нейрамінідази, включаючи ольсетамівір (таміфлю), занамівір (Реленза) та перамівір (Рапіваб), спеціально націлені на віруси грипу, блокуючи активність нейрамінідази вірусу грипу, запобігаючи вивільненню вірусу з інфікованих клітин. Ці три противірусні препарати можуть зменшити симптоми грипу і скоротити тривалість хвороби, але відрізняються за своїми способами введення: ольсетамівір вводять перорально, занамівір інгалюють, а перорамівір вводять внутрішньовенно. Стійкість до цих інгібіторів нейрамінідази все ще здається мінімальною.
Плеконаріл - синтетичний противірусний засіб, що розробляється, який показав перспективність для лікування пікорнавірусів. Використання плеконарілу для лікування застуди, спричиненої риновірусами, не було схвалено FDA в 2002 році через відсутність доведеної ефективності, відсутність стабільності та асоціацію з нерегулярними менструаціями. Подальший її розвиток з цією метою було зупинено в 2007 році. Однак плеконаріл все ще досліджується для використання в лікуванні небезпечних для життя ускладнень ентеровірусів, таких як менінгіт та сепсис. Він також досліджується для використання в глобальній ліквідації специфічного ентеровірусу, поліомієліту. 6 Плеконаріл, здається, працює, зв'язуючись з вірусним капсидом та запобігаючи розкриттю вірусних частинок всередині клітин господаря під час вірусної інфекції.
Віруси зі складними життєвими циклами, такі як ВІЛ, можуть бути важче піддаються лікуванню. По-перше, ВІЛ націлений на CD4-позитивні лейкоцити, які необхідні для нормальної імунної відповіді на інфекцію. По-друге, ВІЛ - це ретровірус, тобто він перетворює свій геном РНК у копію ДНК, яка інтегрується в геном клітини-господаря, таким чином ховаючись у ДНК клітини господаря. По-третє, зворотна транскриптаза ВІЛ не має коректорської активності та вводить мутації, що дозволяють швидко розвивати резистентність до противірусних препаратів. Щоб запобігти виникненню резистентності, в АРТ при ВІЛ зазвичай застосовують комбінацію специфічних синтетичних противірусних препаратів (рис.\(\PageIndex{5}\)).
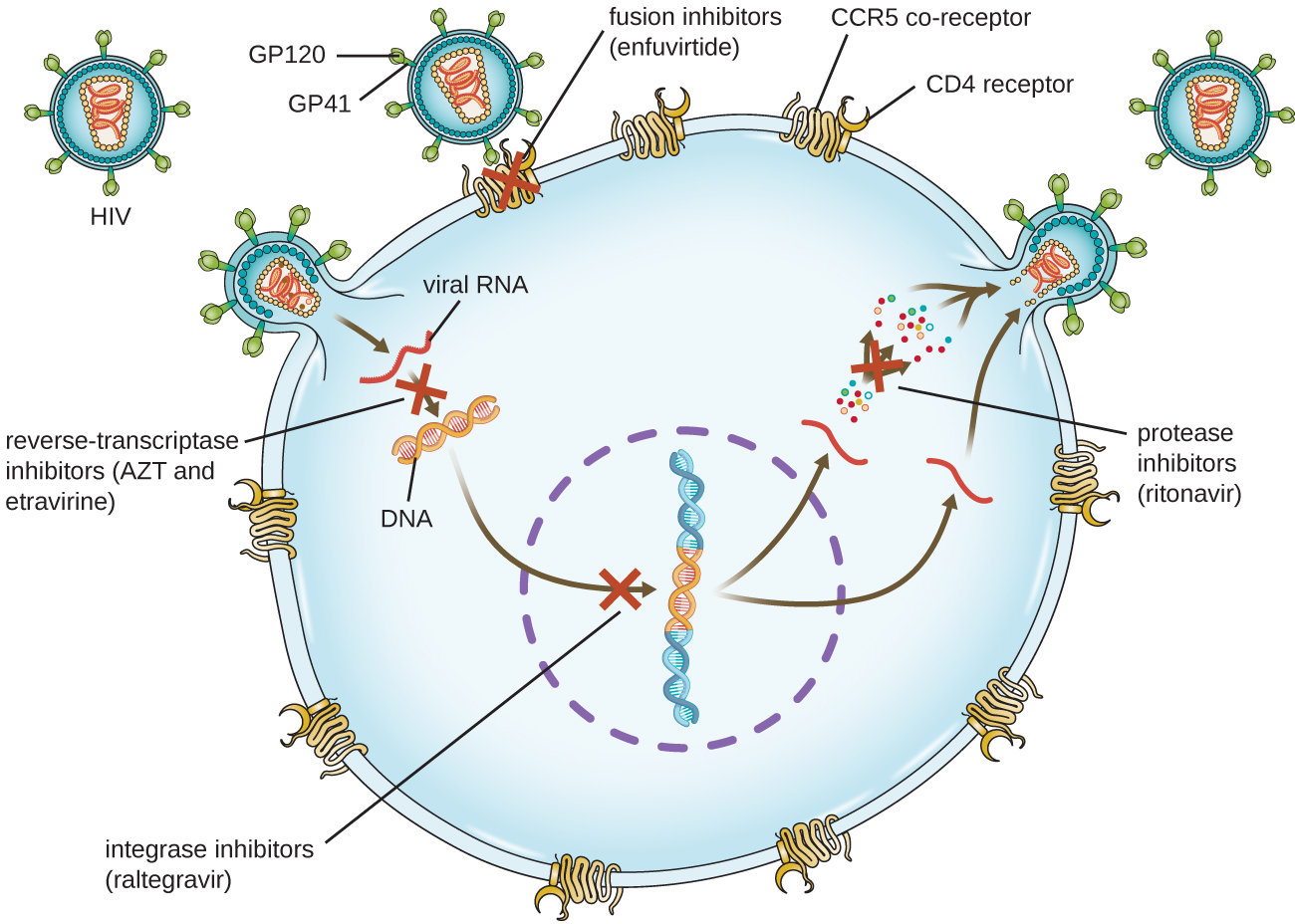
Інгібітори зворотної транскриптази блокують ранню стадію перетворення геному вірусної РНК в ДНК і можуть включати конкурентні нуклеозидні аналогові інгібітори (наприклад, азидотимідин/зидовудин або АЗТ) та ненуклеозидні неконкурентні інгібітори (наприклад, етравірин), які зв'язують зворотну транскриптазу і викликають інактивація конформаційних змін. Препарати, звані інгібіторами протеази (наприклад, ритонавір) блокують переробку вірусних білків і запобігають вірусному дозріванню. Також розробляються інгібітори протеази для лікування інших вірусних типів. 7 Наприклад, симепревір (Olysio) був схвалений для лікування гепатиту С і призначається разом з рибавірином і інтерфероном в комбінованій терапії. Інгібітори інтегрази (наприклад, ралтегравір) блокують активність інтегрази ВІЛ, відповідальної за рекомбінацію ДНК копії вірусного генома в хромосому клітини господаря. Додаткові класи препаратів для лікування ВІЛ включають антагоністи CCR5 та інгібітори злиття (наприклад, енфувіритид), які запобігають зв'язуванню ВІЛ з корецептором клітини-господаря (рецептор хемокіну типу 5 [CCR5]) та злиття вірусної оболонки з мембраною клітини господаря відповідно. У таблиці\(\PageIndex{4}\) наведені різні терапевтичні класи противірусних препаратів, класифікованих за способом дії, з прикладами кожного.
| Механізм дії | Наркотик | Клінічне використання |
|---|---|---|
| Аналогове інгібування нуклеозидів синтезу нуклеїнових кислот | Ацикловір | Герпес-вірусні інфекції |
| Азидотимідин/зидовудин (AZT) | ВІЛ-інфекції | |
| Рибавірин | Вірус гепатиту С та респіраторно-синцитіальні вірусні інфекції | |
| Відарабін | Герпес-вірусні інфекції | |
| Софосбувір | Інфекції вірусом гепатиту С | |
| Ненуклеозидний неконкурентне інгібування | Етравірин | ВІЛ-інфекції |
| Пригнічують втечу вірусу з ендосом | Амантадин, ремантадин | Інфекції вірусом грипу |
| Пригнічують нейрамінадазу | Ольсетамівір, занамівір, перамівір | Інфекції вірусом грипу |
| Пригнічують вірусне викриття | Плеконаріль | Серйозні ентеровірусні інфекції |
| інгібування протеази | ритонавір | ВІЛ-інфекції |
| Сімепревір | Інфекції вірусом гепатиту С | |
| інгібування інтегрази | Ралтегравір | ВІЛ-інфекції |
| Пригнічення злиття мембран | Енфувіритид | ВІЛ-інфекції |
Вправа\(\PageIndex{4}\)
Чому ВІЛ важко лікувати противірусними препаратами?
Щоб дізнатись більше про різні класи антиретровірусних препаратів, що використовуються при АРТ ВІЛ-інфекції, вивчіть кожен із препаратів у класах наркотиків для ВІЛ, що надаються Міністерством охорони здоров'я та соціальних служб США на цьому веб-сайті.
Ключові поняття та резюме
- Оскільки гриби, найпростіші та гельмінти є еукаріотичними організмами, такими як клітини людини, складніше розробляти антимікробні препарати, які спеціально орієнтовані на них. Так само важко націлити віруси, оскільки віруси людини розмножуються всередині людських клітин.
- Протигрибкові препарати перешкоджають синтезу ергостерину, зв'язуються з ергостеролом, щоб порушити цілісність клітинної мембрани гриба, або мішені клітинні стінки компонентів або інших клітинних білків.
- Антипротозойні препарати підвищують клітинний рівень активних форм кисню, перешкоджають реплікації протозойної ДНК (ядерної проти кДНК відповідно) та порушують детоксикацію гема.
- Протигельмінтні препарати порушують глистові та найпростіші утворення мікротрубочок; блокують нейронні передачі; інгібують анаеробне утворення АТФ та/або окислювальне фосфорилювання; індукують приплив кальцію до стрічкових черв'яків, що призводить до спазмів і паралічу; і перешкоджають синтезу РНК у шистосомах.
- Противірусні препарати пригнічують вірусне проникнення, пригнічують вірусне розкриття, пригнічують біосинтез нуклеїнових кислот, запобігають виходу вірусу з ендосом в клітинах-господарях та запобігають вивільненню вірусу з інфікованих клітин.
- Оскільки він може легко мутувати, щоб стати стійким до наркотиків, ВІЛ, як правило, лікується комбінацією декількох антиретровірусних препаратів, які можуть включати інгібітори зворотної транскриптази, інгібітори протеази, інгібітори інтегрази та препарати, які перешкоджають вірусному зв'язуванню та злиття ініціювати зараження.
Виноски
- 1 Центри з контролю та профілактики захворювань. «Лихоманка Долини: Поінформованість є ключовою». www.cdc.gov/feature/valleyfever/ Доступ до 1 червня 2016 року.
- 2 Б. Чу та ін. «Похідне бензимідазолу, що проявляє протипухлинну активність, блокує активність EGFR та HER2 та покращує DR5 у клітині раку молочної залози». Смерть клітин і хвороби 6 (2015) :e1686
- 3 ДЖ.-Х. Пан та ін. «Ніклозамід, старий протигельмінтний засіб, демонструє протипухлинну активність, блокуючи кілька сигнальних шляхів ракових стовбурових клітин». Китайський журнал раку 31 № 4 (2012) :178—184.
- 4 Ф. Імпері та ін. «Нове життя для старого препарату: Антигельмінтний препарат Ніклозамід інгібує зондування кворуму Pseudomonas aeruginosa». Антимікробні засоби та хіміотерапія 57 № 2 (2013) :996-1005.
- 5 А. Юргейт та ін. «Ніклозамід є носієм протонів і орієнтується на кислі ендосоми з широкими противірусними ефектами». Патогени ЛОС 8 № 10 (2012): e1002976.
- 6 М.Ю. Абзуг. «Ентеровіруси: проблеми, які потребують лікування». Журнал інфекції 68 немає. С1 (2014) :108—14.
- 7 Б.Л. Перлман. «Інгібітори протеази для лікування хронічної інфекції гепатиту С генотип-1: новий стандарт догляду». Інфекційні хвороби ланцета 12 № 9 (2012) :717—728.
