8.9: Дозволені значення J - загальне квантове число кутового моменту
- Page ID
- 26753
- Порівняти дві спінові орбітальні схеми зв'язку, які з'єднують сумарні спінові кутові моменти та сумарні орбітальні кутові моменти багатоелектронного спектра
Потрібно вміти ідентифікувати електронні стани, що виникають в результаті заданої електронної конфігурації, і визначати їх відносні енергії. Електронний стан атома характеризується питомою енергією, хвильовою функцією (включаючи спін), конфігурацією електронів, загальним кутовим імпульсом та способом з'єднання орбітальних та спінових кутових моментів різних електронів. Існує два опису зчеплення кутового моменту. Один називається j-j муфтою, а інший називається L-S муфтою. Схема муфти j-j використовується для важких елементів (z > 40), а схема з'єднання L-S використовується для більш легких елементів. Тільки L-S муфта розглядається нижче.
L-S Муфта кутового моменту
Муфта L-S також називається муфтою R-S або Russell-Saunders. У L-S-зв'язку орбітальні і спінові кутові моменти всіх електронів об'єднані окремо
\[L = \sum _i l_i \label{8.11.3} \]
\[S = \sum _i s_i \label{8.11.4} \]
Сумарний вектор кутового імпульсу тоді є сумою загального орбітального вектора кутового імпульсу та загального вектора кутового імпульсу спіна.
\[J = L + S \label{8.11.5} \]
Загальне квантове число моменту імпульсу параметризує сумарний момент моменту даної частинки, поєднуючи його орбітальний кутовий імпульс та власний кутовий імпульс (тобто його спін). Через спін-орбітальну взаємодію в атомі орбітальний кутовий момент більше не комутується з гамільтоном, а також не спін.

Однак загальний момент імпульсу\(J\) робить коммутіруют з гамільтоніаном і так є постійною руху (не змінюється в часі). Відповідними визначеннями кутових моментів є:
Орбітальний кутовий момент
\[|\vec{L}| = \hbar \sqrt{\ell(\ell+1)} \nonumber \]
з його проекцією на вісь z\[L_z = m_\ell \hbar \nonumber \]
Спін Кутовий імпульс
\[ |\vec{S}| = \hbar \sqrt{s(s+1)} \nonumber \]
з його проекцією на вісь z\[ S_z = m_s \hbar \nonumber \]
Загальний кутовий момент
\[ |\vec{J}| = \hbar \sqrt{j(j+1)} \nonumber \]
з його проекцією на вісь z\[ J_z = m_j \hbar \nonumber \]
де
- \(l\)азимутальне квантове число одного електрона,
- \(s\)є спіновим квантовим числом, властивим електрону,
- \(j\)- сумарне квантове число кутового моменту електрона,
Квантові числа приймають значення:
\[\begin{align} & m_\ell \in \{ -\ell, -(\ell-1) \cdots \ell-1, \ell \} , \quad \ell \in \{ 0,1 \cdots n-1 \} \\& m_s \in \{ -s, -(s-1) \cdots s-1, s \} , \\& m_j \in \{ -j, -(j-1) \cdots j-1, j \} , \\& m_j=m_\ell+m_s, \quad j=|\ell+s|\\\end{align} \nonumber \]
і величини такі:
\[\begin{align} & |\textbf{J}| = \hbar\sqrt{j(j+1)} \\& |\textbf{J}_1| = \hbar\sqrt{j_1(j_1+1)} \\& |\textbf{J}_2| = \hbar\sqrt{j_2(j_2+1)} \\\end{align} \nonumber \]
в якому
\[ j \in \{ |j_1 - j_2|, |j_1 - j_2| - 1 \cdots j_1 + j_2 - 1, j_1 + j_2 \} \,\! \nonumber \]
Цей процес може повторюватися для третього електрона, потім четвертого тощо, поки не буде знайдений загальний кутовий момент.
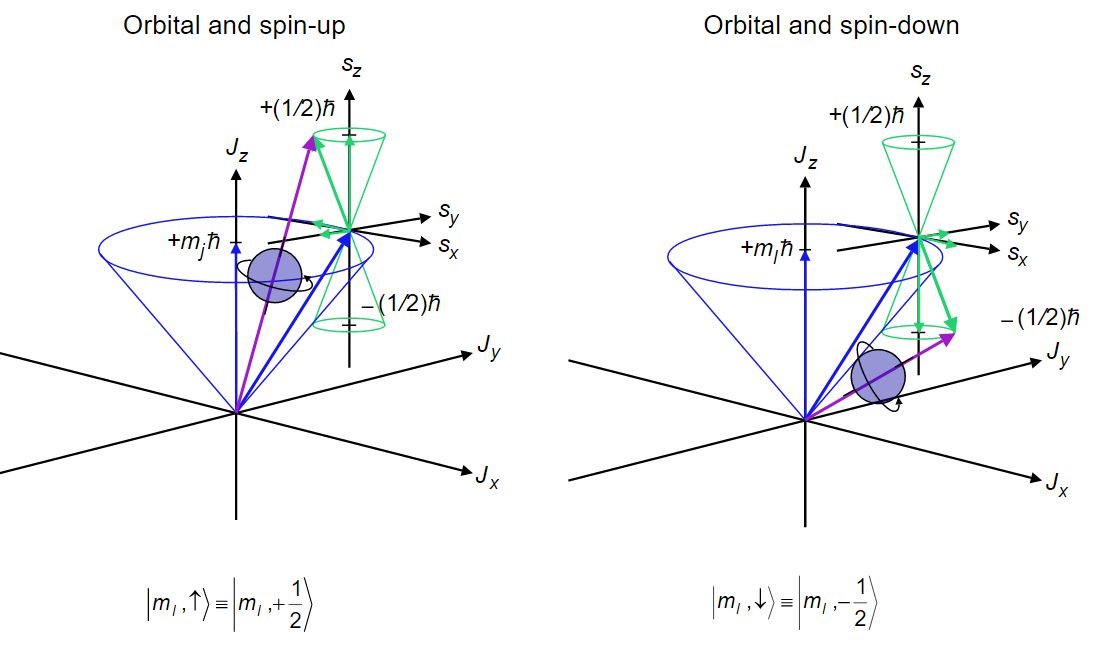
Результат цих векторних сум задається в коді, який називається символом терміна Рассела-Сондерса, і кожен символ терміна ідентифікує енергетичний рівень атома. Отже, енергетичні рівні також називаються термінами. Термін символ має вигляд,\(^{2s+1} L_J\) де кодова буква, яка використовується для загального орбітального кутового моменту квантового числа L = 0, 1, 2, 3, 4, 5 - S, P, D, F, G, H відповідно. Зверніть увагу, як цей код відповідає тому, який використовується для атомних орбіталей. Верхній індекс\(2S+1\) дає спіновий кратність стану, де S - сумарне квантове число спінового моменту моменту. Кратність спина - це кількість спінових станів, пов'язаних із заданим електронним станом. Щоб не переплутати кодову букву S для орбітального моменту моменту зі спіновим квантовим числом S, необхідно уважно вивчити контекст, в якому він використовується. У терміновому символі індекс J дає загальне квантове число моменту моменту. Через спін-орбітального зв'язку, тільки\(J\) і\(M_j\) є дійсними квантові числа, а тому, що спін-орбітальна зв'язок слабка\(L\)\(M_l\)\(S\), і\(m_s\) все ще служать для ідентифікації та характеристики станів для більш легких елементів.
Наприклад, стан землі, тобто найнижчий енергетичний стан атома водню, відповідає конфігурації електронів, в якій електрон займає 1-ю просторову орбіту і може мати або спін,\(\alpha\) або спін\(\beta\). Термін символ для основного стану є\(^2 S_{1/2}\), який читається як «дуплет S 1/2». Спіновий квантове число дорівнює 1/2, тому верхній індекс 2S+1 = 2, що дає спінові кратність стану, тобто кількість спінових станів дорівнює 2 відповідним\(\alpha\) і\(\beta\). S у терміні символ вказує на те, що сумарне квантове число орбітального моменту дорівнює 0 (Для основного стану водню існує лише один електрон і він знаходиться в s-орбітальному с\(l = 0\)). Індексит ½ відноситься до загального квантового числа моменту моменту. Загальний кутовий імпульс - це сума спінових і орбітальних кутових моментів для електронів в атомі. У цьому випадку загальне квантове число моменту моменту - це всього лише квантове число спінового моменту, ½, оскільки орбітальний кутовий імпульс дорівнює нулю. Основний стан має виродження два, оскільки загальний кутовий імпульс може мати проекцію осі z\(+\frac {1}{2} \hbar\) або\(-\frac {1}{2} \hbar\), що відповідає\(m_J\) = +1/2 або -1/2 в результаті двох електронних спінових станів\(\alpha\) і\(\beta\). Ми також можемо сказати, еквівалентно, що термін основного стану або енергетичний рівень є дворазовим виродженим.
Напишіть символ терміна для стану, який має 0 як для спінових, так і для орбітальних квантових чисел кутового моменту.
Напишіть термін символ для стану, який має 0 для спіна і 1 для орбітального кутового моменту квантових чисел.