29.5: Співвідношення властивостей полімеру зі структурою
- Page ID
- 106176
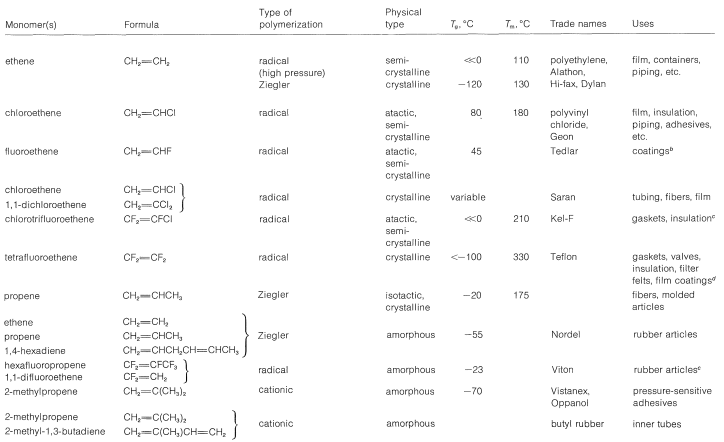
Властивості багатьох комерційно важливих термопластичних і еластичних полімерів можна зрозуміти з точки зору їх хімічної структури, використовуючи концепції, розроблені в попередньому розділі. Таким чином, прості лінійні полімери, поліетилен\(\ce{-(CH_2CH_2)}_n-\), поліметанал\(\ce{-(CH_2-O)}_n-\) і політетрафторетен\(\ce{-(CF_2-CF_2)}_n-\), з регулярними ланцюгами і низькими бар'єрами для обертання навколо зв'язків в ланцюзі мають тенденцію бути в значній мірі кристалічними з досить високими температурами плавлення і низькими температурами скла (див. Таблицю 29-1). Ситуація з поліхлоретеном (полівінілхлоридом), поліфторетеном (полівінілфторидом) та поліетиленілбензолом (полістиролом), як зазвичай готується, зовсім інша. Ці полімери набагато менш кристалічні і при цьому мають досить високі температури скла, що говорить про те, що між ланцюгами існує значна сила притягування. Низький ступінь кристалічності цих полімерів є результатом того, що вони мають низький ступінь регулярності стереохімічної конфігурації хіральних вуглеців в ланцюзі. Відкриття Г. Натта в 1954 році про те, що стереохімічні конфігурації хіральних центрів у полімерних ланцюгах можуть мати вирішальне значення при визначенні їх фізичних властивостей, зробило глибокий вплив як на практичні, так і на теоретичні аспекти хімії полімерів. Робота Натта була виконана насамперед з поліпропеном, і ця речовина є чудовим прикладом важливості стереохімічних конфігурацій.
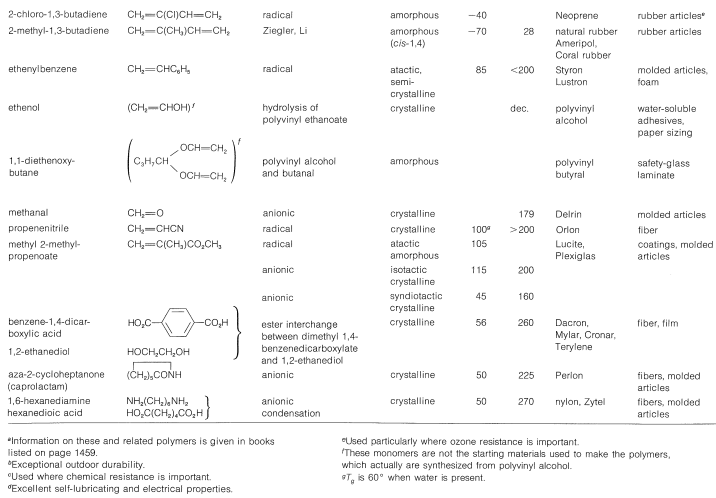
Таблиця 29-1: Представницькі синтетичні термопластичні та еластичні полімери та їх використання\(^a\)
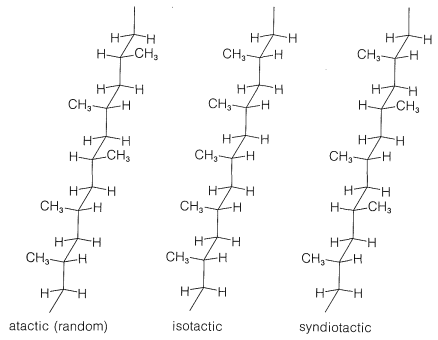
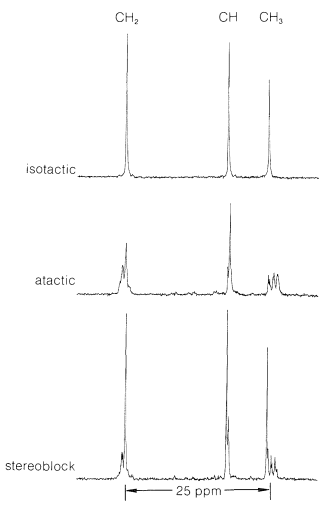
Існують разючі відмінності у фізичних властивостях між атактичною та ізотактичною формами. Атактичний матеріал м'який, еластичний, кілька липкий і досить розчинний в розчинниках, таких як 1,1,2,2-тетрахлоретан. Ізотаксичний поліпропен - твердий, прозорий, міцний кристалічний полімер, який плавиться при\(175^\text{o}\). Він практично не розчиняється у всіх органічних розчинниках при кімнатній температурі, але розчиняється в міру декількох відсотків в гарячому 1,1,2,2-тетрахлоретані. Що відмінність атактичних і ізотактичних полімерів ірисів від відмінностей конфігурацій метильних груп на ланцюгах показана вражаючим чином по\(\ce{^{13}C}\) ямр-спектрам (рис. 29-9). Відмінності в цих спектрах виникають внаслідок відмінностей у взаємодіях між метильними групами для різних конфігурацій, так само, як ми показали вам раніше для осьових та екваторіальних метильних груп на циклогексанових кільцях (Розділ 12-3D).
Чому поліпропен повинен плавитися набагато вище, ніж поліетилен (\(175^\text{o}\)проти\(110^\text{o}\))? Відповідь полягає в відмінностях між способом кристалізації полімерів. Поліетиленові кристаліти мають розширені зигзагоподібні ланцюги, які мають дуже низькі бар'єри для обертання навколо\(\ce{C-C}\) зв'язків. Через перешкоди між метильними групами поліпропен не кристалізується в розширених зигзагоподібних ланцюгах, а замість цього утворює спіраль, щось на зразок\(\alpha\) спіралі (Розділ 25-8A), з ланцюгом вуглецю зсередини та метиловими вуглецями зовні. Ці котушки більш жорсткі, ніж розширені\(\ce{CH_2}\) ланцюги в поліетилені, і мають стабілізуючі міжланцюгові\(\ce{H} \cdots \ce{H}\) взаємодії, так що для плавлення потрібна більш висока температура. Поліпропен може бути холодно витягнутий, утворюючи волокна, що нагадують нейлонові волокна, хоча, як можна було очікувати, ці волокна не відповідають температурі\(270^\text{o}\) плавлення нейлону і через їх вуглеводневого характеру набагато складніше фарбувати.
Хоча і лінійний поліетилен, і ізотактичний поліпропен є кристалічними полімерами, етен-пропенові сополімери, приготовані за допомогою каталізаторів Циглера, є чудовими еластомерами. Мабуть, більш-менш випадкове введення метильних груп по поліетиленовому ланцюгу знижує кристалічність досить різко, щоб привести до утворення аморфного полімеру. Етино-пропеновий сополімер - недорогий еластомер, але не має подвійних зв'язків, не здатний до вулканізації. Полімеризація етена і пропену в присутності невеликої кількості дициклопентадієну або 1,4-гексадієну дає ненасичений гетерополімер, який можна вулканізувати сіркою звичайним способом.

Обґрунтування використання цих конкретних дієнів полягає в тому, що тільки напружена подвійна зв'язок дициклопентадієну і кінцева подвійна зв'язок 1,4-гексадієну піддаються полімеризації за допомогою каталізаторів Циглера. Отже, полімерні ланцюги містять один подвійний зв'язок для кожної молекули дициклопентадієну або 1,4-гексадієну, яка включена. Ці подвійні зв'язки згодом можуть бути перетворені в поперечні зв'язки шляхом вулканізації сіркою (Секції 13-4 і 29-3).
Поліхлоретен (полівінілхлорид), як зазвичай готується, атактичний і не дуже кристалічний. Він відносно крихкий і склоподібний. Властивості полівінілхлориду можна поліпшити за допомогою сополімеризації, як у випадку з етенилетаноат (вінілацетат), який виробляє більш м'який полімер («Вініліт») з кращими формувальними властивостями. Полівінілхлорид також може бути пластифікований шляхом змішування його з речовинами низької летючості, такими як трис- (2-метилфеніл) фосфат (трикрезилфосфат) і дибутилбензол-1,2-дикарбоксилат (дибутилфталат), які при розчиненні в полімері мають тенденцію руйнувати його склоподібну структуру. Пластифікований полівінілхлорид є досить гнучким і широко використовується в якості електроізоляції, пластикового покриття тощо.
Таблиця 29-1 містить інформацію про ряд репрезентативних важливих полімерів і їх застосуванні. Деякі аналогічні дані по іншим полімерам вже наводяться (Розділ 13-4 і табл. 10-4). Важливе використання модифікованих полімерів як іонообмінних смол розглянуто в розділі 25-4С.
