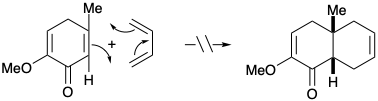4.9: Навчальні питання
- Page ID
- 18770
1. Обведіть «загальні атоми» у цинкасіолі D 1, diterpene, а потім проведіть хвилясті лінії через кожен зв'язок C-C, який включає принаймні один загальний атом і який лежить на приголосному ланцюзі (зверніться до вашої відповіді на питання 4 в розділі 1 для аналізу полярної реактивності цинкасіолу D 1). Можливо, ви захочете використовувати наведені нижче структури як шаблони для деяких ваших малюнків. Просто «вибілити» небажані облігації.
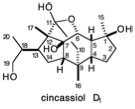
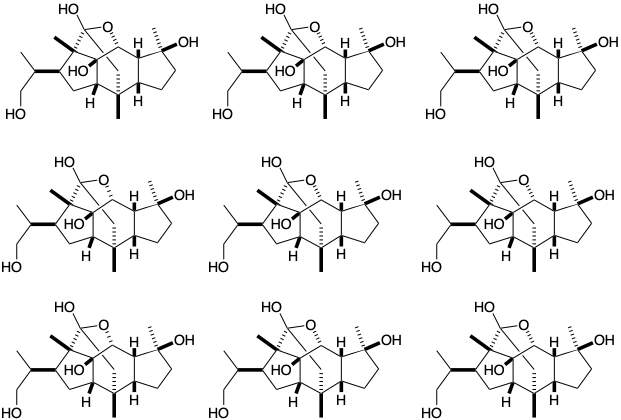
(а) Для кожного з дислокацій, запропонованих вашим топологічним аналізом та посилаючись на ваш попередній полярний аналіз, намалюйте синтепон, який теоретично може забезпечити цільовий скелет полярними реакціями, що утворюють зв'язок С-С.
(b) Для деяких з цих синтонів малюють функціоналізований попередник (синтетичний еквівалент), який може бути використаний в прямому полярному синтезі мішені або який може бути використаний в полярному синтезі, що вимагає додавання метильної групи та/або формування гетероциклічного зв'язку C-O після завершення багатоциклічний вуглецевий скелет шляхом формування полярних C-C-зв'язків.
(c) Для решти синтонів, які містять приголосні схеми, які блокуються четвертинними центрами, синтетичні еквіваленти, що експлуатують полярну активацію, що забезпечується цільовими функціональними групами, недоступні, оскільки сполучення цих функціональних груп з одним або обома реагуючими вуглецевими центрами не легко досягається без попереднього розщеплення додаткових вуглецево-вуглецевих зв'язків. Позначте ці синтетони як «ЗАБЛОКОВАНІ».
2. Дедукція ймовірних біосинтезів терпенів дає чудову можливість практикувати ретросинтетичний аналіз з набором граничних умов: (а) ізопентенілпірофосфат як вихідний матеріал, (б) ациклічний олігомер від голови до хвоста як проміжний продукт, (c) карбокатіонний електрофіл і C = C π-зв'язок нуклеофіл для формування зв'язків С-С, (d) всі реакції проміжних продуктів карбокатів як потенційні етапи, наприклад, β-протонна втрата, і перебудова за допомогою зсувів 1,2-С або гідридних зрушень.
(а) Вивести ймовірні біосинтези для наступних регулярних сесквітерпенів:
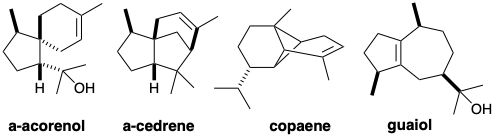
Підказка: зверніть увагу і подумайте про будь-які подібності в структурах α-акоренолу і α-цедрену.
(б) Цинкасіол D 1 є регулярним дітерпеном. У наступній структурі: (а) обведіть одиниці ізопрену, (б) проведіть хвилясті лінії через всі зв'язки C-C, які не є зв'язками всередині одиниць ізопрену, (c) для тих неізопренових зв'язків, які були б присутні в ациклічному геранілгеранілпірофосфатному попереднику цинкасіолу D 1, позначте кінці h або t для позначення голови або хвоста атома ізопрену одиниці.
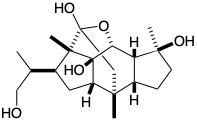
(c) Намалюйте коло навколо кожного з «загальних атомів» (як визначено Корі) у наступній структурі ланостерину (1).
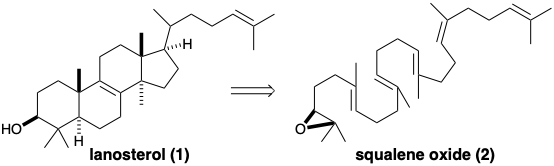
(d) Опишіть топологічну стратегію біосинтезу ланостерину (1) з оксиду сквалену (2).
(e) Написати механізм циклізації полієну та перестановки, що беруть участь у біосинтезі ланостерину (1) з оксиду сквалену (2). Покажіть потік електронів зі стрілками, що вказують від електронних пар в реагентах до їх майбутнього розташування в початкових продуктах. Покажіть циклізацію полієну як єдиний узгоджений процес, що включає кілька електронних пар і веде до проміжного катіону. Потім показати перестановку цього проміжного продукту на ланостерол як інший узгоджений процес, що включає рух декількох електронних пар.
3. Малюючи відповідні резонансні форми ключового катіонного та ключового аніонного проміжного продукту, напишіть механізм, який показує, як реакція формування зв'язку C-C між 3 і 4 генерує 5 процесом, який спирається на стабілізуючий вплив функціональності в 3 і 4, що пов'язано з 3-гідроксильною та 17-кето групами в кінцевій синтетичній мішені, естрону (6).
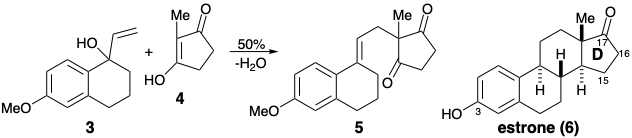
Підказка: 4 - це вінілологічна карбонова кислота.
4. Для кожної з наступних реакцій, які генерують тризаміщений алкен стереоселективно, яка рушійна сила і чому вона є стереоспецифічною?
(а)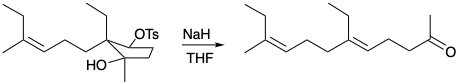
(б)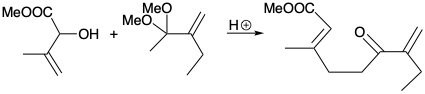
(c)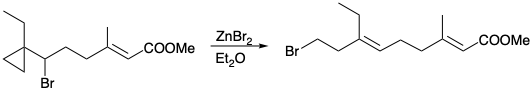
5. Чудова реакція виникає при УФ-опроміненні 7 і 8. Продукт 9, який містить скелет логаніну, генерується стереоселективно.
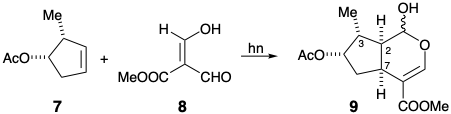
(а) Напишіть механізм для цієї реакції. Покажіть потік електронів зі стрілками, що вказують від електронних пар в реагентах до їх майбутнього розташування в початкових продуктах.
(b) Використовуйте один або кілька з наступних термінів, щоб відповісти на кожне з наступних питань: термодинамічне управління, стереоелектронне управління, стеричне управління підходом або тимчасовий міст. Як досягається стереоконтроль: (i) в положенні 3 щодо позиції 2 в 9? (ii) на 7-позицію щодо 2-позиції в 9?
6. У синтезі Кодзіма-Саки PGF 1α відносна стереохімія в позиціях 8, 9 і 12 встановлюється в перетворенні 10 в 11.
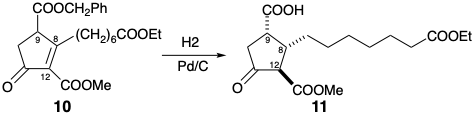
Як досягається стереоконтроль: (i) в положенні 12 щодо позиції 9 в 11? (б) на 8- позиції щодо 9-позиції в 11?
7. Кожна з наступних реакцій дає збій через фатального вади. Для кожної реакції намалюйте структуру власне продукту.
(а)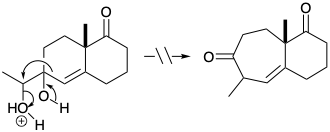
(б)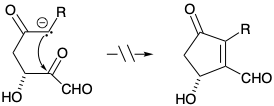
(c)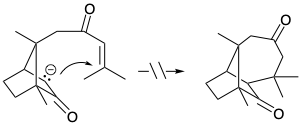
(г)