6.3: Абсолютна конфігурація та система (R) та (S)
- Page ID
- 23672
Мета навчання
- назва хіральних сполук з використанням (R) & (S) номенклатури
ВИКОРИСТОВУЙТЕ ВАШ МОДЕЛЬНИЙ КОМПЛЕКТ: Моделі допомагають візуалізувати структуру. Під час використання моделі переконайтеся, що найнижчий пріоритет вказує на вас. Потім визначте напрямок від найвищого пріоритету замінника до найнижчого: за годинниковою стрілкою (R) або проти годинникової стрілки (S).
ЯКЩО У ВАС НЕМАЄ КОМПЛЕКТУ ДЛЯ МОДЕЛЮВАННЯ: пам'ятайте, що тире означають, що зв'язок збирається в екран, а клини означають, що зв'язок виходить з екрану. Якщо найнижчий пріоритет зв'язок не вказує на спину, подумки поверніть її так, щоб вона була. Однак дуже корисно при вивченні органічної хімії використовувати моделі.
Якщо у вас є набір для моделювання, використовуйте його, коли ви читаєте цей розділ і працюєте над проблемами практики.
Вступ та правила пріоритету Chan-Ingold-Prelog
Щоб однозначно назвати енантіомери сполуки, їх назви повинні включати в себе «врученість» молекули. Букви «R» і «S» визначаються шляхом застосування правил Чан-Інгольд-Прелог (CIP). Оптична активність (+/-) також може передаватися в назві, але повинна бути емпірично виведена. Існують також біохімічні умовності для вуглеводів (цукрів) і амінокислот (будівельних блоків білків).
Метод однозначного присвоєння врученості молекул зародився трьома хіміками: Р.С.Каном, К.Інгольдом і В.Прелогом і, як такий, також часто називають правилами Чан-Інгольда-Прелога. Крім системи СІП, існує два способи експериментального визначення абсолютної конфігурації енантіомера:
- Рентгенівський дифракційний аналіз. Відзначимо, що немає кореляції між знаком обертання і будовою того чи іншого енантіомера.
- Хімічна кореляція з молекулою, структура якої вже визначена за допомогою рентгенівської дифракції.
Однак для нелабораторних цілей вигідно орієнтуватися на систему R/S. Ознака оптичного обертання, хоча і відрізняється для двох енантіомерів хіральної молекули, при однаковій температурі, не може бути використаний для встановлення абсолютної конфігурації енантіомера; це пов'язано з тим, що знак оптичного обертання для конкретного енантіомера може змінюватися, коли температура зміни.
Правила пріоритету Chan-Ingold-Prelog засновані на атомних номерах атомів, що цікавлять. Для хіральності атоми, що представляють інтерес, - це атоми, пов'язані з хіральним вуглецем.
- Атом з більшим атомним номером має вищий пріоритет (I > Br > Cl > S > P > F > O > N > C > H).
- При порівнянні ізотопів атом з більшим числом маси має вищий пріоритет [18 O > 16 O або 15 N > 14 N або 13 C > 12 C або T (3 H) > D (2 H) > H].
- Коли є зв'язок у (2) вище, встановіть відносний пріоритет, перейшовши до наступного атома (ів) уздовж ланцюга, поки не буде спостерігатися перша різниця.
Кілька зв'язків розглядаються так, ніби кожен зв'язок множинного зв'язку пов'язаний з унікальним атомом. Наприклад, етенильна група (СН 2 = СН) має вищий пріоритет, ніж етилова група (СН 3 СН 2). Пріоритет етилового вуглецю - це «дві» зв'язки з атомами вуглецю і один зв'язок з атомом водню порівняно з етиловим вуглецем, який має лише один зв'язок з атомом вуглецю і два зв'язки з двома атомами водню. Аналогічно, вуглецево-вуглецевий потрійний зв'язок ацетилену надасть йому вищий пріоритет CIP, ніж етенильна група, як узагальнено нижче.
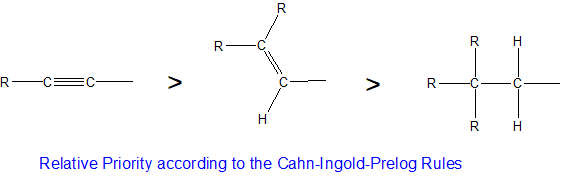
Стереоцентри маркуються R або S
Номенклатура «права рука» і «ліва рука» використовується для назви енантіомерів хірального з'єднання. Стереоцентри позначені як R або S.
Розглянемо діаграму вище зліва: вигнута стрілка намальована проти годинникової стрілки (c-cw) від замісника найвищого пріоритету (1) до замісника найнижчого пріоритету (4) в t he S - конфігурація («Sinister» → Latin=» ліворуч»). Напрямок проти годинникової стрілки можна розпізнати за рухом вліво при виході з 12 o 'положення годинника. Тепер розглянемо діаграму вище праворуч, де вигнута стрілка намальована за годинниковою стрілкою (cw) від замісника найвищого пріоритету (1) до найнижчого пріоритетного замінника (4) у конфігурації R («Rectus» → Latin= «праворуч»). R або S потім додається як префікс, у дужках, до назви енантіомера, що цікавить. Номер локатора необхідний, якщо є більше одного хірального центру. В іншому випадку людина, яка читає ім'я, як очікується, розпізнає хіральний центр.
Приклад 1
Дві хіральні сполуки нижче намальовані, щоб підкреслити хіральний вуглець з повною хімічною назвою під кожною структурою.
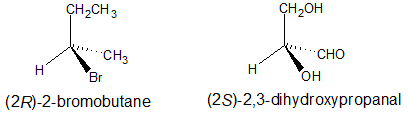
Абсолютні конфігурації перспективних формул
Хімікам потрібен зручний спосіб відрізнити один стереоізомер від іншого. Система Chan-Ingold-Prelog - це набір правил, який дозволяє однозначно визначити стереохімічну конфігурацію будь-якого стереоцентру, використовуючи позначення «R» (від латинського rectus, що означає правша) або 'S' (від латинська зловісна, що означає лівша).
Правила цієї системи стереохімічної номенклатури, на поверхні, досить прості.