9.2: Озон
- Page ID
- 17869
Озон (O 3) - це алотроп кисню, який набагато менш стійкий, ніж двоатомна молекула (O 2). Приземний озон є забруднювачем повітря з шкідливим впливом на дихальну систему, тоді як озоновий шар у верхній атмосфері фільтрує потенційно пошкоджуючий ультрафіолетове світло від досягнення поверхні Землі.
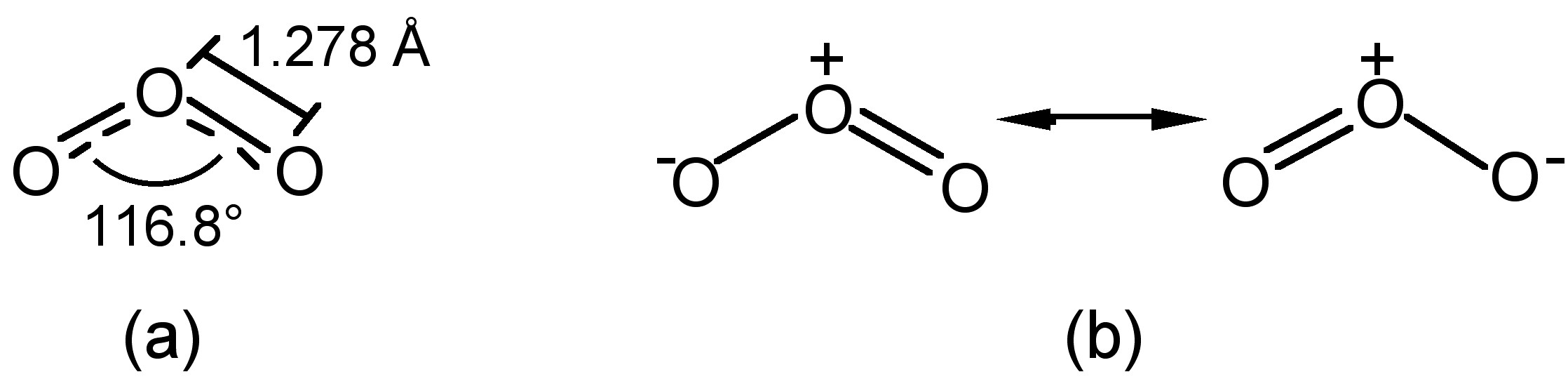
Структура озону вигнута, з симетрією С 2v, схожа\(\PageIndex{1}\) на воду (рис. Центральний кисень має sp 2 гібридизацію з однією самотньою парою. Внаслідок вигнутої структури і резонансної гібридизації (рис.\(\PageIndex{1}\) Б) озон являє собою полярну молекулу (дипольний момент = 0,5337 D).
Озон виробляється шляхом впливу кисню (О 2) електричним розрядом. Озон має характерний запах, який зазвичай може пахнути після удару освітлення; насправді назва озон походить від грецького ozein, що означає запах. У лабораторії озон також може бути отриманий електролізом з використанням катода графітового стрижня, анода з платинового дроту та електроліту сірчаної кислоти (3 М). Реакції половини клітин такі:
\[ \rm 3 H_2O \rightarrow O_3 + 6 H^+ + 6e^- \space\space\space\space\space\space\space (\Delta E_o = -1.53V)\]
\[ \rm 6 H^+ + 6 e^- \rightarrow 3 H_2 \space\space\space\space\space\space\space (\Delta E_o = 0 V)\]
\[ \rm 2 H_2O \rightarrow O_2 + 4 H^+ + 4 e^- \space\space\space\space\space\space\space (\Delta E_o = -1.23 V)\]
Озон також утворюється шляхом фотолізу кисню (Equation\ ref {9.2.4} і\ ref {9.2.5}), як в лабораторії, так і в атмосфері.
\[ \rm O_2 \xrightarrow{h\nu} 2 O\cdot \label{9.2.4}\]
\[ \rm O\cdot + O_2 \rightarrow O_3 \label{9.2.5}\]
Озон є дуже сильним окислювачем і легко окислює цілий ряд матеріалів, наприклад, Рівняння\ ref {9.2.6} і\ ref {9.2.7}. Він також окислює метали (крім золота, платини та іридію) до найвищого ступеня окислення, наприклад, Equation\ ref {9.2.8}.
\[ \rm O_3 + CO \rightarrow CO_2 + O_2 \label{9.2.6}\]
\[ \rm O_3 + 2 I^- + H_2O \rightarrow O_2 + 2OH^- + I_2 \label{9.2.7}\]
\[ \rm 2 Cu^+_{(aq)} + 2 H_3O^+_{(aq)} + O_{2(g)} \rightarrow 2 Cu^{2+}_{(aq)} + 3 H_2O_{(l)} + O_{2(g)} \label{9.2.8}\]
Озаниди металів, які містять аніон озоніду (O 3 -) вибухонебезпечні і повинні зберігатися при кріогенних температурах. Озоніди для всіх лужних металів відомі. KO 3, rBO 3 та CsO 3 можуть бути отримані з відповідних супероксидів.
\[ \rm KO_2 + O_3 \rightarrow KO_3 + O_2\]
Озон як модулятор життя на Землі
Атмосфера Землі виступає джерелом O 2 і сховищем CO 2, але вона також діє як щит для життя. По-перше, майже всі метеорити згоряють при вході через високі температури, породжені тертям атмосфери. По-друге, атмосфера діє як щит для високоенергетичного ультрафіолетового випромінювання.
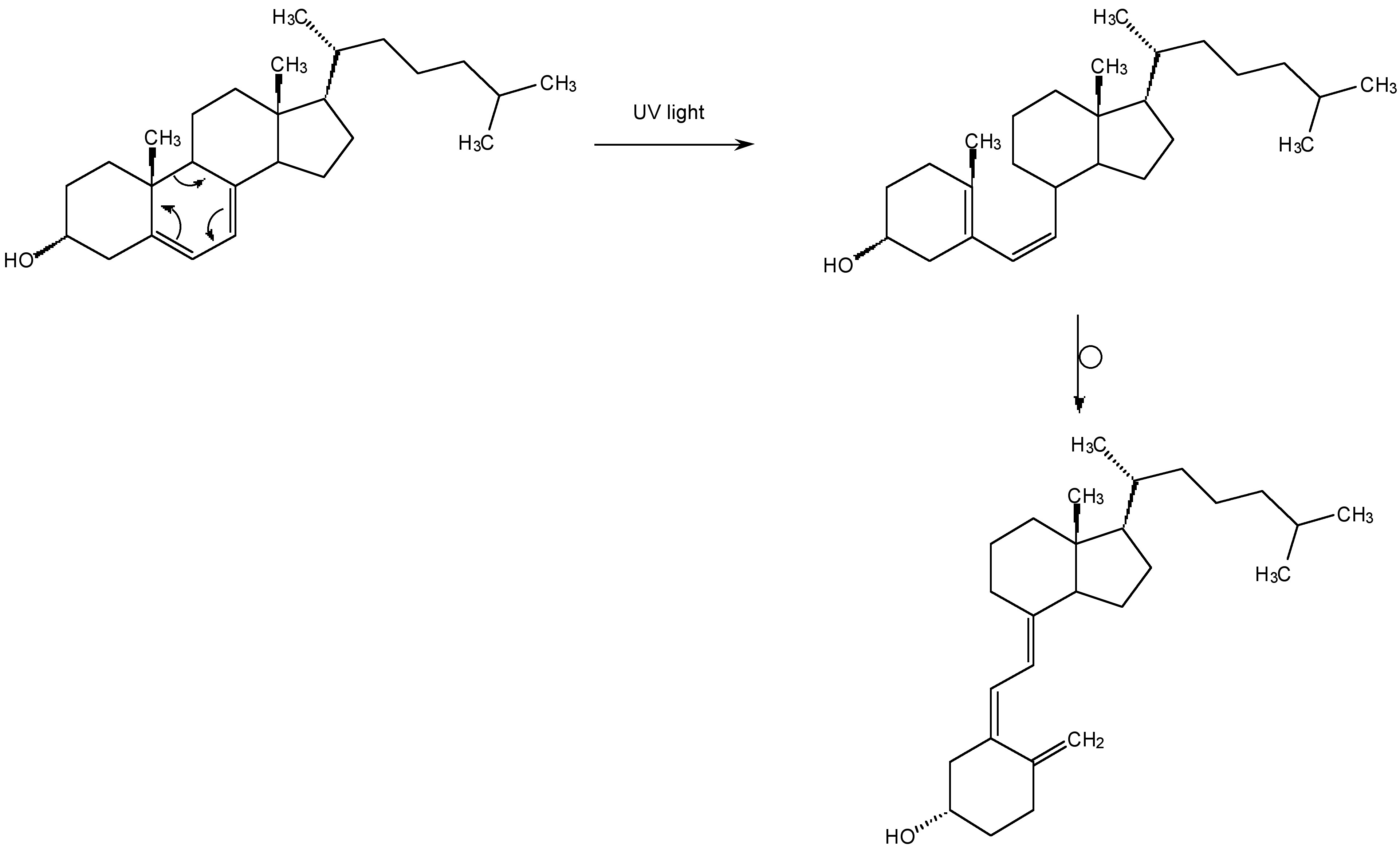
Хоча УФ-випромінювання перетворює 7-дегідрохолестерин в вітамін D3 в шкірі (рис.\(\PageIndex{2}\)), і тому корисно, висока енергія УФ руйнує живі клітини. Насправді затемнення, яке ми називаємо засмагою, насправді є механізмом організму для запобігання подальшому пошкодженню ультрафіолетом. Сонячний опік та рак шкіри спричинені відносно слабким ультрафіолетовим світлом, яке досягає поверхні Землі, без атмосфери ми б піддавалися впливу ультрафіолетового випромінювання високої енергії, що було б небезпекою для всього життя на Землі. «Сонцезахисний екран» Землі - це озон (O 3). А без озону у верхніх слоях атмосфери не було б життя на Землі.
Озоновий шар розташований в нижній частині стратосфери приблизно від 10 км до 50 км над Землею, хоча товщина змінюється сезонно і географічно. Цей шар містить понад 91% озону в атмосфері Землі і поглинає 93-99% ультрафіолетового світла високої частоти сонця. Озон розкладається фотолітично до O 2 та молекулярного кисню (9.2.10), і саме ця реакція становить захист атмосфери від ультрафіолетового випромінювання. Озон природним чином регенерується екзотермічною реакцією молекулярного кисню з O 2, (9.2.11).
\[ \rm O_3 + h\nu \rightarrow O_2 + O\]
\[ \rm O + O_2 \rightarrow O_3\]
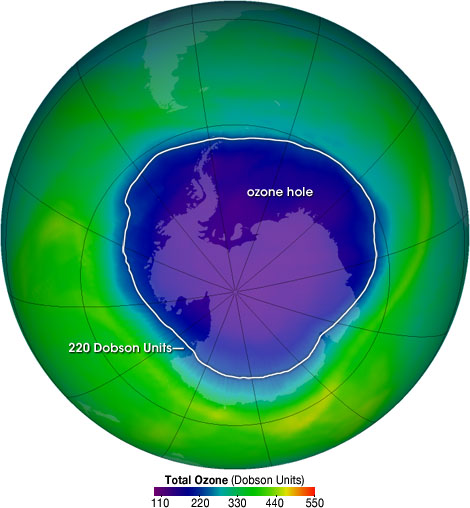
Таким чином, баланс між утворенням і руйнуванням озону є важливим механізмом захисту живих організмів на планеті. Хоча озоновий шар був відносно постійним на Землі протягом мільйонів років, останні 70 спостерігали різкі зміни, включаючи збільшення полярної діри в озоновому шарі. Озонова діра визначається географічно як область, де загальна концентрація озону менше 220 одиниць Добсона.
Озонова діра неухильно зростала в розмірах і тривалості існування протягом останніх двох з половиною десятиліть. В даний час розмір озонової діри над Антарктидою оцінюється приблизно в 30 млн кв.км (рис.\(\PageIndex{3}\)).