1.9: теорія смуг в твердих тілах
- Page ID
- 24289
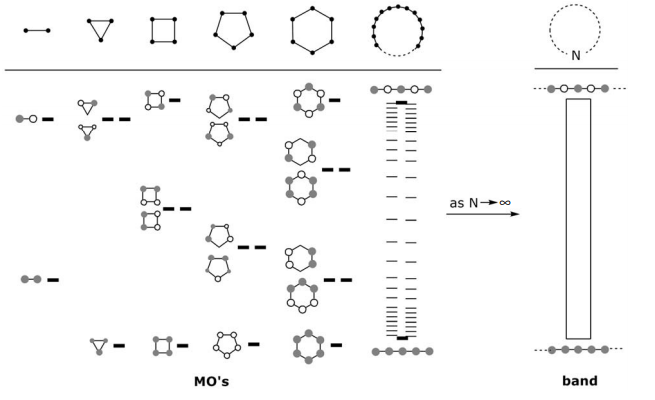
Метод LCAO для циклічних систем забезпечує зручну відправну точку для розробки електронної структури твердих тіл.
При дуже великому N, коли окружність кола наближається ∞, циклічна задача сходиться до лінійної,
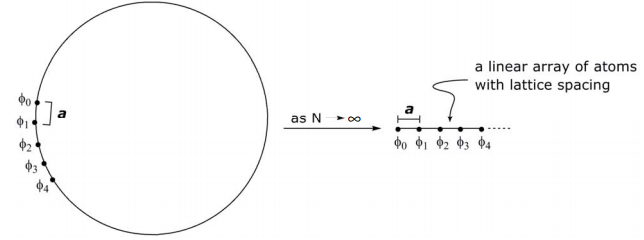
Якісно, з точки зору енергетичного рівня МО,
Більш кількісно, при переході від циклічних до лінійних систем замість опису орбітальних (атомних) позицій під кутом положення атома описується m a, де m - число атома в масиві, а a - відстань між атомами. Таким чином, θ N-циклічного похідного стає m a,
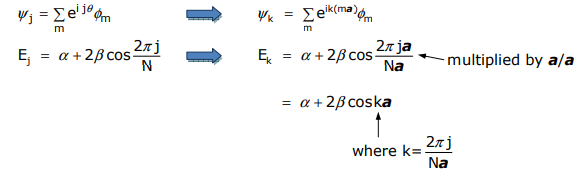
Кілька слів про\(k\). Це:
- міра кількості вузлів
- індекс хвильової функції і відповідно симетрія хвильової функції
- «квантове число» для заданого ψ k
- міра довжини, пов'язана з довжиною хвилі λ —1
- від відношення ДеБроля, λ = (h/p), тому k - це також хвильовий вектор, який вимірює імпульс
Повертаючись до вищевикладеного обговорення, зверніть увагу, що k параметрично залежить від a. Оскільки a - параметр решітки одиничної комірки, існує стільки k, скільки одиничних комірок у кристалі. У лінійному випадку одиничною коміркою є відстань між сусідніми атомами: є n атомів, n одиничних клітин або іншими словами — в 1-D ланцюжку стільки ж k, скільки атомів.
Визначимо енергетичні значення меж, k = 0 і k = (π/ a):
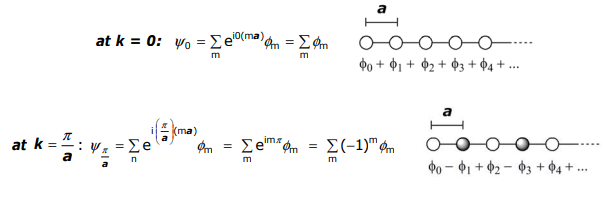
Енергії для цих смугових структур в межах k складають:
\[ E_{0} = \alpha + 2\beta \cos(0)a = \alpha + 2\beta \]
\[ E_{ \dfrac{ \pi }{a}} = \alpha + 2\beta \cos( \dfrac{ \pi }{a} )a = \alpha - 2\beta \]
Зауважте, що k квантовано; отже, існує кінцева кількість значень між α+2β і α—2β, але для дуже великої кількості (~10 23 атомів) між межами k. Таким чином, енергія є безперервною і плавно змінюється функцією між цими межами.
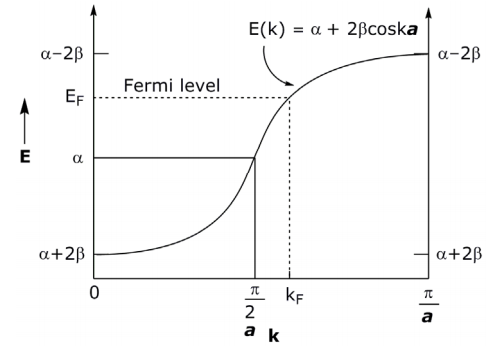
Діапазон - π/ a ≤ k ≤ π/ a або |k| ≤ π/ a є унікальним, оскільки функція повторює себе a a поза цими межами. Цей унікальний діапазон значень k називається зоною Бріллуена. Перша зона Бріллуена побудована вище від 0 до π/ a (симетричне відображення від − π/ a до 0).
При заданому числі e — s у твердому тілі рівні будуть заповнені до певної енергії, званої рівнем Фермі, яка відповідає певному значенню k (= k F). У наведеному вище прикладі k електронів більше, ніж орбіталей, тому k F > k/2 a. Якби кожна атомна орбіталь сприяла 1e — системі, то E F відбуватиметься для k F = π/2 a.
Симетрія окремих атомних орбіталів багато в чому визначає смугову структуру. Розглянемо p-орбіталі, що перекриваються в лінійному масиві (проти 1s орбіталів вищезазначеного лікування). Аналіз граничних форм:
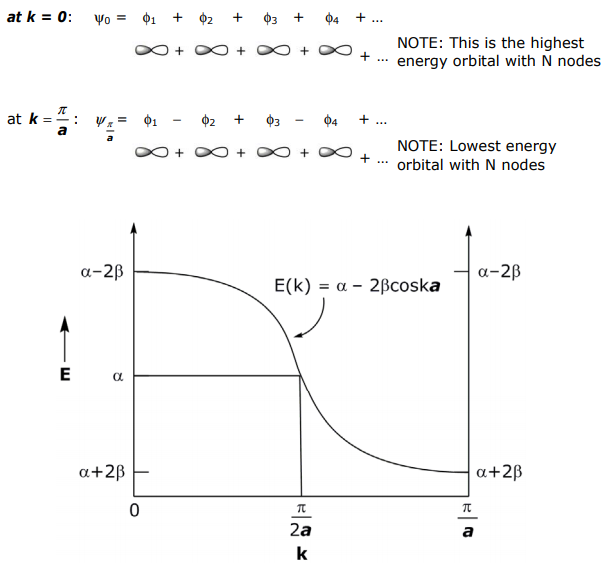
Енергетична смуга протилежна тому, що для sσ орбітальної LCAO, оскільки (+) LCAO для орбітальної pσ є антизв'язуючим.
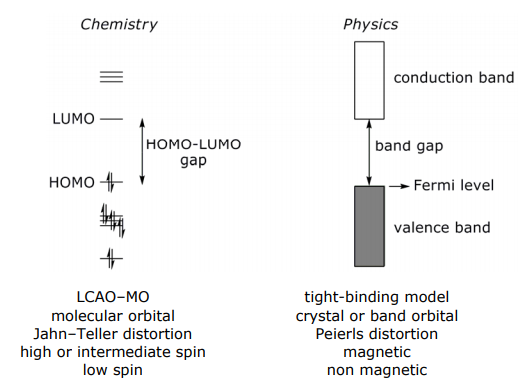
Таким чином, молекули легко пов'язані з твердими речовинами за допомогою теорії Хюкеля. Не дивно, що існує мова хімії, що описує електронну структуру молекул, яка пов'язана з мовою фізики, що описує електронну структуру твердих тіл. Нижче наведені деякі терміни, які хіміки і фізики використовують для опису подібних явищ в молекулах і твердих тілах:
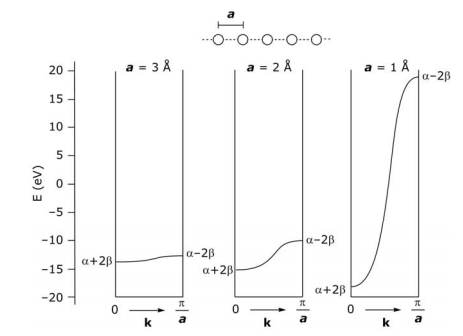
Ширина смуги або дисперсія
Від чого залежить ширина або дисперсія смуги? Що стосується HOMO-LUMO щілини в молекулі, то перекриття сусідніх орбіталей визначає енергетичну дисперсію смуги — чим більше перекриття, тим більше дисперсія. Зверніть увагу, як діапазонна дисперсія лінійного ланцюга атомів H змінюється, коли 1s орбіталі атомів H розташовані на відстані 1, 2, 3 Å один від одного (E ізольованого атома H становить —13,6 еВ):
Щільність держав
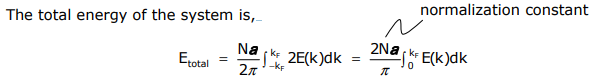
або іншими словами, це площа під кривою до кФ. Ще одна корисна величина - це кількість орбіталей між E (k) + dE (k), зване щільністю станів (DOS). Для 1-D системи,
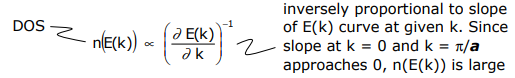
Сюжет вищенаведених рівнянь такий,
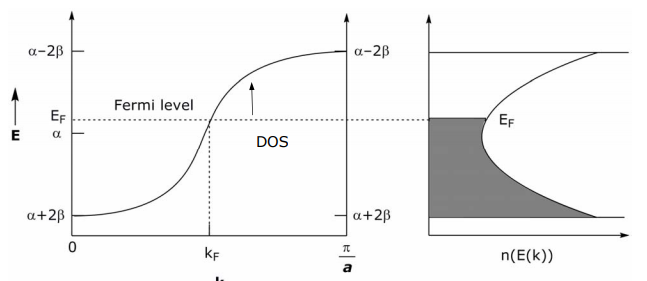
На наведеній вище діаграмі DOS жодна енергетична щілина не розділяє заповнену і порожню смуги, тобто існує безперервна щільність станів — ця властивість характерна для металу. Якщо енергетичний зазор між заповненими і порожніми орбіталями присутній і його можна термічно подолати, то це напівпровідник; енергетичний зазор, який неможливо подолати, - це ізолятор.
Приклад 1-D
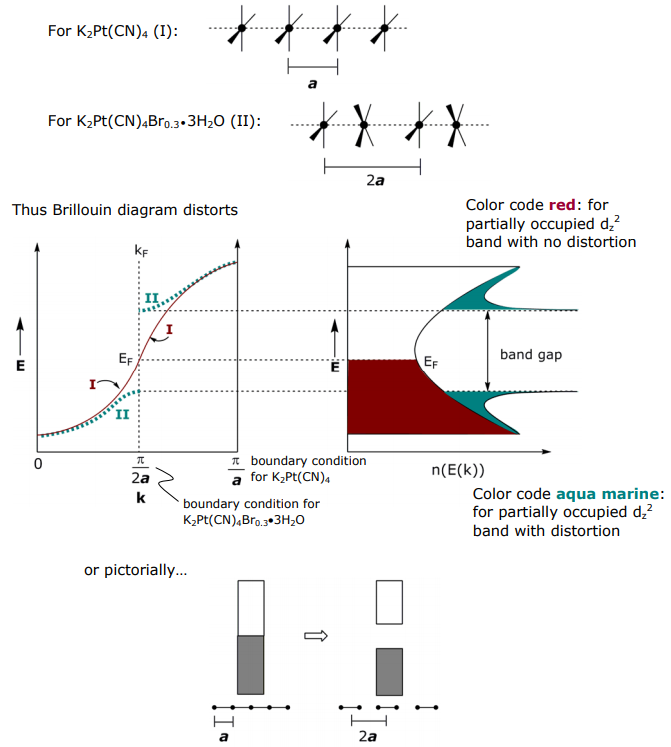
Можливо, найвідомішою системою 1-D в неорганічній хімії є K 2 Pt (CN) 4 та її частково окислена сполука (наприклад, K 2 Pt (CN) 4 Br 0.3).
Нормальний платиноціанід, K 2 Pt (CN) 4:
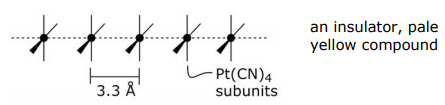
Частково окислений платиноціанід, K 2 Pt (CN) 4 Br 0,3 •3H 2 O:

Примітка: d (Pt-Pt) = 2,78 Å в металі Pt
Щоб пояснити ці розрізнені властивості 1-D сполук, розглянемо молекулярну субодиницю Pt (CN) 4 2-:
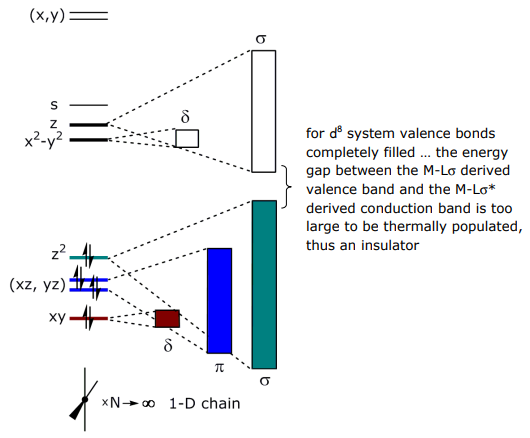
Розсіювання смуг обумовлено різними перекриттями орбіталей dσ, dπ і dδ.
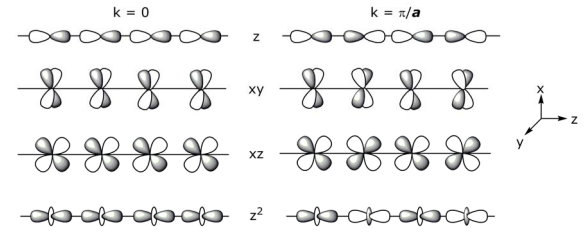
Структура смуги (або перші зони Бріллуена), що походить від прикордонних МО, є:
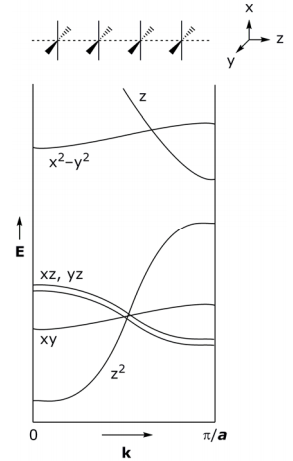
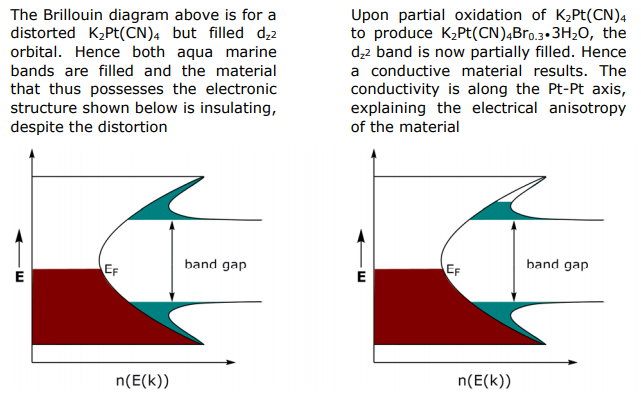
Для частково окисленої системи зв'язка σ, отримана з dz 2, повинна бути частково заповнена і, таким чином, металева, але це не так, частково окислений K 2 Pt (CN) 4 Br x є напівпровідником. Щоб пояснити цю аномалію, розглянемо, як порушується структура смуги при частковому окисленні:
Ізолюючись на смузі d z 2 в K 2 Pt (CN) 4, атоми Pt рівномірно розташовані з розмірністю решітки a (I). При окисленні ланцюг Pt може спотворюватися, щоб надати решітці розмірність 2 a (II). У випадку K 2 Pt (CN) 4 Br 0.3 •3H 2 O спотворення є обертанням субодиниць Pt і утворенням димерів всередині ланцюга, таким чином одиничний розмір комірки прищеплюється до кожного іншого атома Pt.