5.2.2: Орбітальне змішування
- Page ID
- 32855
У попередньому розділі ми ввели спрощену молекулярно-орбітальну (МО) діаграму, припускаючи, що взаємодії були обмежені виродженими орбіталями сумісної симетрії. Версія цієї спрощеної діаграми для гомоядерної діатоміки другого ряду показана на лівій стороні малюнка\(\PageIndex{1}\) (показані лише валентні орбіталі).
Насправді орбіталі сумісної симетрії можуть поєднувати або змішувати, навіть коли вони мають різну енергію. Коли набори орбіталів змішуються, це має ефект зменшення енергії набору нижчої енергії та збільшення енергії набору вищих енергій. Існує два способи пояснення змішування, описані в пунктах нижче. Діаграма праворуч від малюнка\(\PageIndex{1}\) показує, як на рівні енергії впливає змішування орбіти.
- Починаючи зі спрощеної діаграми МО і змішуючи молекулярні орбіталі подібної симетрії: Якщо ми почнемо зі спрощеної діаграми «без змішування», показаної зліва, ми можемо вибрати орбіталі з подібною симетрією і розглянути, що станеться, якщо ці молекулярні орбіталі змішуються. Наприклад, починаючи з діаграми МО в лівій частині малюнка\(\PageIndex{1}\), ми бачимо, що є дві\(\sigma_g\) орбіталі, які мають однакову симетрію (отже, вони мають однакові мітки симетрії). При змішуванні нижча енергія\(\sigma_g(2s)\) зменшиться в енергії, тоді як вища енергія\(\sigma_g(2p)\) збільшиться. Так само є дві\(\sigma_u^{*}\) орбіталі, які будуть змішуватися, зменшуючи енергію,\(\sigma_u^{*}(2s)\) одночасно збільшуючи енергію\(\sigma_u^{*}(2p)\).
- Починаючи з атомних орбіталів сумісної симетрії та змішування: Починаючи з атомних орбіталів, ми можемо вибрати орбіталі, які мають сумісну симетрію, щоб здійснити продуктивну взаємодію, і об'єднати їх як набір для створення молекулярних орбіталів. З двох наборів атомних орбіталів на правій панелі на малюнку\(\PageIndex{1}\) є два набори з чотирьох орбіталей з сумісною симетрією; один - набір двох\(2s\) і двох\(2p_z\) орбіталів. Ці чотири орбіталі можуть поєднуватися, утворюючи молекулярні орбіталі з\(\sigma\) симетрією. Вони об'єднуються, утворюючи один зв'язок з низькою енергією\(\sigma_g\), найвищу енергію\(\sigma_u^{*}\) та дві орбіталі з проміжною енергією (\(\sigma_g\), і\(\sigma_u^{*}\)). Ця обробка може бути виражена у вигляді лінійної комбінації чотирьох атомних орбіталей:\[\Psi=c_{1} \psi\left(2 s_{a}\right) \pm c_{2} \psi\left(2 s_{b}\right) \pm c_{3} \psi\left(2 p_{a}\right) \pm c_{4} \psi\left(2 p_{b}\right) \nonumber \] де коефіцієнти\(c_1=c_2\) і\(c_3=c_4\) для одноядерних двоатомних молекул.
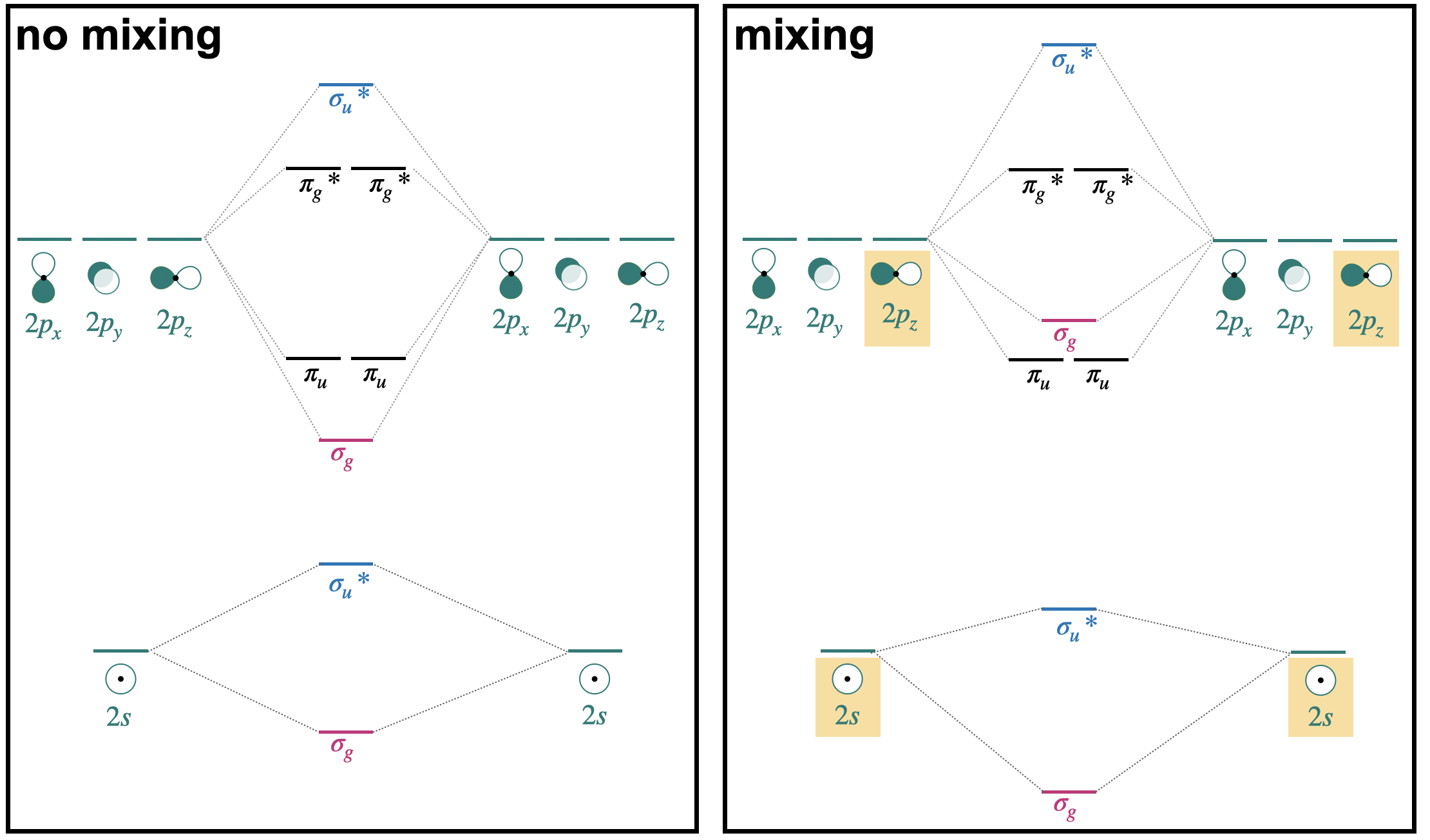
У випадку з одноядерними двоатомними молекулами другого ряду орбітальне змішування має важливі наслідки для енергетичного порядку\(\pi_u(2p)\) орбіталів\(\sigma_g(2p)\) і. Про це і піде мова в наступному розділі.
