1.6: Недосконале твердотільне
- Page ID
- 27779
ВСТУП
Справжні кристали ніколи не бувають ідеальними: вони завжди містять значну щільність дефектів і недосконалостей, які впливають на їх фізичні, хімічні, механічні та електронні властивості. Існування дефектів також відіграє важливу роль в різних технологічних процесах і явищах, таких як відпал, осадження, дифузія, спікання, окислення та інші. Слід зазначити, що дефекти не обов'язково роблять несприятливий вплив на властивості матеріалів. Існує багато ситуацій, коли розумний контроль типів та кількості недосконалостей може призвести до конкретних характеристик, бажаних у системі. Цього можна досягти правильними техніками обробки. По суті, «дефектна інженерія» постає як важливий вид діяльності.
Всі дефекти та недосконалості можна зручно розглядати за чотирма основними поділами: точкові дефекти, дефекти лінії або дислокації, плоскі дефекти або дефекти міжфазної або зернової межі та дефекти об'єму. Ми також можемо додати сюди макроскопічні або об'ємні дефекти, такі як пори, тріщини і сторонні включення, які вводяться в процесі виробництва і обробки твердого стану. Точкові дефекти притаманні рівноважному стану і таким чином визначаються температурою, тиском і складом даної системи. Наявність і концентрація інших дефектів, однак, залежать від способу первинного формування твердого тіла і подальшої обробки.
Коротко розглянемо вплив недосконалостей або кристалічних дефектів на кілька важливих властивостей твердих тіл. Наприклад, електрична поведінка напівпровідників значною мірою контролюється недосконалостями кристалів. Таким чином, провідність кремнію може бути змінена за типом (n або p) і більш ніж на вісім порядків за рахунок додавання дрібних кількостей електрично активних легуючих елементів. При цьому кожен атом легуючої речовини, закладеної заміщенням, являє собою точковий дефект кремнієвої решітки. Той факт, що такі малі кількості домішкових атомів можуть істотно змінювати електричні властивості напівпровідників, відповідає за розвиток транзистора і відкрило все поле технології твердотільних пристроїв. Практично жодне з напівпровідникових властивостей, що призвели до цих інженерних досягнень, не знайдено в «ідеальному» кристалі. Вони являють собою властивості, властиві дефектного твердого стану.
Наявність дислокацій (дефектів ліній) в кристалах забезпечує механізм, за допомогою якого може відбуватися постійна зміна форми або механічна деформація. Кристалічне тверде тіло, вільне від дислокацій, є крихким і практично марним як інженерний матеріал. Хоча існування дислокацій в кристалах забезпечує пластичність (здатність до деформації), теоретична міцність кристалічних твердих тіл різко знижується їх присутністю.
Слід визнати, що дислокації відіграють центральну роль у визначенні таких важливих властивостей, як міцність і пластичність. Насправді практично всі механічні властивості кристалічних твердих тіл в значній мірі контролюються поведінкою недосконалостей ліній.
Здатність феромагнітного матеріалу (наприклад, заліза, нікелю або оксиду заліза) намагнічуватися та розмагнічуватися значною мірою залежить від наявності двовимірних недосконалостей, відомих як стінки Блоха. Ці інтерфейси є кордонами між двома областями кристала, які мають різний магнітний стан. У міру намагнічування ці дефекти мігрують і своїм рухом забезпечують матеріалу чистий магнітний момент. Без існування стінок Блоха всі феромагнітні матеріали були б постійними магнітами. Насправді електромагнітів не існувало б, якби не цей тип дефекту.
Наявність дефектів поверхні, таких як тріщини, призводить до розриву крихких матеріалів, таких як скло, при невеликих прикладених напруженнях. Цей факт знайомий кожному, хто розбив скляну трубку, попередньо подавши в поверхню невелику виїмку (або тріщину). Видалення тріщин з поверхні скла або травленням в плавиковій кислоті, або поліруванням полум'ям майже завжди підвищує міцність на руйнування. Наприклад, скло при відсутності будь-яких поверхневих тріщин має міцність на руйнування\(\sim 10^{10} \mathrm{Newton} / \mathrm{m}^2\) (на відміну від справжнього скла, яке має міцність на руйнування\(\sim 0^7\) Ньютона\(/ \mathrm{m}^2\)).
ТОЧКОВІ ДЕФЕКТИ
Формування точкових дефектів
Незаперечний закон природи говорить: «Ніщо не є ідеальним». Цей закон застосовується як до людини, так і до неорганічного світу кристалічних твердих тіл і може бути сформульований як 2-й закон термодинаміки:
\[\mathrm{F}=\mathrm{H}-\mathrm{TS} \tag{1}\]
де\(\mathrm{F}\) вільна енергія даної системи,\(\mathrm{H}\) - тепловміст або ентальпія, а TS - ентропія, або розлад, термін. Якщо реакція відбувається при температурі\(T\), ми знаходимо зміну,\(\mathrm{F}(\Delta \mathrm{F})\) пов'язану зі зміною\(\mathrm{H}(\Delta \mathrm{H})\), вмістом тепла, а можливо, також зміною TS\((T \Delta S)\). Такий випадок, коли дефекти утворюються в ідеальному твердому тілі: Розподіл енергії в твердому тілі (Максвелл-Больцман) говорить про те, що ряд окремих атомів може набувати достатню кількість теплової енергії для зміщення з місця рівноважної решітки в інтерстиціальне положення. Цей процес формування точкових дефектів вимагає енергії і призводить до деформації решітки, що становить, як обговорювалося раніше, збільшення теплоємності системи (\(\Delta H\)є позитивним і лінійно збільшується з кількістю утворених дефектів). Відхід від досконалості генерацією дефектів призводить до розладу (\(\Delta S\)є позитивним). Величина породженого розладу (\(\Delta S\)) дуже велика під час початкового кроку від досконалості до легкого безладдя, але збільшення розладу (з заданою кількістю породжених дефектів) зменшується у міру збільшення загального розладу.
Відповідно термін швидко\(T \Delta S\) падає на початку, а потім розплющується. Чистий результат (рис. 1), вільна енергія, виявляє мінімум для певної кількості дефектів

твердий [щільність дефекту рівноваги = f (температура)];\(F_{\text{minimum}}\) припускає також, що перехід від досконалості до рівноважної дефектної структури спонтанний: він відбувається природним шляхом!
У той час як детальні механізми утворення атомних вакансій в твердих тілах все ще є предметом великих досліджень, пов'язана з ними енергетика рівноваги зрозуміла: розрахунки теплової енергії атомів в решітці показують, що середня коливальна енергія атомів решітки набагато менше \(1 \mathrm{eV}\)(приблизна зміна енергії, пов'язане з утворенням вакансії, тобто найменша кількість енергії, необхідної для формування вакансії) при кімнатній температурі. Тому атом решітки придбає лише енергію\(\Delta \mathrm{H}_{\mathrm{d}}\), енергію, необхідну для формування дефекту, при виникненні великого коливання енергії. Оскільки відносна ймовірність того, що атом має енергію\(\Delta \mathrm{H}_d\) або більше перевищує енергію основного стану\(e^{-\Delta H_d / k T}\), є, ймовірність того, що атомний ділянку вакантний, змінюється однаково. У (молярному) кристалі, що містить\(\mathrm{N}\) атомні ділянки,\(\mathrm{n}_{\mathrm{d}}\) кількість вакантних ділянок становить, отже,
\[\mathrm{n}_{\mathrm{d}}=\mathrm{ANe}^{-\Delta \mathrm{H}_{\mathrm{d}} / \mathrm{kT}} \tag{2}\]
де
- \(\mathrm{n}_{\mathrm{d}}\)число дефектів (в рівновазі при\(\mathrm{T}\))
- \(\mathrm{N}\)загальна кількість атомних ділянок на моль
- \(\Delta \mathrm{H}_{\mathrm{d}}\)це енергія, необхідна для формування дефекту
- \(\mathrm{T}\)абсолютна температура\((\mathrm{K})\)
- \(\mathrm{k}\)є постійною Больцмана
- \(\mathrm{A}\)є постійною пропорційності
Точкові дефекти в «чистих» металевих системах
Точкові дефекти в «чистих» кристалічних металах - це дефекти атомних розмірів, такі як домішкові атоми, відсутність атома матриці і/або наявність атома матриці в неправильному місці. Деякі з цих точкових дефектів показані на рис.2. Домішковий атом, який займає нормальну ділянку решітки, називається атомом заміщення домішки, а атом домішки, знайдений в міжстиглі між атомами матриці, називається міжстиціальним атомом домішки. Чи займатиме чужорідний атом заміщення

або інтерстиціальний ділянку багато в чому залежить від розміру атома щодо розмірів ділянки. Малі атоми зазвичай є інтерстиціальними домішками, тоді як більші атоми, як правило, є заміщеними домішками.
Вакансія - це атомний ділянку, нормально зайнятий в ідеальному кристалі, з якого відсутній атом. Часто термін «вакансія» використовується для позначення так званого дефекту Шотткі, який утворюється при виході атома або іона з нормального місця решітки і репозиціонує себе в місці решітки на поверхні кристала. Це може бути результатом атомної перестановки в існуючому кристалі при високій температурі, коли рухливість атомів висока через підвищені теплові коливання. Вакансія може також виникати в процесі кристалізації в результаті локальних збурень під час зростання нових атомних площин на поверхні кристалів. Вакансії - це точкові дефекти розміру, майже рівного розміру вихідного (зайнятого) ділянки; енергія формування вакансії відносно низька - зазвичай менше 1 еВ.
Кількість вакансій при рівновазі при кожній температурі в кристалі можна визначити з екв. (2), в якому\(\Delta \mathrm{H}_{\mathrm{d}}\) є енергія, необхідна для того, щоб взяти атом з регулярного ділянки кристала і розмістити його на поверхні для дефекту типу Шотткі. При нагріванні твердого тіла встановлюється нова більш висока рівноважна концентрація вакансій, як правило, спочатку на кристалічних поверхнях, а потім поблизу дислокацій і кордонів зерен, які забезпечують ділянки для атомів, які залишили свою нормальну ділянку решітки. Вакансії поступово поширюються по всьому кристалу (з поверхонь в основну масу). При охолодженні концентрація вакансій знижується за рахунок «дифузії вакансій» до меж зерен або дислокацій, які виступають в ролі стоків. В обох випадках нова рівноважна концентрація вакансії встановлюється тільки через кінцевий проміжок часу. Швидкість переміщення вакансій з точки в точку в решітці зменшується експоненціально зі зниженням температури. Таким чином, при дуже швидкому охолодженні (гасінні) від високої температури близько температури плавлення більшість вакансій не встигають розсіюватися на раковини і, як кажуть, «заморожені в». Це дає значно більшу («нерівноважну») концентрацію вакансій у загартованих зразках, ніж зазначена значенням теплової рівноваги.
Концентрація вільних ділянок решітки в чистих матеріалах дуже мала при низьких температурах - приблизно по одній вакансії кожного\(10^8\) атома ділянки - і збільшується з підвищенням температури приблизно до однієї вакансії на кожній\(10^3\) ділянці при температурі плавлення. Вакансії важливі, оскільки вони контролюють швидкість дифузії матричного (або заміщення) атомів - тобто атоми здатні переміщатися в кристалічному твердому тілі насамперед через наявність вакансій. (Механізм, за допомогою якого вони рухаються, такий же, як і пов'язаний з переміщенням автомобіля на заповненій стоянці до виходу). Це схематично показано на рис.3. Самостійні інтерстиції, як правило, не зустрічаються в тісно упакованих
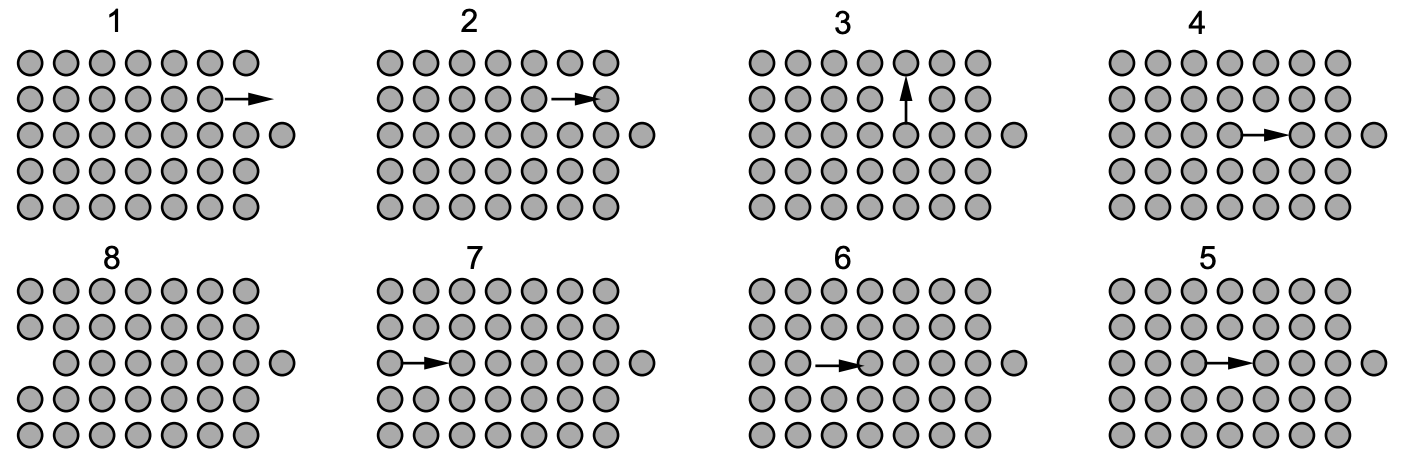
металеві системи, але можуть бути введені опроміненням. Наприклад, високоенергетичні нейтрони від атомного поділу можуть вибити атоми металів зі своїх регулярних ділянок в інтерстиціальні ділянки, створюючи вакансійно-інтерстиціальні пари.
Точкові дефекти іонних твердих тіл
Точкові дефекти в іонних структурах відрізняються від виявлених в чистих елементах через вимогу нейтральності заряду. Наприклад, у чистому моновалентному іонному матеріалі катіонна вакансія повинна бути пов'язана з ним або катіонним інтерстиціалом, або аніонною вакансією для підтримки нейтральності заряду. Аналогічні вимоги пред'являються і до аніонних вакансій. Дефект пари вакансій (міграція катіона і аніона на поверхню) зазвичай називають недосконалістю Шотткі, а дефект вакансії-інтерстиціальної пари називають недосконалістю Френкеля (аніон або катіон покинув своє положення решітки, яке стає вакансією, і перемістилося в міжтканинну позицію). Ці два види недосконалостей показані на рис. 4. Самоінтерстиціальні набагато частіше зустрічаються в іонних структурах, ніж у чистих елементах, оскільки багато іонних сполук мають відносно великі інтерстиціальні сайти. Тобто, часто є інтерстиціальні сайти в одиничній клітині, які мають майже

таке ж оточення, що і звичайні атомні сайти. (Наприклад, в BeO атоми Be заповнюють лише половину наявних чотиригранних ділянок, залишаючи чотири можливі катіонні інтерстиціальні ділянки на одиницю клітини. Таким чином, атом Be може перейти від регулярного місця решітки до майже еквівалентного інтерстиціального сайту з невеликим спотворенням решітки.)
Іноземні атоми в іонних кристалах створюють дефекти, які також повинні підтримувати нейтральність заряду. Наприклад, в NaCl одновалентний катіон, такий як літій, може просто замінити один з іонів натрію як заміщаючу домішку. Але двовалентний катіон, такий як кальцій, що замінює іон натрію, повинен супроводжуватися або вакансією катіону, або аніонним інтерстиціалом, якщо потрібно підтримувати нейтральність заряду. Відповідно, одновалентні домішкові катіони в двовалентній структурі (наприклад, Na в MgO) повинні супроводжуватися відповідною кількістю катіонних інтерстиціалів або аніонних вакансій.
Точкові дефекти в ковалентно зв'язаних твердих тілах
Замісні домішки в ковалентно зв'язаних матеріалах можуть створити унікальну недосконалість електронної структури, якщо атом домішки знаходиться з групи в періодичній таблиці, відмінної від атомів матриці. Наприклад, ви вже розглядали елементи групи V та III групи в матриці IV групи, такі як As або B у Si.
Коли чужорідні атоми включені в кристалічну структуру, будь то в заміщувальних або інтерстиціальних ділянках, ми говоримо, що отримана фаза є твердим розчином матричного матеріалу (розчинника) та чужорідних атомів (розчинника). Термін «твердий розчин», однак, не обмежується низьким вмістом розчинених речовин у легованих напівпровідникових системах; існує багато твердих розчинів, таких як металеві сплави, які містять широкий діапазон складу.
ДЕФЕКТИ ЛІНІЇ
Лінійні дефекти, або дислокації, у кристалічних твердих тілах - це дефекти, які спричиняють спотворення решітки з центром навколо лінії. Дислокація - це просто край зайвої вставленої дробової площини атомів (рис.5). Зазвичай символ\(\perp\) використовується для представлення позитивного

дислокація (позадробова площина) і\(\top\) використовується для представлення негативного вивиху (відсутня дробова площина).
Важливість дислокацій легко демонструється при деформації кристалічних матеріалів. Площина, в якій через решітку рухається дислокація, називається площиною ковзання. При прикладеному напруженні зсуву дислокація рухається, атомний ряд за атомним рядом, і одна частина кристала зміщується щодо іншої. Коли дислокація пройшла крізь кристал, частина кристала над площиною ковзання змістилася на одну атомну відстань щодо ділянки нижче площини ковзання. Іншими словами, рух дислокації змусило кристал змінити свою форму - постійно деформуватися (рис.6).

Зверніть увагу: по обидва боки дислокації кристалічна решітка по суті ідеальна, але в безпосередній близькості від дислокації решітка сильно спотворюється. Для позитивного дислокації краю наявність додаткової половини площини призводить до стиснення атомів над площиною ковзання, тоді як ті, що знаходяться нижче площини ковзання, ставляться в напругу. Отже, крайовий вивих матиме навколо нього поле напруги, яке стискає над площиною ковзання і розтягує нижче площини ковзання.
Пластична деформація ковзанням:
Коли монокристали металу (або напівпровідника) витягуються в напрузі, вони почнуть пластично деформуватися (подовжуватися) при відносно низьких рівнях напружень, а «блоки» кристалів ковзають один над одним через рух дислокації. Одночасно на їх поверхні з'являються так звані лінії ковзання. Встановлено, що деформація ковзанням найлегше відбувається на площині з високою атомною щільністю і з великим міжплощинним інтервалом, тоді як напрямок ковзання у всіх випадках є атомно «тісно упакованим напрямком». Тому для структур FCC ми спостерігаємо як первинну систему ковзання {111} площин у напрямку, тоді як у структурах BCC первинне ковзання відбувається на площині {110} у напрямках. (Слід зазначити, що альтернативним механізмом деформації є «деформаційне побратимство», в даний час не слід розглядати.)
Вивих Підйом:
Підйом - це назва, що дається руху дислокацій, коли зайва «половина» площини подовжується далі в кристал або частково виводиться з нього. Зрозуміло, що процес підйому - це не рух площини, а скоріше її зростання або скорочення в результаті приєднання атомів або «вакансій» відповідно з середовища дислокації (рис.7).
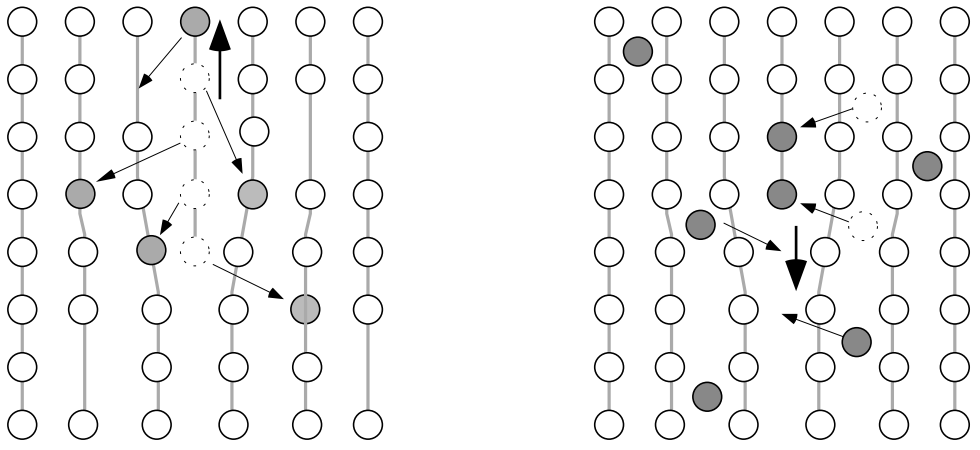
Множення вивихів:
Оскільки під час ковзання кожен вивих виходить з матриці, макроскопічна деформація не могла відбутися з огляду на нормальні щільності дислокації в діапазоні\(10^6-10^8 / \mathrm{cm}^3\). Дослідження деформованих кристалів свідчить про те, що при деформації відбувається розмноження вивихів. Хоча існує безліч механізмів множення, найбільш широко вивченим є джерело Frank-Read (не обговорюватися детально).
Взаємодія вивихів:
Відносну легкість, з якою переміщаються дислокації по твердій матриці, можна віднести до серйозних зміщень атомів в ядрі дислокацій. Якщо ці місцеві напруги зменшуються, рухливість вивихів - і, отже, легкість ковзання - знижується. Встановлено, що домішки поблизу дислокаційних сердечників мають тенденцію знижувати енергію локального спотворення дислокацій і таким чином стабілізувати систему проти ковзання. У багатьох системах навмисно додають домішки (наприклад, твердіння твердим розчином) для підвищення міцності матеріалів. Аналогічно мікроопади, як правило, перешкоджають руху дислокації (наприклад, затвердіння опадів).
МІЖФАЗНІ НЕДОСКОНАЛОСТІ
Кілька різних типів міжфазних або плоских недосконалостей у твердих тілах можна згрупувати в наступні категорії:
- Інтерфейси між твердими речовинами і газами, які називаються вільними поверхнями;
- Інтерфейси між регіонами, де відбувається зміна електронної структури, але не змінюється періодичність розташування атомів, відома як межі домену;
- Інтерфейси між двома кристалами або зернами однієї фази, де є різниця орієнтації в розташуванні атомів через інтерфейс; ці інтерфейси називаються кордонами зерен;
- Інтерфейси між різними фазами, звані фазовими межами, де, як правило, відбувається зміна хімічного складу та розташування атомів через інтерфейс.
Межі зерен властиві кристалічним твердим тілам, тоді як вільні поверхні, межі доменів та межі фаз знаходяться як у кристалічних, так і в аморфних твердих тілах.
Вільні поверхні
Через їх кінцевих розмірів всі тверді матеріали мають вільні поверхні. Розташування атомів на вільній поверхні дещо відрізняється від внутрішньої структури, оскільки поверхневі атоми не мають сусідніх атомів з одного боку. Зазвичай атоми біля поверхні мають однакову кристалічну структуру, але дещо більший параметр решітки, ніж внутрішні атоми.
Мабуть, найважливішим аспектом вільних поверхонь є поверхнева енергія,\((\gamma)\) пов'язана з поверхнями будь-якого твердого тіла. Джерело цієї поверхневої енергії можна побачити, розглядаючи оточення атомів на поверхні та всередині твердого тіла. Щоб вивести атом з нутрощів на поверхню, ми повинні або розірвати, або спотворити якісь зв'язки - тим самим збільшуючи енергію. Поверхнева енергія визначається як збільшення енергії на одиницю площі нової поверхні, що утворюється. У кристалічних твердих тілах поверхнева енергія залежить від кристалографічної орієнтації поверхні - ті поверхні, які є площинами найбільш щільної атомної упаковки, також є площинами найнижчої поверхневої енергії. Це пов'язано з тим, що атоми на цих поверхнях мають менше своїх зв'язків, порушених або, що еквівалентно, мають більшу кількість найближчих сусідів у площині поверхні. Типові значення поверхневих енергій твердих тіл варіюються від приблизно\(10^{-1}\) до\(1 \mathrm{~J} / \mathrm{m}^2\). Як правило, чим сильніше зв'язок у кристалі, тим вища поверхнева енергія.
Поверхневі енергії можуть бути зменшені адсорбцією чужорідних атомів або молекул з навколишньої атмосфери. Наприклад, у слюди поверхнева енергія свіжорозщепленого матеріалу в вакуумі набагато вище поверхневої енергії тієї ж поверхні, розщепленої в повітрі. У цьому випадку кисень адсорбується з повітря, щоб частково задовольнити зламані зв'язки на поверхні. Адсорбція домішкових атомів робить практично неможливим підтримку атомно чистих поверхонь. В результаті такі властивості поверхні, як електронна емісія, швидкість випаровування і швидкість хімічних реакцій, надзвичайно залежать від наявності будь-яких адсорбованих домішок. Ці властивості будуть відрізнятися, якщо вимірювання проводяться в умовах, що дають різну поверхневу адсорбцію.
Межі зерен
Межі зерен відокремлюють області різної кристалографічної спрямованості. Найпростіша форма кордону зерна - це інтерфейс, що складається з паралельного масиву ребер дислокацій. Цей конкретний тип кордону називається межею нахилу, оскільки дезорієнтація у вигляді простого нахилу навколо осі, паралельного дислокаціям. Межі нахилу називаються кордонами з низьким кутом, оскільки кут неправильної орієнтації, як правило, менше\(10^{\circ}\).
Коли межа зерна має дезорієнтацію більше\(10^{\circ}\) або\(15^{\circ}\), вже не практично думати про межу як складену з дислокацій, оскільки інтервал дислокацій був би настільки малим, що вони втратять свою індивідуальну ідентичність. Межа зерен являє собою область шириною в кілька атомних діаметрів, де відбувається перехід в атомній періодичності між сусідніми кристалами або зернами.
Межі зерен мають міжфазну енергію через порушення атомної періодичності в безпосередній близькості від кордону і розбитих зв'язків, які існують через межі розділу. Міжфазна енергія кордонів зерен, як правило, менше, ніж у вільної поверхні, оскільки атоми в межі зерен оточені з усіх боків іншими атомами і мають лише кілька розірваних або спотворених зв'язків.
Тверді тіла з межами зерен відносять до полікристалічних, так як структура складається з безлічі кристалів - кожен з різною кристалографічної орієнтацією. У випадку заліза гранична структура зерна може бути виявлена шляхом переважної хімічної атаки (травлення) на межі зерен, тоді як зерниста структура в поліетилені виявляється за допомогою поляризованого світла. Структура зерна зазвичай визначається шляхом надання середнього діаметра зерна або за допомогою схеми, розробленої Американським товариством випробувань та матеріалів (ASTM). У процедурі ASTM розмір зерна визначається «числом розміру зерна» (n), де
\[N=2^{n-1}\]
з\(\mathrm{N}\) рівним кількості зерен на квадратний дюйм, коли зразок розглядається при 100-кратному збільшенні. Наприклад, при збільшенні, матеріал з\(X=100\) зернистим числом 8 покаже 128 зерен на дюйм\({ }^2\) - цей матеріал по суті має (при\(X=1\))\(1.28 \times 10^6\) зернистості на квадратний дюйм. Якщо зерна приблизно квадратні в поперечному перерізі, це відповідає середньому розмірності зерна\(8.8 \times 10^{-4} \mathrm{in}^*\).
У полікристалічних зразках окремі зерна зазвичай мають випадкову кристалографічну орієнтацію відносно один одного, а зернова структура називається випадково орієнтованою. Однак у деяких випадках зерна мають однакову орієнтацію в межах декількох градусів. У цьому випадку матеріал, як кажуть, має кращу орієнтацію або текстуру.
Межі фаз
Фаза визначається як однорідна, фізично виразна і механічно відокремлювана частина матеріалу із заданим хімічним складом і структурою. Фази можуть бути заміщеними або інтерстиціальними твердими розчинами, впорядкованими сплавами або сполуками, аморфними речовинами або навіть чистими елементами; кристалічна фаза в твердому стані може бути або полікристалічною, або існувати у вигляді монокристала.
Тверді речовини, що складаються з більш ніж одного елемента, можуть - і часто роблять - складатися з ряду фаз. Наприклад, дриль стоматолога, щось до болю знайоме всім нам, складається з суміші дрібних монокристалів карбіду вольфраму, оточених матрицею кобальту. Тут кобальт утворює безперервну фазу. Поліфазні матеріали, такі як дриль стоматолога, зазвичай називають композитними матеріалами. Композитні матеріали мають велике значення в інженерному світі, оскільки вони мають безліч привабливих властивостей, які відрізняють їх від однофазних матеріалів. Наприклад, дриль стоматолога має хороші абразивні характеристики (за рахунок твердих твердих частинок) і хорошу в'язкість і ударостійкість (за рахунок суцільної кобальтової матриці). Ні карбід вольфраму, ні кобальт не мають як стійкості до стирання, так і ударостійкості, але правильне поєднання двох фаз дає композитну структуру з бажаними властивостями.
- *
-
ASTM ще не випустила специфікації в одиницях SI!
Характер інтерфейсу, що розділяє різні фази, дуже схожий на межу зерен. Межі між двома фазами різного хімічного складу та різною кристалічною структурою схожі на межі зерен, тоді як межі між різними фазами зі схожими кристалічними структурами та кристалографічними орієнтаціями можуть бути аналогічними низькокутовим межам зерен як за енергією, так і структурою.
Поняття твердого тіла, що складається з безперервної фази і розривної фази (або фаз), призводить до простої класифікації різних видів композиційних матеріалів. У таблиці 1 наведено цю класифікацію, яка заснована на структурі (аморфної або кристалічної) безперервної і переривчастої фаз.
ТАБЛИЦЯ 1
Класифікація композитних або багатофазних матеріалів
\ (\ begin {масив} {lll}
\ text {Неперервна фаза} &\ begin {масив}
{l}\ text {розривна фаза}
\\ text {(або фази)}\ кінець {масив} &
\ текст {Приклади}\\ hline\ текст {кристалічний} &\ begin { масив} {l}
\ text {Всі металеві системи, такі як литі}\
\ text {залізо, сталь, м'який припій тощо; більшість}\
\ text {природні гірські породи, такі як граніт і}\
\ text {мармур.}
\ end {масив}\\
\ text {Кристалічний} &\\ текст {Аморфний} &\ текст {Немає практичного значення.}\\\ text {Аморфний} &
\ text {Кристалічний} &\ begin {масив} {l}
\ text {Більшість рукотворних керамік, таких}\\
\ text {як будівельна цегла та електричний}\
\ текст {ізолятор фарфор, бетон,}\
\ text {частково кристалічні полімери,}\
\ text {деякі полімерно-кристалічні частинки}\
\ текст {композити.}
\ end {масив}\\
\ text {Amorphous} &\ text {аморфний} &\ begin {масив} {l}
\ text {Скловолокно, асфальт, дерево,}\
\ text {гідратований цемент, інші гелі.}
\ end {масив}
\ end {масив}\)