12.3: Закони про ставки
- Page ID
- 22572
- Поясніть форму і функцію закону ставки
- Використовуйте закони швидкості для розрахунку швидкості реакції
- Використовуйте дані про швидкість та концентрацію для визначення порядку реакції та отримання законів швидкості
Як описано в попередньому модулі, на швидкість реакції впливають концентрації реагентів. Закони швидкості або рівняння швидкості - це математичні вирази, які описують взаємозв'язок між швидкістю хімічної реакції і концентрацією її реагентів. Взагалі закон ставки (або закон диференціальної ставки, як його іноді називають) приймає таку форму:
\[\ce{rate}=k[A]^m[B]^n[C]^p… \nonumber \]
в яких [A], [B], і [C] представляють молярні концентрації реагентів, а k - константа швидкості, специфічна для конкретної реакції при певній температурі. Показники m, n та p зазвичай є додатними цілими числами (хоча можливо, що вони можуть бути дробами або від'ємними числами). Константа швидкості k та показники m, n та p повинні бути визначені експериментально, спостерігаючи за тим, як змінюється швидкість реакції при зміні концентрацій реагентів. Постійна швидкості k не залежить від концентрації A, B або C, але вона змінюється залежно від температури та площі поверхні.
Показники в законі швидкості описують вплив концентрацій реагентів на швидкість реакції та визначають порядок реакції. Розглянемо реакцію, для якої нормовим законом є:
\[\ce{rate}=k[A]^m[B]^n \nonumber \]
Якщо показник m дорівнює 1, реакція першого порядку по відношенню до A. Якщо m дорівнює 2, реакція другого порядку по відношенню до А. Якщо n дорівнює 1, реакція першого порядку в B. Якщо n дорівнює 2, реакція другого порядку в B. Якщо m або n дорівнює нулю, реакція дорівнює нулю порядку в А або В відповідно, і на швидкість реакції не впливає концентрація цього реагенту. Загальний порядок реакції - це сума порядків щодо кожного реагенту. Якщо m = 1 і n = 1, загальний порядок реакції другого порядку (m + n = 1 + 1 = 2).
Закон ставки:
\[\ce{rate}=k[\ce{H2O2}] \nonumber \]
описує реакцію, яка є першим порядком перекису водню і першим порядком в цілому. Закон ставки:
\[\ce{rate}=k[\ce{C4H6}]^2 \nonumber \]
описує реакцію другого порядку в C 4 H 6 і другого порядку в цілому. Закон ставки:
\[\ce{rate}=k[\ce{H+}][\ce{OH-}] \nonumber \]
описує реакцію першого порядку в H +, першого порядку в OH − та другого порядку загалом.
Експеримент показує, що реакція діоксиду азоту з чадним газом:
\[\ce{NO2}(g)+\ce{CO}(g)⟶\ce{NO}(g)+\ce{CO2}(g) \nonumber \]
це другий порядок в NO 2 і нульовий порядок в СО при 100 °С Який закон швидкості для реакції?
Рішення
Реакція буде мати вигляд:
\[\ce{rate}=k[\ce{NO2}]^m[\ce{CO}]^n \nonumber \]
Реакція другого порядку в NO 2; таким чином m = 2. Реакція дорівнює нульовому порядку в СО; таким чином n = 0. Закон ставки це:
\[\ce{rate}=k[\ce{NO2}]^2[\ce{CO}]^0=k[\ce{NO2}]^2 \nonumber \]
Пам'ятайте, що число, підняте до нульової потужності, дорівнює 1, таким чином [СО] 0 = 1, саме тому ми можемо просто скинути концентрацію СО з рівняння швидкості: швидкість реакції виключно залежить від концентрації NO 2. Коли ми розглянемо механізми швидкості пізніше в цьому розділі, ми пояснимо, як концентрація реагенту не може впливати на реакцію, незважаючи на участь у реакції.
Закон швидкості для реакції:
\[\ce{H2}(g)+\ce{2NO}(g)⟶\ce{N2O}(g)+\ce{H2O}(g) \nonumber \]
експериментально визначено як швидкість = k [NO] 2 [H 2]. Які порядки щодо кожного реагенту, і який загальний порядок реакції?
- Відповідь
-
- порядок в НІ = 2;
- порядок в Н 2 = 1;
- загальний порядок = 3
У реакції переетерифікації тригліцерид реагує зі спиртом з утворенням ефіру та гліцерину. Багато студентів дізнаються про реакцію між метанолом (CH 3 OH) та етилацетатом (CH 3 CH 2 OCOCH 3) як реакцію зразка перед вивченням хімічних реакцій, які виробляють біодизель:
\[\ce{CH3OH + CH3CH2OCOCH3 ⟶ CH3OCOCH3 + CH3CH2OH} \nonumber \]
Закон норми для реакції між метанолом і етилацетатом, за певних умов, експериментально визначається як:
\[\ce{rate}=k[\ce{CH3OH}] \nonumber \]
Який порядок реакції щодо метанолу та етилацетату, і який загальний порядок реакції?
- Відповідь
-
- порядок в СН 3 ОН = 1;
- порядок в СН 3 СН 2 ОКОЧ 3 = 0;
- загальне замовлення = 1
Іноді корисно використовувати більш явний алгебраїчний метод, який часто називають методом початкових ставок, для визначення порядків в законі ставок. Для використання цього методу ми вибираємо два набори даних швидкості, які відрізняються концентрацією лише одного реагенту та встановимо співвідношення двох швидкостей та двох законів швидкості. Після скасування рівних членів нам залишається рівняння, яке містить лише одне невідоме - коефіцієнт концентрації, який змінюється. Потім вирішимо це рівняння для коефіцієнта.
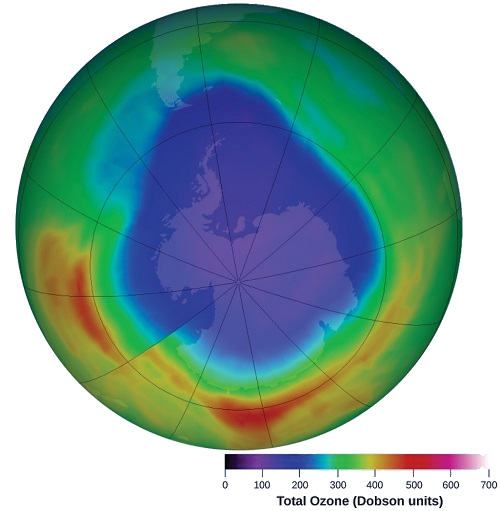
Озон у верхній атмосфері виснажується, коли він реагує з оксидами азоту. Швидкість реакцій оксидів азоту з озоном є важливими факторами при вирішенні того, наскільки значними є ці реакції при утворенні озонової діри над Антарктидою (рис.\(\PageIndex{1}\)). Однією з таких реакцій є поєднання оксиду азоту, NO, з озоном, O 3:
\[\ce{NO}(g)+\ce{O3}(g)⟶\ce{NO2}(g)+\ce{O2}(g) \nonumber \]
Ця реакція була вивчена в лабораторії, і наступні дані швидкості були визначені при 25° C.
| Пробна версія | \([\ce{NO}]\)(моль/л) | \([\ce{O3}]\)(моль/л) | \(\dfrac{Δ[\ce{NO2}]}{Δt}\:\mathrm{(mol\:L^{−1}\:s^{−1})}\) |
|---|---|---|---|
| 1 | \ ([\ ce {NO}]\) (моль/л)» style="вирівнювання тексту: центр; вертикальне вирівнювання: середина; "> 1.00 × 10 −6 | \ ([\ ce {O3}]\) (моль/л)» style="вирівнювання тексту: центр; вертикальне вирівнювання: середина; "> 3,00 × 10 −6 | \ (\ dfrac {Δ [\ ce {NO2}]} {Δt}\:\ mathrm {(mol\ :L^ {−1}\ :s^ {−1})}\)» стиль = "вирівнювання тексту: центр; вертикальне вирівнювання: середина; ">6.60 × 10 −5 |
| 2 | \ ([\ ce {NO}]\) (моль/л)» style="вирівнювання тексту: центр; вертикальне вирівнювання: середина; "> 1.00 × 10 −6 | \ ([\ ce {O3}]\) (моль/л)» style="вирівнювання тексту: центр; вертикальне вирівнювання: середина; "> 6.00 × 10 −6 | \ (\ dfrac {Δ [\ ce {NO2}]} {Δt}\:\ mathrm {(mol\ :L^ {−1}\ :s^ {−1})}\)» стиль = "вирівнювання тексту: центр; вертикальне вирівнювання: середина; ">1.32 × 10 −4 |
| 3 | \ ([\ ce {NO}]\) (моль/л)» style="вирівнювання тексту: центр; вертикальне вирівнювання: середина; "> 1.00 × 10 −6 | \ ([\ ce {O3}]\) (моль/л)» style="вирівнювання тексту: центр; вертикальне вирівнювання: середина; ">9.00 × 10 −6 | \ (\ dfrac {Δ [\ ce {NO2}]} {Δt}\:\ mathrm {(mol\ :L^ {−1}\ :s^ {−1})}\)» стиль = "вирівнювання тексту: центр; вертикальне вирівнювання: середина; ">1.98 × 10 −4 |
| 4 | \ ([\ ce {NO}]\) (моль/л)» style="вирівнювання тексту: центр; вертикальне вирівнювання: середина; "> 2,00 × 10 −6 | \ ([\ ce {O3}]\) (моль/л)» style="вирівнювання тексту: центр; вертикальне вирівнювання: середина; ">9.00 × 10 −6 | \ (\ dfrac {Δ [\ ce {NO2}]} {Δt}\:\ mathrm {(mol\ :L^ {−1}\ :s^ {−1})}\)» стиль = "вирівнювання тексту: центр; вертикальне вирівнювання: середина; ">3.96 × 10 −4 |
| 5 | \ ([\ ce {NO}]\) (моль/л)» style="вирівнювання тексту: центр; вертикальне вирівнювання: середина; "> 3.00 × 10 −6 | \ ([\ ce {O3}]\) (моль/л)» style="вирівнювання тексту: центр; вертикальне вирівнювання: середина; ">9.00 × 10 −6 | \ (\ dfrac {Δ [\ ce {NO2}]} {Δt}\:\ mathrm {(mol\ :L^ {−1}\ :s^ {−1})}\)» стиль = "вирівнювання тексту: центр; вертикальне вирівнювання: середина; ">5.94 × 10 −4 |
Визначте закон швидкості і константу швидкості для реакції при 25 °С.
Рішення
Закон про ставки матиме вигляд:
\[\ce{rate}=k[\ce{NO}]^m[\ce{O3}]^n \nonumber \]
Ми можемо визначити значення m, n та k з експериментальних даних, використовуючи наступний тричастинний процес:
- Визначте значення m з даних, в яких [NO] змінюється і [O 3] постійна. В останніх трьох експериментах [NO] змінюється, тоді як [O 3] залишається постійним. Коли [NO] подвоюється з випробувань 3 до 4, ставка подвоюється, а коли [NO] потроюється з випробувань 3 до 5, ставка також збільшується втричі. Таким чином, ставка також прямо пропорційна [НІ], а m в нормовому законі дорівнює 1.
- Визначте значення n з даних, в яких [O 3] змінюється і [NO] є постійним. У перших трьох експериментах [NO] є постійним і [O 3] змінюється. Швидкість реакції змінюється прямо пропорційно зміні в [О 3]. Коли [O 3] подвоюється від випробування 1 до 2, ставка подвоюється; коли [O 3] потроюється від випробування 1 до 3, ставка збільшується також втричі. Таким чином, ставка прямо пропорційна [О 3], а n дорівнює 1.Закон ставки таким чином:
\[\ce{rate}=k[\ce{NO}]^1[\ce{O3}]^1=k[\ce{NO}][\ce{O3}] \nonumber \]
- Визначте значення k з одного набору концентрацій і відповідної норми.
\ [\ почати {вирівнювати*}
k&=\ математика {\ dfrac {швидкість} {[НІ] [O_3]}}\\
&=\ математика {\ dfrac {6.60×10^ {−5}\ скасувати {моль\: L^ {−1}}\ :s^ {−1}} {(1.00×10^ {−6}\ скасувати\: L^ {−1}}) (3.00×10^ {−6}\ :моль\ :L^ {−1})}}\\
&=\ mathrm {2.20×10^7\ :L\ :mol^ {−1}\ :s^ {−1}}
\ кінець {вирівнювати*}\ nonumber\]Велике значення k говорить нам, що це швидка реакція, яка може зіграти важливу роль у руйнуванні озонового шару, якщо [NO] достатньо великий.
Ацетальдегід розкладається при нагріванні з отриманням метану і чадного газу відповідно до рівняння:
\[\ce{CH3CHO}(g)⟶\ce{CH4}(g)+\ce{CO}(g) \nonumber \]
Визначте закон швидкості і константу швидкості для реакції за наступними експериментальними даними:
| Пробна версія | \([\ce{CH3CHO}]\)(моль/л) | \(−\dfrac{Δ[\ce{CH3CHO}]}{Δt}\mathrm{(mol\:L^{−1}\:s^{−1})}\) |
|---|---|---|
| 1 | \ ([\ ce {CH3CHO}]\) (моль/л)» style="вирівнювання тексту: центр; ">1,75 × 10 −3 | \ (−\ dfrac {Δ [\ ce {CH3CHO}]} {Δt}\ mathrm {(моль\ :L^ {−1}\ :s^ {−1})}\)» стиль = "вирівнювання тексту: центр; ">2.06 × 10 −11 |
| 2 | \ ([\ ce {CH3CHO}]\) (моль/л)» style="вирівнювання тексту: центр; "> 3,50 × 10 −3 | \ (−\ dfrac {Δ [\ ce {CH3CHO}]} {Δt}\ mathrm {(моль\ :L^ {−1}\ :s^ {−1})}\)» стиль = "вирівнювання тексту: центр; ">8.24 × 10 −11 |
| 3 | \ ([\ ce {CH3CHO}]\) (моль/л)» style="вирівнювання тексту: центр; ">7.00 × 10 −3 | \ (−\ dfrac {Δ [\ ce {CH3CHO}]} {Δt}\ mathrm {(моль\ :L^ {−1}\ :s^ {−1})}\)» стиль = "вирівнювання тексту: центр; ">3.30 × 10 |
- Відповідь
-
\(\ce{rate}=k[\ce{CH3CHO}]^2\)з k = 6,73 × 10 −6 л/моль/с
Використовуючи метод початкових швидкостей і експериментальні дані, визначають закон швидкості і значення константи швидкості для цієї реакції:
\[\ce{2NO}(g)+\ce{Cl2}(g)⟶\ce{2NOCl}(g) \nonumber \]
| Пробний | [НІ] (моль/л) | \([Cl_2]\)(моль/л) | \(−\dfrac{Δ[\ce{NO}]}{2Δt}\mathrm{(mol\:L^{−1}\:s^{−1})}\) |
|---|---|---|---|
| 1 | 0,10 | \ ([Cl_2]\) (моль/л)» style="вирівнювання тексту: центр; "> 0,10 | \ (−\ dfrac {Δ [\ ce {NO}]} {2Δt}\ mathrm {(моль\ :L^ {−1}\ :s^ {−1})}\)» стиль = "вирівнювання тексту: центр; ">0.00300 |
| 2 | 0,10 | \ ([Cl_2]\) (моль/л)» style="вирівнювання тексту: центр; "> 0,15 | \ (−\ dfrac {Δ [\ ce {NO}]} {2Δt}\ mathrm {(моль\ :L^ {−1}\ :s^ {−1})}\)» стиль = "вирівнювання тексту: центр; ">0.00450 |
| 3 | 0,15 | \ ([Cl_2]\) (моль/л)» style="вирівнювання тексту: центр; "> 0,10 | \ (−\ dfrac {Δ [\ ce {NO}]} {2Δt}\ mathrm {(моль\ :L^ {−1}\ :s^ {−1})}\)» стиль = "вирівнювання тексту: центр; ">0.00675 |
Рішення
Нормативний закон для цієї реакції матиме вигляд:
\[\ce{rate}=k[\ce{NO}]^m[\ce{Cl2}]^n \nonumber \]
Як і в прикладі\(\PageIndex{2}\), ми можемо підійти до цієї задачі поетапно, визначаючи значення m і n з експериментальних даних і потім використовуючи ці значення для визначення значення k. Однак у цьому прикладі ми будемо використовувати інший підхід для визначення значень m і n:
Визначте значення m з даних, в яких [NO] змінюється і [Cl 2] постійна. Ми можемо написати співвідношення з індексами x та y, щоб вказати дані двох різних випробувань:
\[\dfrac{\ce{rate}_x}{\ce{rate}_y}=\dfrac{k[\ce{NO}]^m_x[\ce{Cl2}]^n_x}{k[\ce{NO}]^m_y[\ce{Cl2}]^n_y} \nonumber \]
Використання третього пробного і першого пробного, в якому [Cl 2] не змінюється, дає:
\[\mathrm{\dfrac{rate\: 3}{rate\: 1}}=\dfrac{0.00675}{0.00300}=\dfrac{k(0.15)^m(0.10)^n}{k(0.10)^m(0.10)^n} \nonumber \]
Після скасування еквівалентних членів в чисельнику і знаменнику нам залишається:
\[\dfrac{0.00675}{0.00300}=\dfrac{(0.15)^m}{(0.10)^m} \nonumber \]що спрощує:
\[2.25=(1.5)^m \nonumber \]
Ми можемо використовувати натуральні колоди для визначення значення показника m:
\ ln (2.25) &=м\ ln (1.5)
\ dfrac {\ ln (2.25)} {\ ln (1.5)} &= м
2&= м
\ кінець {align*}\)
Ми можемо легко підтвердити результат, оскільки:
- Визначте значення n з даних, в яких [Cl 2] змінюється і [NO] є постійною. \[\mathrm{\dfrac{rate\: 2}{rate\: 1}}=\dfrac{0.00450}{0.00300}=\dfrac{k(0.10)^m(0.15)^n}{k(0.10)^m(0.10)^n} \nonumber \]
Скасування дає:
\[\dfrac{0.0045}{0.0030}=\dfrac{(0.15)^n}{(0.10)^n} \nonumber \]
що спрощує:
\[1.5=(1.5)^n \nonumber \]
При цьому n має бути 1, а форма закону ставки дорівнює:
\[\ce{Rate}=k[\ce{NO}]^m[\ce{Cl2}]^n=k[\ce{NO}]^2[\ce{Cl2}] \nonumber \]
- Визначте числове значення постійної швидкості k з відповідними одиницями. Одиницями швидкості реакції є моль/л/с. Одиниці для k - це все, що потрібно, щоб заміщення у вираз закону швидкості надало відповідні одиниці для швидкості. У цьому прикладі одиницями концентрації є моль 3 /л 3. Одиниці для k повинні бути моль −2 л 2 /с так, щоб норма була в перерахунку на моль/л/с.
Щоб визначити значення k після розв'язання виразу закону швидкості, просто підключіть значення з першого експериментального випробування та вирішіть для k:
\ (\ почати {вирівнювати*}
\ матрм {0,00300\ :моль\ :L^ {−1}\ :s^ {−1}} &=k\ mathrm {(0,10\ :моль\ :L^ {−1}) ^2 (0.10\ :моль\ :L^ {−1}) ^1}\\
k&=\ mathrm {3.0\ :mol^ {−2}\ :L^2\ :s^ {−1}}
\ end {align*}\)
Використовуйте надані дані початкові дані швидкості, щоб вивести закон швидкості для реакції, рівняння якої дорівнює:
\[\ce{OCl-}(aq)+\ce{I-}(aq)⟶\ce{OI-}(aq)+\ce{Cl-}(aq) \nonumber \]
| Пробна версія | [CoL −] (моль/л) | [I −] (моль/л) | Початкова швидкість (моль/л/с) |
|---|---|---|---|
| 1 | 0,0040 | 0,0020 | 0,00184 |
| 2 | 0,0020 | 0,0040 | 0,00092 |
| 3 | 0,0020 | 0,0020 | 0.00046 |
Визначте вираз закону швидкості і значення константи швидкості k з відповідними одиницями для цієї реакції.
- Відповідь
-
\(\mathrm{\dfrac{rate\: 2}{rate\: 3}}=\dfrac{0.00092}{0.00046}=\dfrac{k(0.0020)^x(0.0040)^y}{k(0.0020)^x(0.0020)^y}\)
2,00 = 2,00 г
у = 1
\(\mathrm{\dfrac{rate\: 1}{rate\: 2}}=\dfrac{0.00184}{0.00092}=\dfrac{k(0.0040)^x(0.0020)^y}{k(0.0020)^x(0.0040)^y}\)
\ (\ почати {вирівнювати*}
2.00&=\ dfrac {2^x} {2^y}\\
2.00&=\ dfrac {2^x} {2^1}\\
4.00&=2^x\
x & = 2
\ end {align*}\)
Підставляючи дані концентрації з випробування 1 та розв'язуючи для k врожайності:
\ (\ почати {вирівнювати*}
\ ce {швидкість} &= k [\ ce {oCl-}] ^2 [\ ce {I-}] ^1\\
0.00184&= k (0,0040) ^2 (0,0020) ^1\\
k&=\ матхрм {5.75×10^4\ :mol^ {−2}\ :L^2}\ :L^2\ :s^ {−1}}
\ end {вирівнювати*}\)
Порядок реакції і швидкість постійних одиниць
У деяких наших прикладах порядок реакцій у законі швидкості збігається з коефіцієнтами в хімічному рівнянні для реакції. Це всього лише збіг обставин і дуже часто не так. Закони швидкості можуть проявляти дробові порядки для деяких реагентів, а негативні порядки реакцій іноді спостерігаються, коли збільшення концентрації одного реагенту викликає зниження швидкості реакції. Наведено кілька прикладів, що ілюструють ці моменти:
\ (\ ce {NO2 + CONO + СО2}\ hspace {20px}\ ce {швидкість} = k [\ ce {NO2}] ^2
\\ ce {CH3CHOCH4+ СО}\ hspace {20px}\ ce {швидкість} = k [\ ce {CH3CHO}] ^2
\\ ce {2N2O52NO2 + O2}\ hspace {20px}\ ce {швидкість} = k [\ ce {N2O5}]
\\ ce {2NO2+ F22NO2F}\ hspace {20px}\ ce {швидкість} = k [\ ce {NO2}] [\ ce {F2}]\
\ ce {2 No2Cl2No2 + Cl2}\ hspace {20px}\ ce {швидкість} = k [\ ce {No2Cl}]\)
Важливо відзначити, що закони швидкості визначаються тільки експериментом і не достовірно прогнозуються реакційною стехіометрією.
Порядки реакції також відіграють певну роль у визначенні одиниць для постійної швидкості k. У\(\PageIndex{2}\) прикладі реакції другого порядку ми знайшли одиниці для k бути\(\mathrm{L\:mol^{-1}\:s^{-1}}\), тоді як у\(\PageIndex{3}\) прикладі реакції третього порядку ми знайшли одиниці для k моль −2 L 2 /s. Якщо говорити загальніше, одиниці для константи швидкості для a реакція порядку\( (m+n)\) є\(\ce{mol}^{1−(m+n)}\ce L^{(m+n)−1}\ce s^{−1}\). Таблиця\(\PageIndex{1}\) підсумовує одиниці постійної швидкості для загальних порядків реакції.
| Порядок реакції | Одиниці k |
|---|---|
| \( (m+n)\) | \(\ce{mol}^{1−(m+n)}\ce L^{(m+n)−1}\ce s^{−1}\) |
| нуль | моль/л/с |
| перший | s −1 |
| другий | Л/моль/с |
| третій | моль −2 л 2 с −1 |
Зверніть увагу, що одиниці в таблиці також можуть бути виражені через молярність (М) замість моль/л Також можуть використовуватися одиниці часу, відмінні від другого (такі як хвилини, години, дні), в залежності від ситуації.
Резюме
Закони швидкості дають математичний опис того, як зміни кількості речовини впливають на швидкість хімічної реакції. Закони швидкості визначаються експериментально і не можуть бути передбачені реакційною стехіометрією. Порядок реакції описує, наскільки зміна кількості кожної речовини впливає на загальну швидкість, а загальний порядок реакції - це сума порядків для кожної речовини, присутньої в реакції. Реакційні замовлення, як правило, першого порядку, другого порядку або нульового порядку, але можливі дробові і навіть негативні замовлення.
Глосарій
- метод початкових ставок
- використання більш явного алгебраїчного методу для визначення порядків в нормовому законі
- загальний порядок реакції
- сума порядків реакції для кожної речовини, представленої в нормовому законі
- постійна швидкість (к)
- константа пропорційності у взаємозв'язку між швидкістю реакції та концентраціями реагентів
- ставка закон
- (також рівняння швидкості) математичне рівняння, що показує залежність швидкості реакції від постійної швидкості і концентрації одного або декількох реагентів
- реакція порядок
- значення показника в нормовому законі, виражене у вигляді порядкового числа (наприклад, нульовий порядок для 0, перший порядок для 1, другий порядок для 2 і так далі)
