16.7: Хронологія розробки акумуляторів
- Page ID
- 19198
Хоча розробка практичних акумуляторів значною мірою паралелювала розширення електричних технологій приблизно з середини 19 століття, зараз вважається, що дуже примітивний вид акумулятора, мабуть, використовувався більше 2000 років тому. Коротка популярність автомобілів з електричним приводом у 1920-х роках заохочувала розвиток акумуляторних батарей. Широке застосування портативних «персональних» електричних пристроїв дозволило зберегти пошуки кращих акумуляторів дуже живим.
|
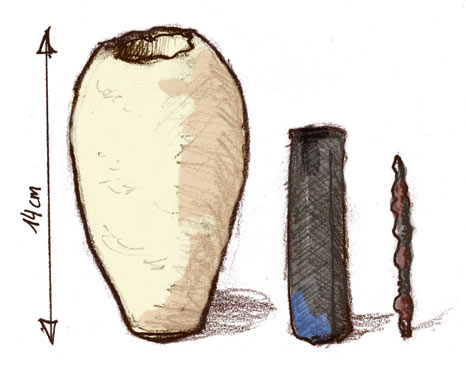
«Багдадська батарея» - 1000 до н.е.?
Малюнок з трьох частин. (CC-BY-SA 2.5; Іронія) |
Фаянсові банки, що містять залізний стрижень, оточений мідним циліндром, були виявлені поблизу Багдада в 1938 році. Вважається, що вони були використані парфянською цивілізацією, яка окупувала регіон близько 2000 років тому як джерело електроенергії для пластини золота на срібло. |
|
Аллесандро Вольта 1782
|
Його «Вольтайська купа», стопка цинкових і срібних дисків, розділених мокрою тканиною, що містить сіль або слабкий розчин кислоти, була першою батареєю, відомою західній цивілізації. |
| Сер Хамфрі Дейві 1813 | Деві будує 2000-плитний акумулятор, який займає 889 квадратних футів у підвалі Британського Королівського товариства. Його більш ранні батареї забезпечували харчування для першої публічної демонстрації електричного освітлення (вуглецевої дуги). |
| Майкл Фарадей, 1830-і | Фарадей відкрив основи гальванічних елементів та електролізу, які ставлять електрохімію на тверду наукову основу. |
|
1836 - клітина Деніелла (також відома як вороняча лапка або гравітаційна клітина.)
|
Джон Деніелл (англійський хімік і метеоролог) розробив першу сучасну камеру зберігання, засновану на принципах Фарадея. Він складається з великої скляної банки з мідним зіркоподібним електродом у нижній частині та підвішеного вгорі цинкового електрода у формі «гусячої лапки». Дно банки заповнили концентрованим розчином мідного купоросу. Поверх цього наливали розведену сірчану кислоту, нижня щільність якої тримала її зверху. Це була перша практична батарея, яка знайшла широке застосування для живлення телеграфів та систем залізничної сигналізації та домашніх дверних дзвінків. |
|
1839 - Вільям Гроув (валлійська)
|
Гроув був найвідомішим у 19 столітті своєю «азотною кислотною батареєю», яка набула широкого використання в ранній телеграфії.
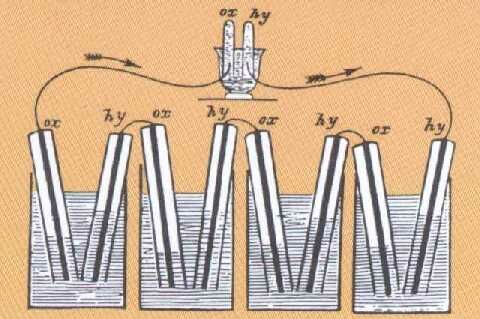
Однак зараз він найвідоміший своєю «газовольтною батареєю», в якій виявлений «зворотний електроліз»: рекомбінація H 2 і O 2 після електролізу води на платинових електродах. Це була перша демонстрація того, що ми зараз знаємо як воднево-кисневий паливний елемент (див. Нижче). |
|
1859 - Гастон Планте (французька)
|
Винаходить першу свинцево-кислотну накопичувальну камеру, яка складалася з двох листів свинцю, розділених гумовим листом, згорнутих в спіраль і занурених в розведену сірчану кислоту. |
|
1866 - Жорж Лекланше (французька)
|
До 1868 року в телеграфних системах використовувалося двадцять тисяч осередків Лекланше. Оригінальні клітини Лекланше були побудовані в пористих горщиках, які були важкими і схильні до поломки. Протягом двадцяти років інші винахідники модифікували конструкцію в те, що ми зараз знаємо як «сухі клітини», які стали широко використовуватися в перших ліхтарях (1909) та в радіостанціях з батарейками 1920-х років. |
|
1881 - Фор та інші
|
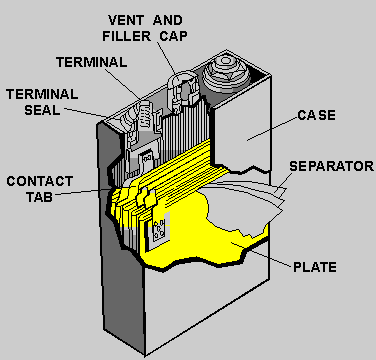
Розробка першої практичної свинцево-кислотної накопичувальної клітини. Основним поліпшенням дизайну Planté стало додавання пасти PbSO 4 до позитивної пластини. |
|
1905 Нікель-залізна клітина
|
Едісон, який був настільки ж хіміком, як всебічним винахідником, вважав, що свинець у клітині типу Планте робить їх занадто важкими, і що наявність кислоти в контакті з будь-яким металом за своєю суттю є поганою ідеєю. Після довгих експериментів він розробив вдалу лужну батарею. Клітина Едісона використовує анод заліза, катод оксиду нікелю та електроліт KOH. Ця клітина надзвичайно міцна і все ще використовується в певних промислових додатках, але вона ніколи не змогла витіснити свинцево-кислотну клітинку, як сподівався Едісон. |
| 1950-х | Подібна комірка, яка використовує нікелевий анод замість заліза, була першою акумуляторною коміркою, яка була досить маленькою для використання в портативних споживчих пристроях. Головний його недолік полягає в тому, що він руйнується повним розрядом. |
| 1949 - Лужні сухі клітини - Лью Уррі (Eveready Battery Co.) |
Перший комерційний лужний сухий елемент. Ці замінники KOH для корозійного NH 4 Cl, що використовуються в старих сухих камерах і тривають в 5-8 разів довше. |
| 1947 - Клітина Меркурія (Рубен і Меллорі, 1950-х) |
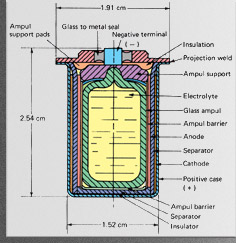
Це була одна з перших клітин типу «кнопки», яка широко використовувалася в камерах та слухових апаратах. Сталість виходу 1.34 v зробила їх популярними для використання в чутливих інструментах і кардіостимуляторах серця. Чиста реакція клітин Zn (s) + HgO (и) → ZnO (s) + Hg (л) Більшість країн заборонили продажі цих клітин, щоб зменшити забруднення навколишнього середовища ртуттю. |
|
Нікель-кадмієві (NiCaD) клітини
|
Клітка NiCad швидко стає однією з найпопулярніших акумуляторних батарей для невеликих споживчих пристроїв. Вони можуть подавати високий струм і пройти сотні циклів заряду/розряду. Оскільки кадмій є токсином навколишнього середовища, їх використання не рекомендується. |
| 1959 - Паливний елемент - Френсіс Бекон (Великобританія) | Перший практичний паливний елемент був розроблений британським інженером Френсісом Беконом (1904-1992). У цій воднево-кисневій осередку використовувався лужний електроліт і недорогі нікелеві електроди. |
|
Кінець 1960-х - нікель-металгідридні клітини
|
Гідридний іон Н - був би ідеальним катодним матеріалом, за винятком того факту, що його продукт окислення Н 2 є газом. Відкриття того, що певні сполуки, такі як LiNi 5 та ZrNi 2, можуть діяти як «водневі губки», зробило практичним використання гідридів металів як катодного матеріалу. Однією з особливостей Ni-MH клітин є те, що їх підзарядка є екзотермічним процесом, так що необхідно допускати належне розсіювання тепла. Ці батареї широко використовуються в стільникових телефонах, комп'ютерах та портативних електроінструментах. Електродні реакції відбуваються в концентрованому електроліті КОН: Катод (+): NiOH + Н 2 О + е — → Ni (ОН) 2 + ОН — Анод (-): (1/х) МН х + ОН — → (1/х) М + Н 2 О + е — |
|
1990-ті - літієві елементи (Sony Corp.)
|
Літій є ідеальним анодним матеріалом завдяки своїй низькій щільності та високому потенціалу відновлення, що робить клітини на основі Li найбільш компактними способами зберігання електричної енергії. Літієві клітини використовуються в наручних годинниках, кардіостимуляторах і цифрових камерах. Обидва первинні (не перезаряджаються) та акумуляторні типи були доступні протягом деякого часу. Більш пізні програми є в портативних електроінструментів і - мабуть, найголовніше, в електричних або гібридних автомобілей. Сучасні літієві елементи працюють шляхом транспортування іонів Li + між електродами, в які іони можуть бути вставлені або інтеркалізовані. Катоди - це оксиди перехідних металів літію, такі як LiCoO 3, тоді як аноди - вуглець, що містить літій, LiC 6. Вид, який піддається окисленню-відновленню, - це не літій, а перехідний метал, наприклад Co (III) -Co (IV). |
Літієві батареї як запальні пристрої
Були численні повідомлення про пожежі та вибухи, пов'язані з літієвими батареями. У 2006 році корпорації Dell довелося відкликати 4,1 мільйона акумуляторів Sony, які були поставлені разом з ноутбуками Dell і були визнані під загрозою через виробничий дефект. Це ілюструє труднощі концентрації великої кількості хімічної енергії в невеликому пакеті, що, звичайно, є метою всіх розробників акумуляторів, які прагнуть задовольнити комерційні вимоги, починаючи від побутової особистої електроніки до автомобілів з електричним живленням. Повністю заряджені катоди оксиду кобальту літію з дефіцитом літію за своєю суттю нестабільні, контролюються лише тонкою ізоляційною мембраною, яка, якщо випадково зламається, може призвести до термічного втечі за участю газоподібного кисню, вуглецю, органічних розчинників та (в деяких випадках) хлорат літію - все компоненти, необхідні для запеклого вогню.
Багато досліджень пішло в розробку безвідмовних мембран. В одному типі, виготовленому ExxonMobil і орієнтованому на автомобільний ринок, пори призначені для закриття і, таким чином, гальмують проходження іонів літію, коли температура піднімається вище безпечного рівня.
Біологічні батареї
Наостанок слід згадати про біологічних батареях, які зустрічаються в ряді електричних риб. «Електричні органи» цих риб є модифікованими м'язовими клітинами, відомими як електроцити, які розташовані в довгих стеках. Нейронний сигнал від мозку призводить до того, що всі електроцити в стеці поляризуються одночасно, фактично створюючи батарею, виготовлену з послідовно з'єднаних клітин. Більшість електричних риб виробляють лише невелику напругу, яку вони використовують для навігації, багато в тому, як кажани використовують звук для ехо-розташування здобичі. Відомий електричний вугор, однак, здатний виробляти 600-вольтовий поштовх, який він використовує, щоб оглушити довколишню здобич.