7.3: Робота і тепло
- Page ID
- 22645
- Визначте тип роботи з точки зору тиску і обсягу.
- Визначте теплоту.
- Пов'язати кількість тепла зі зміною температури.
Ми вже визначили роботу як силу, що діє через відстань. Існують і інші еквівалентні визначення роботи, які також важливі в хімії.
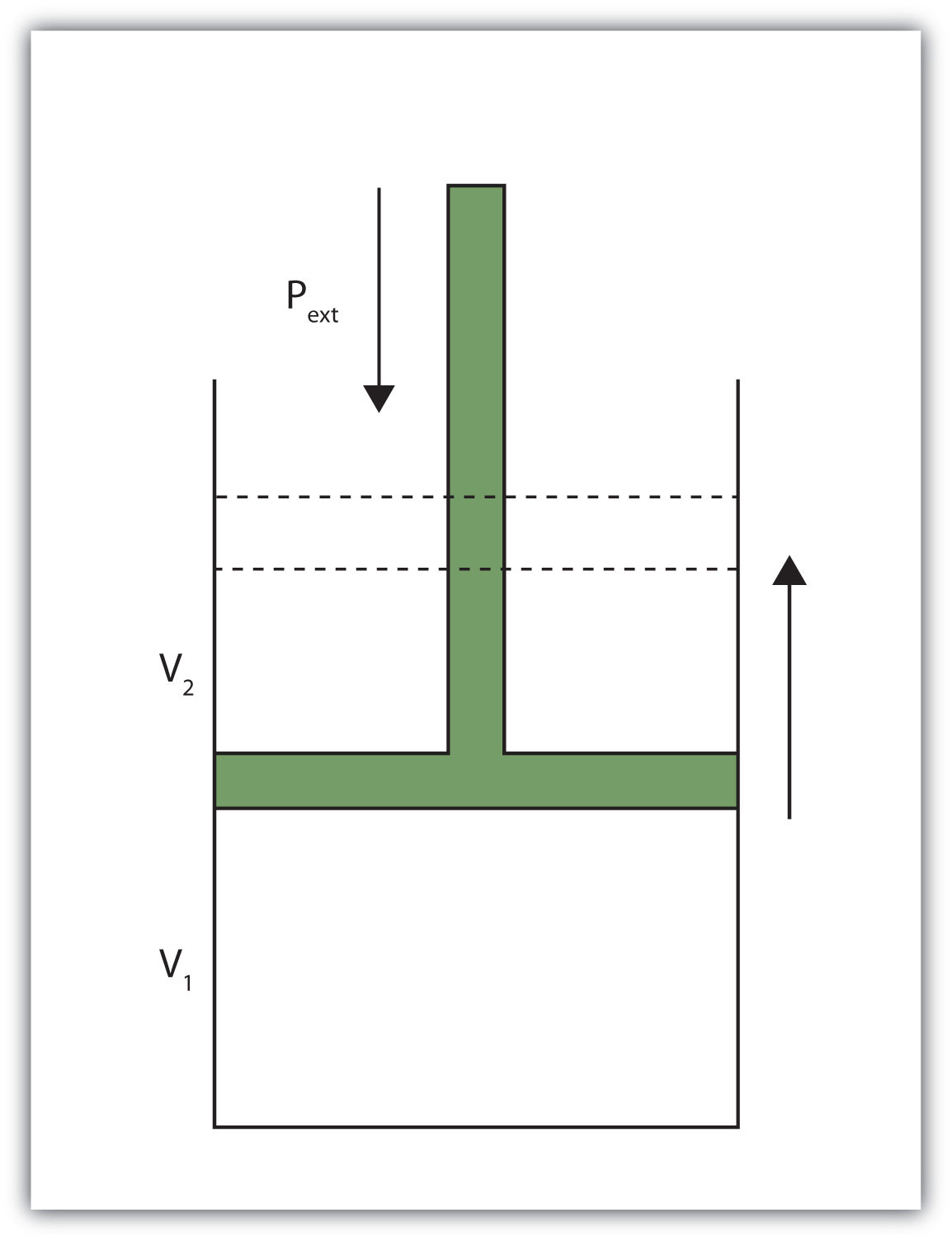
Коли певний обсяг газу розширюється, він працює проти зовнішнього тиску для розширення (рис.\(\PageIndex{1}\) - Об'єм проти тиску). Тобто газ повинен виконувати роботи. Якщо припустити, що зовнішній тиск P ext є постійним, обсяг роботи, виконаної газом, задається рівнянням
\[w = −P_{ext} × ΔV \nonumber \]
\(ΔV\)де - зміна обсягу газу. Цей термін завжди кінцевий обсяг мінус початковий обсяг,
\[ΔV = V_{final} − V_{initial} \nonumber \]
і може бути позитивним або негативним, залежно від того, є V кінцевим більшим (розширюється) або меншим (скорочується), ніж V початковий. Негативний знак в рівнянні для роботи важливий і має на увазі, що в міру розширення обсягу (Δ V позитивний) газ в системі втрачає енергію в міру роботи. З іншого боку, якщо газ стискається, Δ V є негативним, а два негативні ознаки роблять роботу позитивною, тому енергія додається до системи.
Наостанок розглянемо одиниці. Зміни обсягу зазвичай виражаються в одиницях, як літри, тоді як тиск зазвичай виражається в атмосферах. Коли ми використовуємо рівняння для визначення роботи, одиниця для роботи виходить як літр·атмосфер, або L·ATM. Це не дуже поширений агрегат для роботи. Однак існує коефіцієнт перерахунку між L·atm і загальною одиницею роботи, джоулями:
1 л·атм = 101,32 Дж
Використовуючи цей коефіцієнт перетворення та попереднє рівняння для роботи, ми можемо обчислити роботу, виконану при розширенні або стисненні газу.
Яку роботу виконує газ, якщо він розширюється з 3,44 л до 6,19 л проти постійного зовнішнього тиску 1,26 атм? Висловіть остаточну відповідь в джоулі.
Рішення
Для початку потрібно визначити зміну обсягу, Δ V. Зміна - це завжди кінцеве значення мінус початкове значення:
Δ V = V кінцевий − V початковий = 6,19 L − 3,44 L = 2,75 L
Тепер ми можемо скористатися визначенням роботи для визначення виконаної роботи:
w = − P внутр · Δ V = − (1,26 атм) (2,75 л) = −3,47 л·атм
Тепер будуємо коефіцієнт перетворення з співвідношення між літр·атмосфер і джоулями:
\[-3.47\cancel{L.atm}\times \times \frac{101.32\, J}{1\cancel{L.atm}}=-351\, J\nonumber \]
Обмежуємо остаточну відповідь трьома значущими цифрами, якщо це доречно.
Яка робота виконується при розширенні газу від 0,66 л до 1,33 л проти зовнішнього тиску 0,775 атм?
- Відповідь
-
−53 ДЖ
Тепло - ще один аспект енергії. Тепло - це передача енергії від одного тіла до іншого за рахунок різниці температур. Наприклад, коли ми торкаємося чогось руками, ми інтерпретуємо цей предмет як гарячий або холодний залежно від того, як передається енергія: Якщо енергія передається у ваші руки, об'єкт відчуває себе гарячим. Якщо енергія передається від рук до предмета, руки відчувають холод. Оскільки тепло є мірою передачі енергії, тепло також вимірюється в джоулі.
Для даного об'єкта кількість задіяного тепла (q) пропорційна двом речам: масі об'єкта (\(m\)) і зміні температури (\(ΔT\)), викликаному передачею енергії. Ми можемо записати це математично як
\[q\alpha \, m\times \Delta T\nonumber \]
де означає «пропорційно». Щоб зробити пропорційність рівністю, ми включаємо константу пропорційності. При цьому константа пропорційності позначається c і називається питомою теплоємністю, або, більш лаконічно, питомою теплотою:
\ [q = mCΔt\ number\]
де маса, питома теплоємність, зміна температури множаться разом. Питома теплота - це міра того, скільки енергії потрібно для зміни температури речовини; чим більше питома теплота, тим більше енергії потрібно для зміни температури. Агрегати для питомої теплоти є
в залежності від того, яка\(ΔT\) одиниця. Можна відзначити відхід від наполягання, що температура виражається в Кельвіні. Це пов'язано з тим, що зміна температури має однакове значення, незалежно від того, виражаються температури в градусах Цельсія або кельвінів.
Розрахуйте задіяну теплоту при підвищенні температури 25,0 г Fe від 22° C до 76° C, питома теплоємність Fe становить 0,449 Дж/г ·° C.
Рішення
Для початку потрібно визначити Δ T. Зміна - це завжди кінцеве значення мінус початкове значення:
Δ Т = 76°C − 22°C = 54°C
Тепер ми можемо використовувати вираз для q, замінити всі змінні, і вирішити для тепла:
\[q=(25.0\, g)(0.449\frac{J}{g.^{\circ}C})(54^{\circ}C)=610\, J\nonumber \]
Зверніть увагу, як одиниці g і° C скасовують, залишаючи J, одиницю тепла. Також зверніть увагу, що це значення q за своєю суттю є позитивним, тобто енергія йде в систему.
Розрахуйте задіяну теплоту при підвищенні температури 76,5 г Ag з 17,8° C до 144,5° C Питома теплоємність Ag становить 0,233 Дж/г ·° C.
- Відповідь
-
2 260 КМ
Як і в будь-якому рівнянні, коли ви знаєте всю змінну, крім однієї, у виразі для q, ви можете визначити змінну, що залишилася, використовуючи алгебру.
Для підвищення температури 373 г Hg на 104° C потрібно 5 408 Дж тепла.
Рішення
Ми можемо почати з рівняння для q, але тепер дані різні значення, і нам потрібно вирішити для питомої теплоти. Зверніть увагу, що Δ T дається безпосередньо як 104° C. підставляючи,
5,408 Дж = (373 г) c (104° C)
Розділимо обидві сторони рівняння на 373 г і 104°C:
\[c=\frac{5408\, J}{(373g)(104^{\circ}C)}\nonumber \]
Поєднавши числа і зібравши воєдино всі одиниці, отримуємо
\[c=0.139\frac{J}{g.^{\circ}C}\nonumber \]
Золото має питому теплоємність 0,129 Дж/г ·°С, якщо для підвищення температури зразка золота на 99,9° C потрібно 1,377 Дж, яка маса золота?
- Відповідь
-
107 г
Таблиця\(\PageIndex{1}\): Питомі теплоти різних речовин, перераховуються питомі теплоти деяких речовин. Питома теплоємність - це фізична властивість речовин, тому вона є характеристикою речовини. Загальна думка полягає в тому, що чим нижче питома теплоємність, тим менше енергії потрібно для зміни температури речовини на певну кількість.
| Речовина | Питома теплота (Дж/г ·° C) |
|---|---|
| вода | 4.184 |
| залізо | 0,449 |
| золото | 0.129 |
| ртуті | 0.139 |
| алюміній | 0.900 |
| етиловий спирт | 2.419 |
| магній | 1.03 |
| гелій | 5.171 |
| кисень | 0,918 |
Ключові виноси
- Робота може бути визначена як зміна обсягу газу проти постійного зовнішнього тиску.
- Тепло - це передача енергії за рахунок перепадів температур.
- Тепло можна розраховувати за масою, зміною температури, питомою теплотою.
