14.2: Фактори, що впливають на тиск газу
Тиск повітря в баскетболі потрібно регулювати так, щоб м'яч відскакував на правильну висоту. Перед грою, чиновники перевіряють м'яч, скинувши його з висоти плечей і бачачи, як далеко назад він відскакує. Що б чиновник зробив, якби м'яч не підскочив вгору досить високо, або якщо він відскочив занадто високо?
Тиск всередині контейнера залежить від кількості газу всередині контейнера. Якщо баскетбол не підстрибує досить високо, чиновник може виправити ситуацію, використовуючи ручний насос і додавши більше повітря до м'яча. І навпаки, якщо він підстрибує занадто високо, чиновник може випустити трохи повітря з м'яча.
Фактори, що впливають на тиск газу
Нагадаємо з кінетико-молекулярної теорії, що частинки газу рухаються випадково і по прямих лініях до тих пір, поки вони пружно не зіткнуться або з іншими частинками газу, або з однією зі стінок контейнера. Саме ці зіткнення зі стінками ємності визначають тиск газу. Чотири змінні використовуються для опису стану газу: тиск(P)(V), об'єм(T), температура та кількість газу, виміряна кількістю молів (\ left (n\ right)\). Ми розглянемо окремо, як обсяг, температура та кількість газу кожен впливає на тиск закритого зразка газу.
Кількість газу
На малюнку нижче показано, що відбувається при додаванні повітря в жорстку ємність. Жорсткий контейнер - це той, який не здатний розширюватися або скорочуватися. Сталева каністра - приклад жорсткої ємності.
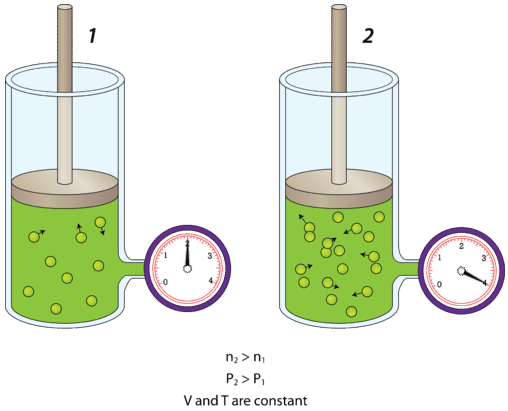
Каністра зліва містить газ під певним тиском. Потім приєднаний повітряний насос використовується для подвоєння кількості газу в каністрі. Оскільки каністра не може розширюватися, збільшена кількість молекул повітря буде вражати внутрішні стінки каністри вдвічі частіше, ніж раніше. Результатом є те, що тиск всередині каністри подвоюється. Як ви могли собі уявити, якщо все більше і більше повітря постійно додається до жорсткого контейнера, він може врешті-решт лопнути. Зменшення кількості молекул в жорсткій ємності має зворотний ефект, і тиск знижується.
Обсяг
На тиск впливає і обсяг ємності. Якщо обсяг контейнера зменшується, молекули газу мають менше місця, в якому можна пересуватися. В результаті вони будуть частіше вдарятися об стінки ємності, а тиск підвищується.
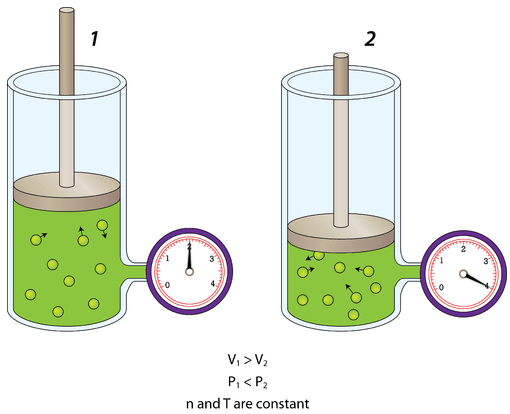
На малюнку нижче показаний балон з газом, обсяг якого регулюється регульованим поршнем. Зліва поршень витягується в основному назовні і манометр зчитує певний тиск. Праворуч поршень штовхнули так, щоб обсяг закритої частини ємності, де знаходиться газ, був скорочений навпіл. Тиск газу подвоюється. Збільшення обсягу ємності мало б зворотний ефект, а тиск газу зменшився б.
Температура
Було б дуже недоцільно розміщувати баночку супу над багаттям, не випускаючи банки. У міру нагрівання банки вона може вибухнути. Кінетико-молекулярна теорія пояснює, чому. Повітря всередині жорсткої банки супу отримує більше кінетичної енергії від тепла, що надходить від багаття. Кінетична енергія змушує молекули повітря рухатися швидше; вони частіше і з більшою силою впливають на стінки контейнера. Збільшення тиску всередині може з часом перевищити міцність банки і вона вибухне. Додатковим фактором є те, що суп може почати кипіти, що потім сприятиме ще більшому газу і більшому тиску на внутрішню частину банки.
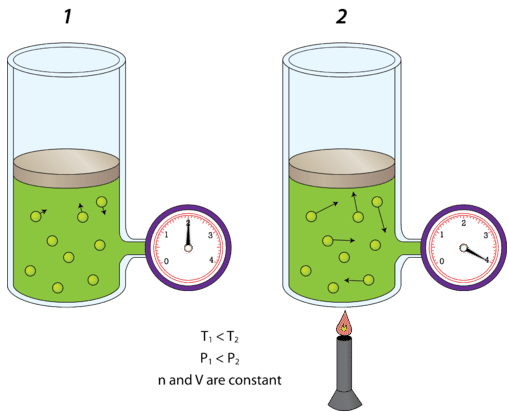
На малюнку нижче зображений балон з газом (зліва), який знаходиться при кімнатній температурі(300K). Праворуч циліндр нагрівався до тих пір, поки температура Кельвіна не збільшилася вдвічі600K. Кінетична енергія молекул газу збільшується, тому зіткнення зі стінками ємності тепер більш сильні, ніж були раніше. В результаті тиск газу подвоюється. Зниження температури матиме протилежний ефект, а тиск закритого газу зменшиться.
Резюме
- Збільшення кількості молекул газу, при цьому обсяг ємності залишається постійним, підвищує тиск.
- Зменшення об'єму ємності підвищує тиск газу.
- Підвищення температури газу в жорсткій ємності підвищує тиск.