4.19: Атомна одиниця маси
Нинішня система вимірювання в Сполучених Штатах являє собою солянку різних одиниць, багато з яких важко взаємоконвертувати. Ми принаймні маємо стандартизовані одиниці в наші дні, на відміну від минулих століть. Свого часу виміри довжини визначалися як відстань від кінця одного придатка до іншого. Наприклад, двір визначався як відстань від носа короля до кінчика великого пальця, коли його рука була витягнута.
Стандартизовані вимірювання дозволяють людям всюди отримати однакову кількість чогось. Зверніть увагу на червоні та білі мітки на газовому насосі, зображені нижче. Ці етикетки засвідчують, що газовий насос був перевірений і перекачує точний галон газу. Стандартні вимірювання в науці дуже важливі, щоб ми могли порівняти експериментальні дані з однієї лабораторії в іншу, і переконатися, що ми всі говоримо про одне і те ж.
Атомна маса
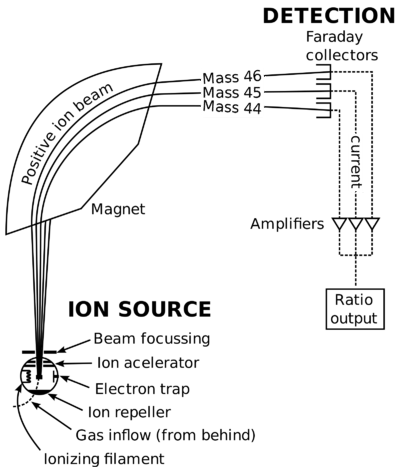
Маси окремих атомів дуже і дуже малі. Використовуючи сучасний прилад під назвою мас-спектрометр, можна виміряти такі незначні маси. Атом кисню-16, наприклад, має масу в2.66×10−23g. Хоча порівняння мас, виміряних у грамах, мали б певну корисність, набагато практичніше мати систему, яка дозволить нам легше порівнювати відносні атомні маси. Вчені вирішили використовувати нуклід вуглецю-12 як еталонний стандарт, за яким будуть порівнюватися всі інші маси. За визначенням одному атому вуглецю-12 присвоюється маса 12 атомних одиниць маси(amu). Атомна одиниця маси визначається як маса, рівна одній дванадцятій масі атома вуглецю-12. Маса будь-якого ізотопу будь-якого елемента виражається по відношенню до стандарту вуглець-12. Наприклад, один атом гелію-4 має масу в4.0026amu. Атом сірки-32 має масу в31.972amu.
Атом вуглецю-12 має в своєму ядрі шість протонів і шість нейтронів для масового числа 12. Оскільки на ядро припадає майже вся маса атома, один протон або одиночний нейтрон має масу приблизно1amu. Однак, як видно з прикладів гелію та сірки, маси окремих атомів не є цілими числами. Це пов'язано з тим, що на масу атома дуже незначно впливає взаємодія різних частинок всередині ядра, і враховується мала маса електрона.
Резюме
- Вуглець-12 є еталоном для всіх розрахунків атомної маси.
- Атомна одиниця маси визначається як маса, рівна одній дванадцятій масі атома вуглецю-12.
- На масу атома впливають взаємодії частинок всередині ядра.
Рецензія
- Який прилад використовується для вимірювання маси атомів?
- Скільки важить один атом кисню-16 в грамах?
- Який еталонний стандарт для одиниць атомної маси?
- Як визначається одиниця атомної маси?
- Чому числа для атомної маси окремих атомів не цілі числа?
