1.7: Ендокринна система
- Page ID
- 72893
Вступ

Вивчивши цю главу, ви зможете:
- Визначте внесок ендокринної системи в гомеостаз
- Обговорити хімічний склад гормонів і механізми дії гормонів
- Узагальнити місце виробництва, регуляції та впливу гормонів гіпофіза, щитовидної залози, паращитовидної залози, надниркових залоз та шишкоподібної залози
- Обговоріть гормональну регуляцію репродуктивної системи
- Поясніть роль ендокринних клітин підшлункової залози в регуляції глюкози в крові
- Визначте гормони, що виділяються серцем, нирками та іншими органами з вторинними ендокринними функціями
- Обговорити кілька поширених захворювань, пов'язаних з дисфункцією ендокринної системи
- Обговорити ембріональний розвиток і вплив старіння на ендокринну систему
Можливо, ви ніколи не думали про це таким чином, але коли ви надсилаєте текстове повідомлення двом друзям, щоб зустрітися з вами в їдальні о шостій годині, ви надсилаєте цифрові сигнали, які (сподіваєтесь) вплинуть на їхню поведінку - навіть якщо вони знаходяться на деякій відстані. Аналогічно певні клітини посилають хімічні сигнали іншим клітинам організму, які впливають на їх поведінку. Цей міжклітинний зв'язок на міжміські відстані, координація та контроль є критичними для гомеостазу, і це основна функція ендокринної системи.
Огляд ендокринної системи
До кінця цього розділу ви зможете:
- Розрізняють види міжклітинного зв'язку, їх значення, механізми і наслідки
- Визначте основні органи і тканини ендокринної системи і їх розташування в організмі
Зв'язок - це процес, при якому відправник передає сигнали одному або декільком приймачам для контролю і координації дій. В організмі людини в відносно «далекому» спілкуванні беруть участь дві основні системи органів: нервова система і ендокринна система. Разом ці дві системи в першу чергу відповідають за підтримку гомеостазу в організмі.
Нейронна та ендокринна сигналізація
Нервова система використовує два типи міжклітинного зв'язку - електричну та хімічну сигналізацію - або прямою дією електричного потенціалу, або в останньому випадку через дію хімічних нейромедіаторів, таких як серотонін або норадреналін. Нейромедіатори діють локально і швидко. Коли електричний сигнал у вигляді потенціалу дії надходить на синаптичний термінал, вони розсіюються через синаптичну щілину (проміжок між нейроном, що відправляє і приймальним нейроном або м'язовою клітиною). Після того, як нейромедіатори взаємодіють (зв'язуються) з рецепторами на приймальній (постсинаптичної) клітині, стимуляція рецепторів перетворюється у відповідь, таку як продовження електричної сигналізації або модифікація клітинної відповіді. Клітинка-мішень реагує протягом мілісекунд після отримання хімічного «повідомлення»; ця реакція потім дуже швидко припиняється, як тільки нейронна сигналізація закінчується. Таким чином, нейронна комунікація забезпечує функції організму, які передбачають швидкі, короткі дії, такі як рух, відчуття та пізнання. На відміну від цього, ендокринна система використовує лише один метод зв'язку: хімічну сигналізацію. Ці сигнали посилаються ендокринними органами, які виділяють хімічні речовини - гормон - у позаклітинну рідину. Гормони транспортуються переважно через кровотік по всьому тілу, де вони зв'язуються з рецепторами на клітинах-мішенях, викликаючи характерну відповідь. Як результат, ендокринна сигналізація вимагає більше часу, ніж нейронна сигналізація, щоб спонукати відповідь у клітинах-мішенях, хоча точна кількість часу змінюється залежно від різних гормонів. Наприклад, гормони, що виділяються, коли ви стикаєтеся з небезпечною або лякаючою ситуацією, яка називається реакцією боротьби чи втечі, відбуваються вивільненням гормонів надниркових залоз - адреналіну та норадреналіну - протягом декількох секунд. Навпаки, може знадобитися до 48 годин, щоб клітини-мішені реагували на певні репродуктивні гормони.
Крім того, ендокринна сигналізація, як правило, менш специфічна, ніж нейронна сигналізація. Один і той же гормон може відігравати певну роль у різних фізіологічних процесах залежно від залучених клітин-мішеней. Наприклад, гормон окситоцин сприяє скороченню матки у породіль. Це також важливо при грудному вигодовуванні, і може бути залучено в сексуальну реакцію та почуття емоційної прихильності як у чоловіків, так і у жінок.
Взагалі нервова система передбачає швидку реакцію на швидкі зміни зовнішнього середовища, а ендокринна система, як правило, повільніше діє - піклуючись про внутрішнє середовище організму, підтримуючи гомеостаз та контролюючи розмноження (Таблиця (Ендокринна та нервова системи)). Отже, як реакція боротьби чи втечі, про яку згадувалося раніше, відбувається так швидко, якщо гормони зазвичай повільніше діють? Це тому, що дві системи з'єднані. Саме швидка дія нервової системи у відповідь на небезпеку в навколишньому середовищі стимулює надниркові залози виділяти свої гормони. Як результат, нервова система може викликати швидкі ендокринні реакції, щоб не відставати від різких змін як у зовнішньому, так і у внутрішньому середовищі, коли це необхідно.
| Ендокринна та нервова системи | ||
|---|---|---|
| Ендокринна система | Нервова система | |
| Механізм (и) сигналізації | Хімічна | Хімічні/електричні |
| Первинний хімічний сигнал | Гормони | Нейромедіатори |
| Пройдена відстань | Довгі або короткі | Завжди короткий |
| Час відгуку | Швидкий або повільний | Завжди швидко |
| Навколишнє середовище цільового | Внутрішні | Внутрішня і зовнішня |
Структури ендокринної системи
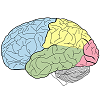
Ендокринна система складається з клітин, тканин і органів, які виділяють гормони в якості первинної або вторинної функції. Ендокринна залоза є основним гравцем в цій системі. Основною функцією цих безпротокових залоз є виділення своїх гормонів безпосередньо в навколишню рідину. Потім інтерстиціальна рідина і кровоносні судини транспортують гормони по всьому тілу. До складу ендокринної системи входять гіпофіз, щитовидна, паращитовидна, надниркова і шишкоподібна залози (рис. 1. Ендокринна система). Деякі з цих залоз мають як ендокринні, так і неендокринні функції. Наприклад, підшлункова залоза містить клітини, які функціонують у травленні, а також клітини, які виділяють гормони інсулін та глюкагон, які регулюють рівень глюкози в крові. Гіпоталамус, тимус, серце, нирки, шлунок, тонкий кишечник, печінка, шкіра, жіночі яєчники та чоловічі яєчка - це інші органи, які містять клітини з ендокринною функцією. Більш того, вже давно відомо, що жирова тканина виробляє гормони, а останні дослідження показали, що навіть кісткова тканина має ендокринні функції.

Безпротокові ендокринні залози не слід плутати з екзокринною системою організму, чиї залози виділяють свої виділення через протоки. Приклади екзокринних залоз включають сальні і потові залози шкіри. Як тільки що зазначалося, підшлункова залоза також має екзокринну функцію: велика частина її клітин виділяє панкреатичний сік через підшлункову і допоміжну протоки в просвіт тонкої кишки.
Інші види хімічної сигналізації
При ендокринній сигналізації гормони, що виділяються в позаклітинну рідину, дифундують у кров або лімфу, а потім можуть долати великі відстані по всьому тілу. На відміну від цього, аутокринна сигналізація відбувається в межах однієї і тієї ж клітини. Аутокрин (auto - = «self») - це хімічна речовина, яка викликає відповідь в тій же клітині, яка її секретувала. Інтерлейкін-1, або ІЛ-1, є сигнальною молекулою, яка відіграє важливу роль у запальній реакції. Клітини, які виділяють ІЛ-1, мають рецептори на їх клітинній поверхні, які зв'язують ці молекули, в результаті чого відбувається аутокринна сигналізація.
Локальний міжклітинний зв'язок - це провінція паракрину, яку також називають паракринним фактором, який є хімічною речовиною, що індукує відповідь у сусідніх клітинам. Хоча паракрини можуть потрапляти в кров, їх концентрація, як правило, занадто низька, щоб викликати відповідь з віддалених тканин. Знайомим прикладом для тих, хто страждає на астму, є гістамін, паракрин, який виділяється імунними клітинами в бронхіальному дереві. Гістамін змушує клітини гладкої мускулатури бронхів звужуватися, звужуючи дихальні шляхи. Інший приклад - нейромедіатори нервової системи, які діють лише локально всередині синаптичної щілини.
Ендокринолог
Ендокринологія - спеціальність в галузі медицини, яка фокусується на лікуванні порушень ендокринної системи. Ендокринологи - лікарі, які спеціалізуються в цій галузі, є фахівцями в лікуванні захворювань, пов'язаних з гормональною системою, починаючи від захворювань щитовидної залози і закінчуючи цукровим діабетом. Ендокринні хірурги лікують ендокринні захворювання шляхом видалення або резекції ураженої ендокринної залози.
Пацієнти, яких направляють до ендокринологів, можуть мати ознаки та симптоми або результати аналізу крові, які свідчать про надмірне або порушене функціонування ендокринної залози або ендокринних клітин. Ендокринолог може призначити додаткові аналізи крові, щоб визначити, чи є гормональний фон пацієнта ненормальним, або вони можуть стимулювати або пригнічувати функцію підозрюваної ендокринної залози, а потім взяти кров на аналіз. Лікування варіюється залежно від діагнозу. Деякі ендокринні порушення, такі як діабет 2 типу, можуть реагувати на зміни способу життя, такі як скромна втрата ваги, прийняття здорової дієти та регулярні фізичні навантаження. Інші розлади можуть вимагати прийому ліків, таких як заміна гормонів та звичайний моніторинг ендокринолога. До них відносяться порушення гіпофіза, які можуть вплинути на ріст і порушення щитовидної залози, які можуть призвести до різних метаболічних проблем.
Деякі пацієнти відчувають проблеми зі здоров'ям в результаті нормального зниження гормонів, які можуть супроводжувати старіння. Ці пацієнти можуть проконсультуватися з ендокринологом, щоб зважити ризики та переваги замісної гормональної терапії, призначеної для підвищення їх природного рівня репродуктивних гормонів.
Окрім лікування пацієнтів, ендокринологи можуть брати участь у дослідженнях, щоб покращити розуміння порушень ендокринної системи та розробити нові методи лікування цих захворювань.
Огляд глави
Ендокринна система складається з клітин, тканин і органів, які виділяють гормони, критичні для гомеостазу. Організм координує свої функції за допомогою двох основних типів зв'язку: нервової та ендокринної. Нейронний зв'язок включає як електричну, так і хімічну сигналізацію між нейронами і клітинами-мішенями. Ендокринна комунікація передбачає хімічну сигналізацію за допомогою викиду гормонів у позаклітинну рідину. Звідти гормони дифундують у кров і можуть подорожувати до віддалених областей тіла, де вони викликають відповідь у клітинах-мішенях. Ендокринні залози - це безпротокові залози, які виділяють гормони. Багато органів тіла з іншими первинними функціями - такими як серце, шлунок і нирки - також мають гормони секретують клітини.
Гормони
До кінця цього розділу ви зможете:
- Визначте три основні класи гормонів на основі хімічної структури
- Порівняйте і контрастуйте внутрішньоклітинні і клітинні мембранні гормональні рецептори
- Опишіть сигнальні шляхи, які включають CamP та IP3
- Визначте кілька факторів, які впливають на реакцію клітини-мішені
- Обговоріть роль петель зворотного зв'язку та гуморальних, гормональних та нервових подразників у контролі гормонів
Хоча даний гормон може подорожувати по всьому тілу в крові, це вплине на активність тільки його клітини-мішені; тобто клітини з рецепторами для цього конкретного гормону. Після того, як гормон зв'язується з рецептором, ініціюється ланцюжок подій, що призводить до реакції клітини-мішені. Гормони відіграють вирішальну роль у регуляції фізіологічних процесів через реакції клітин-мішеней, які вони регулюють. Ці відповіді сприяють розмноженню людини, росту та розвитку тканин організму, обміну речовин, рідини та електролітного балансу, сну та багатьох інших функцій організму. Основні гормони людського організму і їх наслідки визначені в таблиці (ендокринні залози і їх основні гормони).
| Ендокринні залози та їх основні гормони | |||
|---|---|---|---|
| ендокринна залоза | супутні гормони | Хімічний клас | Ефект |
| Гіпофіз (передній) | Гормон росту (GH) | Протеїн | Сприяє зростанню тканин організму |
| Гіпофіз (передній) | Пролактин (PRL) | Пептид | Сприяє виробленню молока |
| Гіпофіз (передній) | Тиреотропний гормон (ТТГ) | глікопротеїн | Стимулює вивільнення гормонів |
| Гіпофіз (передній) | Адренокортикотропний гормон (АКТГ) | Пептид | Стимулює викид гормонів корою надниркових |
| Гіпофіз (передній) | Фолікулостимулюючий гормон (ФСГ) | глікопротеїн | Стимулює вироблення гамет |
| Гіпофіз (передній) | Лютеїнізуючого гормону (ЛГ) | глікопротеїн | Стимулює вироблення андрогенів статевими залозами |
| Гіпофіз (задній) | Антидіуретичний гормон (АДГ) | Пептид | Стимулює реабсорбцію води нирками |
| Гіпофіз (задній) | Окситоцин | Пептид | Стимулює скорочення матки під час пологів |
| Щитовидна | Тироксин (Т 4), трийодтиронін (Т 3) | Амін | Стимулювати основний метаболізм |
| Щитовидна | Кальцитонін | Пептид | Знижує рівень Ca 2+ в крові |
| паращитовидної залози | Паратиреоїдний гормон (ПТГ) | Пептид | Підвищує рівень Ca 2+ в крові |
| Надниркових залоз (кора) | Альдостерон | Стероїдні | Підвищує рівень Na + в крові |
| Надниркових залоз (кора) | Кортизол, кортикостерон, кортизон | Стероїдні | Підвищення рівня глюкози в крові |
| Наднирники (мозок) | Адреналін, норадреналін | Амін | Стимулюйте реакцію бій чи втечу |
| шишкоподібний | Мелатонін | Амін | Регулює цикли сну |
| підшлункової залози | Інсулін | Протеїн | Знижує рівень глюкози в крові |
| підшлункової залози | глюкагон | Протеїн | Підвищує рівень глюкози в крові |
| яєчка | Тестостерон | Стероїдні | Стимулює розвиток чоловічих вторинних статевих ознак і вироблення сперми |
| яєчники | Естрогени і прогестерон | Стероїдні | Стимулюють розвиток жіночих вторинних статевих ознак і готують організм до пологів |
види гормонів
Гормони людського організму можна розділити на дві основні групи на основі їх хімічної структури. Гормони, отримані з амінокислот, включають аміни, пептиди, і білки. Ті, що походять від ліпідів, включають стероїди (Рисунок 1. Амін, пептид, білок, і структура стероїдних гормонів). Ці хімічні групи впливають на розподіл гормону, тип рецепторів він зв'язується з, і інші аспекти його функції.

Амін Гормони
Гормони, отримані від модифікації амінокислот, називаються гормонами аміну. Як правило, вихідна структура амінокислоти модифікована таким чином, що —COOH, або карбоксильна, група видаляється, тоді як -NH 3 +, або амін, група залишається.
Гормони аміну синтезуються з амінокислот триптофану або тирозину. Прикладом гормону, отриманого з триптофану, є мелатонін, який секретується шишкоподібною залозою і допомагає регулювати циркадний ритм. Похідні тирозину включають гормони щитовидної залози, що регулюють обмін речовин, а також катехоламіни, такі як адреналін, норадреналін та дофамін. Адреналін і норадреналін секретуються мозковим мозком надниркових залоз і відіграють певну роль у реакції боротьби або польоту, тоді як дофамін секретується гіпоталамусом і пригнічує вивільнення певних передніх гормонів гіпофіза.
Пептид і білкові гормони
Тоді як амінні гормони походять від однієї амінокислоти, пептидні та білкові гормони складаються з декількох амінокислот, які зв'язуються, утворюючи амінокислотний ланцюг. Пептидні гормони складаються з коротких ланцюжків амінокислот, тоді як білкові гормони - більш довгі поліпептиди. Обидва типи синтезуються, як і інші білки організму: ДНК транскрибується в мРНК, яка перекладається в амінокислотний ланцюг.
Приклади пептидних гормонів включають антидіуретичний гормон (АДГ), гормон гіпофіза, важливий для балансу рідини, і передсердно-натрійуретичний пептид, який виробляється серцем і сприяє зниженню артеріального тиску. Деякі приклади білкових гормонів включають гормон росту, який виробляється гіпофізом, і фолікулостимулюючий гормон (ФСГ), який має приєднану вуглеводну групу і, таким чином, класифікується як глікопротеїн. ФСГ допомагає стимулювати дозрівання яйцеклітин в яєчниках і сперматозоїдів в яєчках.
Стероїдні гормони
Первинні гормони, отримані з ліпідів, є стероїди. Стероїдні гормони виводяться з ліпідного холестерину. Наприклад, репродуктивні гормони тестостерон і естрогени, які виробляються статевими залозами (яєчка і яєчники) - це стероїдні гормони. Наднирники виробляють стероїдний гормон альдостерон, який бере участь в осморегуляції, і кортизол, який відіграє певну роль в обміні речовин.
Як і холестерин, стероїдні гормони не розчиняються у воді (вони гідрофобні). Оскільки кров на водній основі, гормони, отримані з ліпідів, повинні подорожувати до своєї цільової клітини-цілі, пов'язаної з транспортним білком. Ця більш складна структура продовжує період напіввиведення стероїдних гормонів набагато довше, ніж гормони, отримані з амінокислот. Період напіврозпаду гормону є час, необхідний для половини концентрації гормону, щоб бути деградовані. Наприклад, ліпідний гормон кортизол має період напіврозпаду приблизно від 60 до 90 хвилин. На відміну від цього, амінокислота - похідний гормон адреналін має період напіврозпаду приблизно одну хвилину.
Шляхи дії гормонів
Повідомлення, яке посилає гормон, приймається рецептором гормонів, білком, розташованим або всередині клітини, або всередині клітинної мембрани. Рецептор оброблятиме повідомлення, ініціюючи інші сигнальні події або клітинні механізми, які призводять до реакції клітини-мішені. Гормонові рецептори розпізнають молекули зі специфічними формами і бічними групами, і реагують тільки на ті гормони, які розпізнаються. Один і той же тип рецепторів може розташовуватися на клітині різних тканин організму, і викликати дещо різні реакції. Таким чином, реакція, викликана гормоном, залежить не тільки від гормону, але і від клітини-мішені.
Як тільки клітина-мішень отримує сигнал гормону, вона може реагувати різними способами. Відповідь може включати стимуляцію синтезу білка, активацію або дезактивацію ферментів, зміну проникності клітинної мембрани, змінені швидкості мітозу і росту клітин, а також стимуляцію секреції продуктів. Більше того, один гормон може бути здатний індукувати різні реакції в даній клітині.
Шляхи за участю внутрішньоклітинних рецепторів гормон
Внутрішньоклітинні рецептори гормонів розташовані всередині клітини. Гормони, які зв'язуються з цим типом рецепторів, повинні мати можливість перетнути клітинну мембрану. Стероїдні гормони походять з холестерину і тому можуть легко дифузно через ліпідний бішар клітинної мембрани, щоб досягти внутрішньоклітинного рецептора (рис. Зв'язування ліпідно-розчинних гормонів). Гормони щитовидної залози, які містять бензольні кільця, шиповані йодом, також є ліпідно-розчинними і можуть потрапляти в клітину.
Розташування зв'язування стероїдних і тиреоїдних гормонів відрізняється незначно: стероїдний гормон може зв'язуватися з його рецептором всередині цитозолу або всередині ядра. У будь-якому випадку це зв'язування генерує комплекс гормон-рецепторів, який рухається до хроматину в ядрі клітини і зв'язується з певним сегментом ДНК клітини. На відміну від цього, гормони щитовидної залози зв'язуються з рецепторами, вже пов'язаними з ДНК. Як для стероїдних, так і для гормонів щитовидної залози зв'язування гормон-рецепторного комплексу з ДНК запускає транскрипцію гена-мішені до мРНК, який переміщається в цитозол і направляє синтез білка рибосомами.

Шляхи за участю рецепторів гормонів мембрани клітин
Гідрофільні або водорозчинні гормони не в змозі дифузувати через ліпідний бішар клітинної мембрани і тому повинні передавати своє повідомлення рецептору, розташованому на поверхні клітини. За винятком гормонів щитовидної залози, які є ліпідно-розчинними, всі гормони, отримані амінокислотами, зв'язуються з рецепторами клітинної мембрани, які розташовані, принаймні частково, на позаклітинній поверхні клітинної мембрани. Тому вони не впливають безпосередньо на транскрипцію генів-мішеней, а замість цього ініціюють сигнальний каскад, який здійснюється молекулою, яка називається другим месенджером. В цьому випадку гормон називається першим месенджером.
Другий месенджер, який використовується більшістю гормонів, - циклічний аденозинмонофосфат (цАМФ). У другій системі посланника цАМФ водорозчинний гормон зв'язується зі своїм рецептором в клітинній мембрані (Крок 1 на рис. 3. (Зв'язування водорозчинних гормонів)). Цей рецептор пов'язаний з внутрішньоклітинним компонентом, званим білком G, і зв'язування гормону активує компонент G-білка (Крок 2). Активований білок G, в свою чергу, активує фермент під назвою аденілілциклаза, також відомий як аденілатциклаза (Крок 3), який перетворює аденозинтрифосфат (АТФ) в цАМФ (Крок 4). Як другий месенджер, цАМФ активує тип ферменту, який називається білково-кіназою, яка присутня в цитозолі (Крок 5). Активовані протеїнкінази ініціюють фосфорилирующий каскад, в якому множинні протеїнкінази фосфорилюють (додають фосфатну групу до) численні і різні клітинні білки, включаючи інші ферменти (Крок 6).

Фосфорилювання клітинних білків може викликати найрізноманітніші ефекти, від метаболізму поживних речовин до синтезу різних гормонів та інших продуктів. Ефекти варіюються залежно від типу клітини-мішені, задіяних G-білків та кіназ та фосфорилювання білків. Приклади гормонів, які використовують цАМФ як другий месенджер, включають кальцитонін, який важливий для побудови кісток та регулювання рівня кальцію в крові; глюкагон, який відіграє роль у рівні глюкози в крові; і тиреотропний гормон, який викликає вивільнення T 3 і T 4 з щитовидної залози.
Загалом, каскад фосфорилювання значно підвищує ефективність, швидкість та специфічність гормональної відповіді, оскільки тисячі сигнальних подій можуть бути ініційовані одночасно у відповідь на дуже низьку концентрацію гормону в крові. Однак тривалість гормонального сигналу коротка, оскільки цАМФ швидко деактивується ферментом фосфодіестеразою (ФДЕ), який знаходиться в цитозолі. Дія PDE допомагає гарантувати, що реакція клітини-мішені швидко припиняється, якщо нові гормони не надходять на клітинну мембрану.
Важливо відзначити, що існують також білки G, які знижують рівень цАМФ в клітині у відповідь на зв'язування гормонів. Наприклад, коли гормон росту інгібуючий гормон (GHIH), також відомий як соматостатин, зв'язується з його рецепторами в гіпофізі, рівень цАМФ знижується, тим самим пригнічуючи секрецію людського гормону росту.
Не всі водорозчинні гормони ініціюють другу систему месенджера цАМФ. Одна поширена альтернативна система використовує іони кальцію як другий месенджер. У цій системі білки G активують фермент фосфоліпазу С (ПЛК), який функціонує аналогічно аденілілциклазі. Після активації ПЛК розщеплює зв'язаний мембраною фосфоліпід на дві молекули: діацилгліцерин (DAG) та трифосфат інозитолу (IP 3). Як і цАМФ, DAG активує протеїнкінази, які ініціюють каскад фосфорилювання. У той же час IP 3 викликає виділення іонів кальцію з місць зберігання всередині цитозолю, наприклад, зсередини гладкої ендоплазматичної сітки. Потім іони кальцію діють як другі месенджери двома способами: вони можуть безпосередньо впливати на ферментативну та іншу клітинну діяльність, або вони можуть зв'язуватися з білками, що зв'язують кальцій, найпоширенішим з яких є кальмодулін. Після зв'язування кальцію кальмодулін здатний модулювати протеїнкіназу всередині клітини. Приклади гормонів, які використовують іони кальцію як другий месенджер системи включають ангіотензин II, який допомагає регулювати кров'яний тиск через звуження судин, і гормон росту-рилізинг гормону (GHRH), який викликає гіпофіз вивільнити гормони росту.
Фактори, що впливають на відповідь цільових клітин
Ви пам'ятаєте, що клітини-мішені повинні мати рецептори, специфічні для даного гормону, якщо цей гормон повинен викликати відповідь. Але на реакцію клітини-мішені впливають кілька інших факторів. Наприклад, наявність значного рівня гормону, що циркулює в крові, може призвести до того, що клітини-мішені зменшують кількість рецепторів цього гормону. Цей процес називається downgulation, і це дозволяє клітинам стати менш реактивними до надмірного рівня гормонів. Коли рівень гормону хронічно знижується, клітини-мішені беруть участь в регуляції, щоб збільшити їх кількість рецепторів. Цей процес дозволяє клітинам бути більш чутливими до гормону, який присутній. Клітини також можуть змінювати чутливість самих рецепторів до різних гормонів.
Два або більше гормонів можуть взаємодіяти, щоб впливати на реакцію клітин різними способами. Три найпоширеніші типи взаємодії такі:
- Дозволюючий ефект, при якому присутність одного гормону дозволяє іншому гормону діяти. Наприклад, гормони щитовидної залози мають складні дозвільні відносини з певними репродуктивними гормонами. Таким чином, дефіцит йоду, компонента гормонів щитовидної залози, може вплинути на розвиток і функціонування репродуктивної системи.
- Синергетичний ефект, при якому два гормони зі схожими ефектами виробляють посилену реакцію. У деяких випадках для адекватної реакції потрібно два гормони. Наприклад, два різні репродуктивні гормони - ФСГ з гіпофіза і естрогени з яєчників - необхідні для дозрівання жіночих яйцеклітин (яйцеклітин).
- Антагоністичний ефект, при якому два гормони мають протилежну дію. Знайомий приклад - вплив двох гормонів підшлункової залози, інсуліну і глюкагону. Інсулін збільшує зберігання печінки глюкози у вигляді глікогену, знижуючи рівень глюкози в крові, тоді як глюкагон стимулює розпад запасів глікогену, підвищуючи рівень глюкози в крові.
Регуляція секреції гормонів
Щоб запобігти ненормальному рівню гормонів та потенційному захворюванню, рівень гормонів повинен бути жорстко контрольований. Організм підтримує цей контроль, балансуючи вироблення гормонів і деградацію. Петлі зворотного зв'язку регулюють ініціювання та підтримку більшості секреції гормонів у відповідь на різні подразники.
Роль петель зворотного зв'язку
Внесок петель зворотного зв'язку в гомеостаз буде лише коротко розглянуто тут. Позитивні петлі зворотного зв'язку характеризуються виділенням додаткового гормону у відповідь на вихідне виділення гормону. Вивільнення окситоцину під час пологів - петля позитивного зворотного зв'язку. Початковий викид окситоцину починає сигналізувати про скорочення маткових м'язів, що штовхає плід до шийки матки, змушуючи його розтягуватися. Це, в свою чергу, сигналізує гіпофізу вивільнити більше окситоцину, викликаючи посилення трудових скорочень. Вивільнення окситоцину зменшується після народження дитини.
Більш поширеним методом регуляції гормонів є петля негативного зворотного зв'язку. Негативний зворотний зв'язок характеризується пригніченням подальшої секреції гормону у відповідь на адекватні рівні цього гормону. Це дозволяє рівень гормону в крові регулюватися в вузькому діапазоні. Прикладом петлі негативного зворотного зв'язку є вивільнення глюкокортикоїдних гормонів з надниркових залоз, за вказівкою гіпоталамуса і гіпофіза. У міру підвищення концентрації глюкокортикоїдів в крові гіпоталамус і гіпофіз знижують свою сигналізацію надниркових залоз для запобігання додаткової секреції глюкокортикоїдів (рис. Негативний зворотний зв'язок).

Роль стимулів ендокринних залоз
Рефлекси, спровоковані як хімічними, так і нервовими подразниками, контролюють ендокринну активність. Ці рефлекси можуть бути простими, включаючи лише одну відповідь на гормони, або вони можуть бути більш складними і включати багато гормонів, як у випадку з гіпоталамічним контролем різних передніх гормонів, що контролюються гіпофізом.
Гуморальні подразники - це зміни рівня в крові негормональних хімічних речовин, таких як поживні речовини або іони, які викликають вивільнення або гальмування гормону, щоб, в свою чергу, підтримувати гомеостаз. Наприклад, осморецептори в гіпоталамусі виявляють зміни осмолярності крові (концентрацію розчинених речовин в плазмі крові). Якщо осмолярність крові занадто висока, що означає, що кров недостатньо розріджена, осморецептори сигналізують гіпоталамусу про вивільнення АДГ. Гормон змушує нирки реабсорбувати більше води і зменшувати обсяг виробленої сечі. Така реабсорбція викликає зниження осмолярності крові, розріджуючи кров до відповідного рівня. Регуляція глюкози в крові - ще один приклад. Високий рівень глюкози в крові викликає викид інсуліну з підшлункової залози, що збільшує поглинання глюкози клітинами і зберігання печінки глюкози у вигляді глікогену.
Ендокринна залоза може також виділяти гормон у відповідь на присутність іншого гормону, що виробляється інший ендокринної залози. Такі гормональні подразники часто залучають гіпоталамус, який виробляє рилізинг і пригнічують гормони, що контролюють секрецію різноманітних гормонів гіпофіза.
Крім цих хімічних сигналів, гормони також можуть виділятися у відповідь на нервові подразники. Поширеним прикладом нервових подразників є активація реакції «бій чи втеча» симпатичною нервовою системою. Коли індивід сприймає небезпеку, симпатичні нейрони сигналізують наднирковим залозам про виділення норадреналіну і адреналіну. Два гормони розширюють кровоносні судини, збільшують частоту серця та дихання та пригнічують травну та імунну системи. Ці відповіді підвищують транспортування організму кисню до мозку та м'язів, тим самим покращуючи здатність організму боротися або тікати.
Бісфенол А і ендокринні порушення
Можливо, ви чули новини про вплив хімічної речовини під назвою бісфенол А (BPA) у різних типах харчової упаковки. BPA використовується у виробництві твердих пластмас і епоксидних смол. Загальні предмети, пов'язані з харчовими продуктами, які можуть містити BPA, включають підкладку алюмінієвих банок, пластикові контейнери для зберігання їжі, чашки для пиття, а також дитячі пляшечки та «сиппі» чашки. Інші види використання BPA включають медичне обладнання, зубні пломби та футерування водопровідних труб.
Дослідження показують, що BPA є ендокринним порушником, а це означає, що він негативно впливає на ендокринну систему, особливо в період пренатального та післяпологового розвитку. Зокрема, BPA імітує гормональні ефекти естрогенів і має протилежний ефект - андрогенів. Управління з контролю за продуктами та ліками США (FDA) зазначає у своїй заяві про безпеку BPA, що, хоча традиційні дослідження токсикології підтримували безпеку низьких рівнів впливу BPA, останні дослідження з використанням нових підходів до тестування на тонкі ефекти призвели до деякого занепокоєння потенційними наслідками BPA на мозок, поведінку та передміхурову залозу у плодів, немовлят та маленьких дітей. FDA в даний час сприяє зменшенню використання BPA в харчових матеріалах. Багато американських компаній добровільно видалили BPA з дитячих пляшечок, «сиппі» чашок та накладок банок для дитячих сумішей, а більшість продаваних сьогодні пластикових пляшок з водою багаторазового використання можуть похвалитися тим, що вони «не містять BPA». На відміну від цього, і Канада, і Європейський Союз повністю заборонили використання BPA в дитячих товарах.
Потенційні шкідливі наслідки BPA були вивчені як на тваринних моделям, так і на людях і включають в себе велику різноманітність наслідків для здоров'я, таких як затримка розвитку та захворювання. Наприклад, пренатальний вплив BPA протягом першого триместру вагітності людини може бути пов'язано з хрипами і агресивною поведінкою в дитячому віці. Дорослі, схильні до високого рівня BPA, можуть відчувати змінену сигналізацію щитовидної залози та чоловічу сексуальну дисфункцію. Експозиція BPA під час пренатального або післяпологового періоду розвитку у моделей тварин спостерігалася, що спричиняє неврологічні затримки, зміни структури та функції мозку, сексуальну дисфункцію, астму та підвищений ризик розвитку множинних ракових захворювань. Дослідження in vitro також показали, що вплив BPA викликає молекулярні зміни, які ініціюють розвиток раку молочної залози, передміхурової залози та мозку. Хоча ці дослідження залучили BPA до численних шкідливих наслідків для здоров'я, деякі експерти застерігають, що деякі з цих досліджень можуть бути недосконалими і що потрібно провести більше досліджень. Тим часом FDA рекомендує споживачам вжити запобіжних заходів, щоб обмежити їх вплив BPA. На додаток до придбання продуктів харчування в упаковці без BPA, споживачі повинні уникати перенесення або зберігання продуктів або рідин у пляшках з кодом переробки 3 або 7. Продукти та рідини не повинні нагріватися мікрохвильовою піччю у будь-якій формі пластику: замість цього використовуйте папір, скло або кераміку.
Огляд глави
Гормони походять з амінокислот або ліпідів. Гормони аміну походять з амінокислот триптофану або тирозину. Більші амінокислотні гормони включають пептиди і білкові гормони. Стероїдні гормони виводяться з холестерину.
Стероїдні гормони і гормон щитовидної залози є ліпід Всі інші гормони, отримані амінокислотами, розчинні у воді. Гідрофобні гормони здатні дифузно крізь мембрану і взаємодіяти з внутрішньоклітинним рецептором. На відміну від цього, гідрофільні гормони повинні взаємодіяти з рецепторами клітинної мембрани. Вони, як правило, пов'язані з білком G, який активується, коли гормон зв'язує рецептор. Це ініціює сигнальний каскад, який включає другий месенджер, такий як циклічний аденозинмонофосфат (цАМФ). Другі системи месенджерів значно посилюють гормональний сигнал, створюючи більш широку, ефективнішу та швидшу реакцію.
Гормони виділяються при стимуляції, яка має хімічне або нервове походження. Регуляція викиду гормонів в першу чергу досягається за рахунок негативного зворотного зв'язку. Різні подразники можуть викликати викид гормонів, але є три основних типи. Гуморальні подразники - це зміни рівня іонів або поживних речовин у крові. Гормональні подразники - це зміни рівня гормонів, які ініціюють або пригнічують секрецію іншого гормону. Нарешті, нервовий подразник виникає, коли нервовий імпульс спонукає до секреції або гальмування гормону.
Гіпофіз і гіпоталамус
До кінця цього розділу ви зможете:
- Поясніть взаємозв'язки анатомії і функцій гіпоталамуса і задньої і передньої частки гіпофіза
- Визначте два гормони, що виділяються із заднього гіпофіза, їх клітини-мішені та їх основні дії
- Визначте шість гормонів, що виробляються передньою часткою гіпофіза, їх клітинами-мішенями, їх основними діями та їх регулюванням гіпоталамусом
Гіпоталамус-гіпофізарний комплекс можна розглядати як «командний центр» ендокринної системи. Цей комплекс виділяє кілька гормонів, які безпосередньо виробляють реакції в тканинах-мішенях, а також гормони, що регулюють синтез і секрецію гормонів інших залоз. Крім того, комплекс гіпоталамус-гіпофіз координує повідомлення ендокринної та нервової систем. У багатьох випадках стимул, отриманий нервовою системою, повинен проходити через комплекс гіпоталамус-гіпофіз, щоб бути перетвореним на гормони, які можуть ініціювати відповідь.
Гіпоталамус - це будова проміжного мозку, розташованого спереду і нижче таламуса (рис. Гіпоталамус-гіпофізарний комплекс). Він має як нервову, так і ендокринну функції, виробляючи і виділяючи багато гормонів. Крім того, гіпоталамус анатомічно і функціонально пов'язаний з гіпофізом (або гіпофізом), органом розміром з боби, підвішеним до нього стовбуром, який називається інфундибулом (або гіпофізом стебла). Гіпофіз колискою всередині sellaturcica клиноподібної кістки черепа. Він складається з двох часток, які виникають з різних частин ембріональної тканини: задній гіпофіз (нейрогіпофіз) - нервова тканина, тоді як передній гіпофіз (також відомий як аденогіпофіз) - це залозиста тканина, яка розвивається з примітивного травного тракту. Гормони, що виділяються заднім і переднім гіпофізом, і проміжною зоною між частками зведені в табл. (Гормони гіпофіза).

| гормони гіпофіза | |||
|---|---|---|---|
| Доля гіпофіза | супутні гормони | Хімічний клас | Ефект |
| Передній | Гормон росту (GH) | Протеїн | Сприяє зростанню тканин організму |
| Передній | Пролактин (PRL) | Пептид | Сприяє виробленню молока з молочних залоз |
| Передній | Тиреотропний гормон (ТТГ) | глікопротеїн | Стимулює виділення гормонів щитовидної залози |
| Передній | Адренокортикотропний гормон (АКТГ) | Пептид | Стимулює викид гормонів корою надниркових |
| Передній | Фолікулостимулюючий гормон (ФСГ) | глікопротеїн | Стимулює вироблення гамет в статевих залозах |
| Передній | Лютеїнізуючого гормону (ЛГ) | глікопротеїн | Стимулює вироблення андрогенів статевими залозами |
| Задня | Антидіуретичний гормон (АДГ) | Пептид | Стимулює реабсорбцію води нирками |
| Задня | Окситоцин | Пептид | Стимулює скорочення матки під час пологів |
| Проміжна зона | Меланоцитарно-стимулюючий гормон | Пептид | Стимулює утворення меланіну в меланоцитах |
задній гіпофіз
Задній гіпофіз насправді є продовженням нейронів паравентрикулярного і супраоптичного ядер гіпоталамуса. Клітинні тіла цих областей відпочивають в гіпоталамусі, але їх аксони спускаються як гіпоталамо-гіпофізарний тракт всередині інфундибулума, і закінчуються в аксонових терміналах, які складають задній гіпофіз (рис. 2. Задній гіпофіз).

Задній гіпофіз не виробляє гормони, а скоріше зберігає і виділяє гормони, що виробляються гіпоталамусом. Паравентрикулярні ядра виробляють гормон окситоцин, тоді як супраоптичні ядра виробляють АДГ. Ці гормони подорожують по аксонам в місця зберігання в аксонних терміналах заднього гіпофіза. У відповідь на сигнали від тих же гіпоталамічних нейронів гормони вивільняються з терміналів аксона в кров.
Окситоцин
Коли розвиток плода завершується, пептидний гормон окситоцин (tocia- = «пологи») стимулює скорочення матки і розширення шийки матки. Протягом більшої частини вагітності рецептори гормону окситоцину не виражаються при високих рівнях в матці. Ближче до кінця вагітності синтез окситоцинових рецепторів в матці збільшується, а гладком'язові клітини матки стають більш чутливими до його впливу. Окситоцин постійно вивільняється протягом пологів через механізм позитивного зворотного зв'язку. Як зазначалося раніше, окситоцин спонукає маткові скорочення, які штовхають головку плода до шийки матки. У відповідь розтягнення шийки матки стимулює додатковий окситоцин, який синтезується гіпоталамусом і вивільняється з гіпофіза. Це підвищує інтенсивність і ефективність скорочень матки і спонукає до додаткового розширення шийки матки. Петля зворотного зв'язку триває до народження.
Хоча високий рівень окситоцину в крові матері починає знижуватися відразу після народження, окситоцин продовжує відігравати певну роль у здоров'ї матері та новонародженого. По-перше, окситоцин необхідний для рефлексу викиду молока (зазвичай його називають «відпускати») у годуючих жінок. У міру того як новонароджений починає смоктати, сенсорні рецептори в сосках передають сигнали гіпоталамусу. У відповідь окситоцин виділяється і викидається в кров. Протягом декількох секунд клітини в молочних протоках матері скорочуються, викидаючи молоко в рот немовляти. По-друге, як у чоловіків, так і у жінок вважається, що окситоцин сприяє зв'язку батьків та новонароджених, відомому як прихильність. Вважається, що окситоцин також бере участь у почуттях любові та близькості, а також у сексуальній реакції.
Антидіуретичний гормон (АДГ)
Концентрація розчиненої речовини в крові, або осмолярність крові, може змінюватися у відповідь на споживання певних продуктів і рідин, а також у відповідь на захворювання, травми, ліки або інші фактори. Осмолярність крові постійно контролюється осморецепторами - спеціалізованими клітинами в межах гіпоталамуса, які особливо чутливі до концентрації іонів натрію та інших розчинених речовин.
У відповідь на високу осмолярність крові, яка може виникнути під час зневоднення або після дуже солоної їжі, осморецептори сигналізують задньому гіпофізу про вивільнення антидіуретичного гормону (АДГ). Клітини-мішені АДГ розташовуються в трубчастих клітині нирок. Його дія полягає в підвищенні проникності епітелію для води, що дозволяє збільшити реабсорбцію води. Чим більше води реабсорбується з фільтрату, тим більша кількість води, яка повертається в кров і тим менше, що виділяється з сечею. Більша концентрація води призводить до зниження концентрації розчинених речовин. АДГ також відомий як вазопресин, оскільки в дуже високих концентраціях він викликає звуження кровоносних судин, що підвищує артеріальний тиск за рахунок збільшення периферичного опору. Вивільнення АДГ контролюється петлею негативного зворотного зв'язку. У міру зменшення осмолярності крові гіпоталамічні осморецептори відчувають зміну і спонукають відповідне зниження секреції АДГ. В результаті з фільтрату сечі реабсорбується менше води.
Цікаво, що препарати можуть впливати на секрецію АДГ. Наприклад, споживання алкоголю гальмує виділення АДГ, що призводить до збільшення вироблення сечі, що в кінцевому підсумку може призвести до зневоднення та похмілля. Захворювання під назвою нецукровий діабет характеризується хронічною недостатньою продукцією АДГ, що викликає хронічне зневоднення. Оскільки мало АДГ виробляється і виділяється, недостатня кількість води реабсорбується нирками. Хоча пацієнти відчувають спрагу та збільшують споживання рідини, це не ефективно знижує концентрацію розчиненої речовини в крові, оскільки рівень АДГ недостатньо високий, щоб викликати реабсорбцію води в нирках. Електролітний дисбаланс може виникнути у важких випадках нецукрового діабету.
Передня гіпофіза
Передній гіпофіз бере початок з травного тракту в ембріоні і мігрує до мозку під час розвитку плода. Розрізняють три області: pars distalis - сама передня, pars intermedia примикає до заднього гіпофіза, а pars tuberalis - струнка «трубка», яка обгортає інфундибулум.
Нагадаємо, що задній гіпофіз не синтезує гормони, а просто зберігає їх. На відміну від цього, передній гіпофіз виробляє гормони. Однак секреція гормонів з передньої частини гіпофіза регулюється двома класами гормонів. Ці гормони, що виділяються гіпоталамусом - є вивільняючими гормонами, які стимулюють секрецію гормонів з передньої частини гіпофіза та інгібуючих гормонів, які пригнічують секрецію.
Гіпоталамічні гормони секретуються нейронами, але надходять в передній гіпофіз через кровоносні судини (рис. 3. Передній гіпофіз). Всередині інфундибулума знаходиться міст капілярів, який з'єднує гіпоталамус з переднім гіпофізом. Ця мережа, яка називається гіпофізарною портальною системою, дозволяє транспортувати гормони гіпоталамуса до передньої частини гіпофіза без попереднього потрапляння в системний кровотік. Система бере свій початок від верхньої гіпофізарної артерії, яка відгалужується від сонних артерій і транспортує кров до гіпоталамуса. Гілки верхньої гіпофізарної артерії утворюють гипофізарную портальну систему (див. Рис. Передній гіпофіз). Гіпоталамічні вивільняють і гальмують гормони подорожують через первинне капілярне сплетіння до ворітних вен, які несуть їх в передній гіпофіз. Гормони, що виробляються переднім гіпофізом (у відповідь на вивільнення гормонів), надходять у вторинне капілярне сплетіння, а звідти стікають в кровообіг.

Передній гіпофіз виробляє сім гормонів. Це гормон росту (GH), тиреотропний гормон (ТТГ), адренокортикотропний гормон (АКТГ), фолікулостимулюючий гормон (ФСГ), лютеїнізуючий гормон (ЛГ), бета-ендорфін та пролактин. З гормонів передньої частини гіпофіза ТТГ, АКТГ, ФСГ і ЛГ в сукупності називають тропічними гормонами (троп- = «поворот»), оскільки вони включають або вимикають функцію інших залоз внутрішньої секреції.
Гормон росту
Ендокринна система регулює зростання людського організму, синтез білка, і клітинної реплікації. Основний гормон, що беруть участь у цьому процесі є гормон росту (GH), також називається соматотропін — білковий гормон виробляється і секретується передньої гіпофіза залози. Його основна функція є анаболічним; він сприяє синтезу білка і побудови тканин за допомогою прямих і непрямих механізмів (рис. 4. Гормональна регуляція росту). Рівні GH контролюються вивільненням GHRH і GHIH (також відомий як соматостатин) з гіпоталамуса.

Глюкозощадний ефект виникає, коли ГР стимулює ліполіз, або розпад жирової тканини, виділяючи жирні кислоти в кров. В результаті багато тканин переходять з глюкози на жирні кислоти в якості свого основного джерела енергії, а значить, з кровотоку забирається менше глюкози.
GH також ініціює діабетогенний ефект, в якому GH стимулює печінку, щоб розщепити глікоген до глюкози, який потім депонується в крові. Назва «діабетогенний» походить від подібності в підвищеному рівні глюкози в крові спостерігається між особами з нелікованим цукровим діабетом і осіб, які відчувають надлишок GH. Рівень глюкози в крові підвищується в результаті поєднання глюкозощадного і діабетогенного ефектів.
GH опосередковано опосередковує зростання і синтез білка шляхом запуску печінки та інших тканин виробляти групу білків, званих інсуліноподібними факторами росту (IGF). Ці білки посилюють клітинну проліферацію і пригнічують апоптоз або запрограмовану загибель клітин. IGF стимулюють клітини, щоб збільшити їх поглинання амінокислот з крові для синтезу білка. Клітини скелетних м'язів і хрящів особливо чутливі до стимуляції від IGF.
Дисфункція контролю росту ендокринної системи може призвести до декількох порушень. Наприклад, гігантизм - це розлад у дітей, який викликаний секрецією аномально великої кількості GH, що призводить до надмірного зростання. Подібний стан у дорослих є акромегалія, розлад, який призводить до зростання кісток в обличчя, руки, і ноги у відповідь на надмірний рівень GH у осіб, які перестали рости. Аномально низький рівень GH у дітей може викликати порушення росту — розлад називається гіпофіза карликовості (також відомий як недолік гормону росту).
Тиреотропний гормон
Діяльність щитовидної залози регулюється тиреотропним гормоном (ТТГ), також званим тиреотропіном. ТТГ вивільняється з передньої частини гіпофіза у відповідь на тиреотропін-рилізинг гормон (ТРГ) з гіпоталамуса. Як обговорювалося коротко, він запускає секрецію гормонів щитовидної залози щитовидною залозою. У класичному циклі негативного зворотного зв'язку підвищений рівень гормонів щитовидної залози в крові потім викликає падіння виробництва ТРГ і згодом ТТГ.
Адренокортикотропний гормон
Адренокортикотропний гормон (АКТГ), який також називають кортикотропіном, стимулює кору надниркових залоз (більш поверхнева «кора» надниркових залоз) секретувати кортикостероїдні гормони, такі як кортизол. АКТГ походять від молекули попередника, відомої як про-опіомеланотропін (POMC), яка при розщепленні виробляє кілька біологічно активних молекул, включаючи АКТГ, меланоцит-стимулюючий гормон та опіоїдні пептиди мозку, відомі як ендорфіни.
Вивільнення АКТГ регулюється кортикотропін-рилізинг-гормоном (CRH) з гіпоталамуса у відповідь на нормальні фізіологічні ритми. Різноманітні стресові фактори також можуть впливати на його вивільнення, а роль АКТГ у реакції на стрес обговорюється далі в цьому розділі.
Фолікулостимулюючий гормон і лютеїнізуючого гормону
Ендокринні залози виділяють різні гормони, які контролюють розвиток і регуляцію репродуктивної системи (ці залози включають передню гіпофіз, кору надниркових залоз, і статеві залози - яєчка у чоловіків і яєчники у жінок). Значна частина розвитку репродуктивної системи відбувається в період статевого дозрівання і відзначається розвитком статево-специфічних ознак як у чоловіків, так і у жіночих підлітків. Статеве дозрівання ініціюється гонадотропін-рилізинг-гормоном (GnRH), гормоном, що виробляється і секретується гіпоталамусом. ГнРГ стимулює передній гіпофіз виділяти гонадотропіни - гормони, які регулюють функцію статевих залоз. Рівні GnRH регулюються через петлю негативного зворотного зв'язку; високі рівні репродуктивних гормонів гальмують вивільнення ГнРГ. Протягом усього життя гонадотропіни регулюють репродуктивну функцію і, у випадку з жінками, початок і припинення репродуктивної здатності.
До складу гонадотропінів входять два глікопротеїнові гормони: фолікулостимулюючий гормон (ФСГ) стимулює вироблення і дозрівання статевих клітин, або гамети, включаючи яйцеклітини у жінок і сперматозоїди у чоловіків. ФСГ також сприяє росту фолікулів; ці фолікули потім вивільняють естрогени в жіночих яєчниках. Лютеїнізуючий гормон (ЛГ) запускає овуляцію у жінок, а також вироблення яєчниками естрогенів і прогестерону. ЛГ стимулює вироблення тестостерону чоловічими яєчками.
пролактин
Як випливає з назви, пролактин (ПРЛ) сприяє лактації (виробленню молока) у жінок. Під час вагітності він сприяє розвитку молочних залоз, а після пологів стимулює молочні залози виробляти грудне молоко. Однак ефекти пролактину сильно залежать від дозвільних ефектів естрогенів, прогестерону та інших гормонів. І як зазначалося раніше, відведення молока відбувається у відповідь на стимуляцію з боку окситоцину.
У невагітної жінки секреція пролактину пригнічується гормоном, що інгібує пролактин (ПІГ), який насправді є нейромедіатором дофаміну, і вивільняється з нейронів в гіпоталамусі. Тільки під час вагітності рівень пролактину підвищується у відповідь на пролактин-рилізинг гормон (PRH) з гіпоталамуса.
Проміжний гіпофіз: Меланоцит-стимулюючий гормон
Клітини в зоні між частками гіпофіза виділяють гормон, відомий як меланоцит-стимулюючий гормон (MSH), який утворюється при розщепленні протеїна-попередника про-опіомеланокортину (POMC). Місцеве вироблення MSH в шкірі відповідає за вироблення меланіну у відповідь на вплив ультрафіолетового світла. Роль MSH, що виробляється гіпофізом, є більш складною. Наприклад, люди зі світлішою шкірою зазвичай мають таку ж кількість MSH, як люди з більш темною шкірою. Тим не менш, цей гормон здатний потемніти шкіру, індукуючи вироблення меланіну в меланоцитах шкіри. Жінки також демонструють підвищене вироблення MSH під час вагітності; в поєднанні з естрогенами це може призвести до більш темної пігментації шкіри, особливо шкіри ареол і малих статевих губ. Малюнок 5. (Основні гормони гіпофіза) є резюме гормонів гіпофіза і їх основні ефекти.

Огляд глави
Комплекс гіпоталамус-гіпофіз знаходиться в проміжному відділі головного мозку. Гіпоталамус і гіпофіз з'єднані структурою, яка називається інфундибулом, яка містить судинну систему і нервові аксони. Гіпофіз ділиться на дві різні структури з різним ембріональним походженням. У задній частці розміщені аксонні термінали гіпоталамічних нейронів. Він зберігає і виділяє в кров два гіпоталамічні гормони: окситоцин і антидіуретичний гормон (АДГ). Передня частка з'єднана з гіпоталамусом судинною системою в інфундибулі і виробляє і виділяє шість гормонів. Їх секреція регулюється, однак, шляхом вивільнення і пригнічення гормонів з гіпоталамуса. Шість передніх гормонів гіпофіза: гормон росту (GH), тиреотропний гормон (ТТГ), адренокортикотропний гормон (АКТГ), фолікулостимулюючий гормон (ФСГ), лютеїнізуючий гормон (ЛГ) та пролактин (PRL).
Щитовидна залоза
До кінця цього розділу ви зможете:
- Опишіть розташування і анатомію щитовидної залози
- Обговорити синтез трийодтироніну і тироксину
- Поясніть роль гормонів щитовидної залози в регуляції основного обміну
- Визначте гормон, що виробляється парафолікулярними клітинами щитовидної залози
Орган у формі метелика щитовидна залоза розташована спереду від трахеї, трохи поступається гортані (рис. 1. Щитовидна залоза). Медіальна область, звана перешийком, фланкується крилоподібної лівою і правою частками. Кожна з часток щитовидної залози закладена паращитовидними залозами, в першу чергу на їх задніх поверхнях. Тканина щитовидної залози складається в основному з фолікулів щитовидної залози. Фолікули складаються з центральної порожнини, заповненої липкою рідиною, званої колоїдної. Оточений стінкою епітеліальних фолікульних клітин, колоїд є центром вироблення гормонів щитовидної залози, і це виробництво залежить від необхідного та унікального компонента гормонів: йоду.

Синтез і вивільнення тиреоїдних
Гормони виробляються в колоїді, коли атоми мінерального йоду приєднуються до глікопротеїну, званому тиреоглобуліном, який секретується в колоїд клітинами фолікула. Наступні кроки окреслюють збірку гормонів:
- Зв'язування ТТГ з його рецепторами в фолікульних клітині щитовидної залози змушує клітини активно транспортувати іони йодиду (I —) через свою клітинну мембрану, з кровотоку в цитозол. В результаті концентрація іонів йодиду, «потрапили» в фолікулярні клітини, у багато разів перевищує концентрацію в крові.
- Іони йодиду потім переміщаються в просвіт клітин фолікула, які межують з колоїдом. Там іони піддаються окисленню (видаляються їх негативно заряджені електрони). Окислення двох іонів йодиду (2 I —) призводить до отримання йоду (I 2), який проходить через мембрану клітини фолікула в колоїд.
- У колоїді ферменти пероксидази пов'язують йод з амінокислотами тирозину в тиреоглобуліні для отримання двох посередників: тирозин, приєднаний до одного йоду, і тирозин, приєднаний до двох йодів. Коли один з кожного з цих посередників пов'язаний ковалентними зв'язками, отримане з'єднання - трийодтиронін (Т 3), гормон щитовидної залози з трьома йодами. Набагато частіше дві копії другої посередницької зв'язку, утворюючи тетрайодтиронін, також відомий як тироксин (T 4), гормон щитовидної залози з чотирма йодами.
Ці гормони залишаються в колоїдному центрі фолікулів щитовидної залози до тих пір, поки ТТГ не стимулює ендоцитоз колоїду назад в клітини фолікула. Там лізосомальні ферменти розщеплюють колоїд тиреоглобуліну, виділяючи вільні Т 3 і Т 4, які дифузіруются по мембрані клітини фолікула і потрапляють в кров.
У крові менше одного відсотка циркулюючих Т 3 і Т 4 залишається незв'язаним. Цей вільний T 3 і T 4 може перетнути ліпідний бішар клітинних мембран і бути прийнятий клітинами. Решта 99 відсотків циркулюючих T 3 і T 4 пов'язані зі спеціалізованими транспортними білками, званими тироксинзв'язуючими глобулінами (ТБГ), з альбуміном або з іншими білками плазми. Така «упаковка» запобігає їх вільній дифузії в клітини організму. Коли рівень Т 3 і Т 4 в крові починає знижуватися, пов'язані Т 3 і Т 4 звільняються з цих білків плазми і легко перетинають мембрану клітин-мішеней. Т 3 є більш потужним, ніж T 4, і багато клітин перетворюють T 4 в T 3 шляхом видалення атома йоду.
Регуляція синтезу ТГ
Вивільнення Т 3 і Т 4 з щитовидної залози регулюється тиреотропним гормоном (ТТГ). Як показано на малюнку 2. (Класична петля негативного зворотного зв'язку), низький рівень T 3 і T 4 в крові стимулюють вивільнення тиреотропін-рилізинг-гормону (ТРГ) з гіпоталамуса, що запускає секрецію ТТГ з передньої частини гіпофіза. У свою чергу, ТТГ стимулює щитовидну залозу виділяти Т 3 і Т 4. Рівні ТРГ, ТТГ, Т 3 і Т 4 регулюються системою негативного зворотного зв'язку, в якій підвищуючі рівні Т 3 і Т 4 знижують вироблення і секрецію ТТГ.

Функції гормонів щитовидної залози
Гормони щитовидної залози, T 3 і T 4, часто називають метаболічними гормонами, оскільки їх рівні впливають на основний метаболізм організму, кількість енергії, що використовується організмом у спокої. Коли Т 3 і Т 4 зв'язуються з внутрішньоклітинними рецепторами, розташованими на мітохондріях, вони викликають збільшення розщеплення поживних речовин і використання кисню для вироблення АТФ. Крім того, Т 3 і Т 4 ініціюють транскрипцію генів, що беруть участь в окисленні глюкози. Хоча ці механізми спонукають клітини виробляти більше АТФ, процес неефективний, і аномально підвищений рівень тепла виділяється як побічний продукт цих реакцій. Це так званий калоригенний ефект (калорій- = «тепло») підвищує температуру тіла.
Адекватний рівень гормонів щитовидної залози також необхідний для синтезу білка, а також для розвитку та росту тканин плода та дитинства. Вони особливо критичні для нормального розвитку нервової системи як внутрішньоутробно, так і в ранньому дитячому віці, і продовжують підтримувати неврологічну функцію у дорослих. Як зазначалося раніше, ці гормони щитовидної залози мають складний взаємозв'язок з репродуктивними гормонами, а недоліки можуть впливати на лібідо, фертильність та інші аспекти репродуктивної функції. Нарешті, гормони щитовидної залози підвищують чутливість організму до катехоламінів (адреналіну та норадреналіну) з мозкового мозку надниркових залоз шляхом регуляції рецепторів в кровоносних судибах. При надмірному рівні гормонів Т 3 і Т 4 цей ефект прискорює частоту серцевих скорочень, підсилює серцебиття, підвищує артеріальний тиск. Оскільки гормони щитовидної залози регулюють обмін речовин, вироблення тепла, синтез білка та багато інших функцій організму, порушення щитовидної залози можуть мати важкі та поширені наслідки.
Ендокринна система: дефіцит йоду, гіпотиреоз та гіпертиреоз
Як обговорювалося вище, дієтичний йод необхідний для синтезу Т 3 і Т 4. Але для більшої частини населення світу продукти харчування не забезпечують належного рівня цього мінералу, оскільки кількість змінюється залежно від рівня ґрунту, в якому вирощувалася їжа, а також зрошення та використовувані добрива. Морська риба та креветки, як правило, мають високий рівень, оскільки вони концентрують йод з морської води, але багатьом людям у регіонах, що не мають виходу до моря, не вистачає доступу до морепродуктів. Таким чином, основним джерелом дієтичного йоду в багатьох країнах є йодована сіль. Зміцнення солі йодом почалося в США в 1924 році, і міжнародні зусилля з йодування солі в найбідніших країнах світу тривають і сьогодні.
Дієтичний дефіцит йоду може призвести до порушення здатності синтезувати Т 3 і Т 4, що призводить до безлічі важких порушень. Коли Т 3 і Т 4 не можуть бути вироблені, ТТГ виділяється у зростаючій кількості. В результаті такої гіперстимуляції тиреоглобулін накопичується в фолікулах щитовидної залози, збільшуючи їх відкладення колоїду. Накопичення колоїду збільшує загальний розмір щитовидної залози, стан називається зоб (рис. 3. Зоб). Зоб - це лише видима ознака дефіциту. Інші порушення дефіциту йоду включають порушення росту та розвитку, зниження фертильності та внутрішньоутробну та дитячу смерть. Крім того, йододефіцит є основною причиною попереджуваної розумової відсталості у всьому світі. Неонатальний гіпотиреоз (кретинізм) характеризується когнітивним дефіцитом, низьким зростанням, а іноді глухотою та глухотою у дітей та дорослих, народжених матерями, які мали дефіцит йоду під час вагітності.

У районах світу, що мають доступ до йодованої солі, дефіцит харчування зустрічається рідко. Натомість запалення щитовидної залози є більш поширеною причиною низького рівня гормонів щитовидної залози в крові. Називається гіпотиреозом, стан характеризується низькою швидкістю обміну речовин, збільшенням ваги, похолоданням кінцівок, запорами, зниженням лібідо, порушеннями менструального циклу та зниженням розумової активності. На відміну від цього, гіпертиреоз - аномально підвищений рівень гормонів щитовидної залози в крові - часто викликається пухлиною гіпофіза або щитовидної залози. При хворобі Грейвса гіперщитовидний стан виникає внаслідок аутоімунної реакції, при якій антитіла надмірно стимулюють клітини фолікула щитовидної залози. Гіпертиреоз може призвести до збільшення швидкості обміну речовин, надмірного тепла та потовиділення тіла, діареї, втрати ваги, тремору та збільшення частоти серцевих скорочень. Очі людини можуть випирати (звані екзофтальмом), оскільки антитіла виробляють запалення в м'яких тканині орбіт. У людини також може розвинутися зоб.
Кальцитонін
Щитовидна залоза також виділяє гормон, званий кальцитоніном, який виробляється парафолікулярними клітинами (також званими клітинами С), які стрижуть тканину між різними фолікулами. Кальцитонін виділяється у відповідь на підвищення рівня кальцію в крові. Здається, він має функцію зменшення концентрації кальцію в крові шляхом:
- Пригнічення активності остеокластів, кісткових клітин, які виділяють кальцій в кровообіг шляхом деградації кісткового матриксу
- Підвищення остеобластної активності
- Зниження всмоктування кальцію в кишечнику
- Збільшення втрати кальцію в сечі
Однак ці функції зазвичай не є значними для підтримки гомеостазу кальцію, тому важливість кальцитоніну не зовсім зрозуміла. Фармацевтичні препарати кальцитоніну іноді призначають для зниження активності остеокластів у людей з остеопорозом і для зменшення деградації хряща у людей з остеоартрозом. Гормони, що виділяються щитовидною залозою, зведені в таблиці (гормони щитовидної залози
| гормони щитовидної | ||
|---|---|---|
| супутні гормони | Хімічний клас | Ефект |
| Тироксин (Т 4), трийодтиронін (Т 3) | Амін | Стимулювати основний метаболізм |
| Кальцитонін | Пептид | Знижує рівень Ca 2+ в крові |
Звичайно, кальцій критичний для багатьох інших біологічних процесів. Це другий посланник у багатьох сигнальних шляхах і має важливе значення для скорочення м'язів, передачі нервових імпульсів та згортання крові. З огляду на ці ролі, не дивно, що рівень кальцію в крові жорстко регулюється ендокринною системою. Органи, що беруть участь в регуляції, - це паращитовидні залози.
Огляд глави
Щитовидна залоза являє собою орган у формі метелика, розташований в шиї спереду від трахеї. Його гормони регулюють основний обмін, використання кисню, обмін поживних речовин, вироблення АТФ, гомеостаз кальцію. Вони також сприяють синтезу білка і нормальному росту і розвитку тканин організму, включаючи дозрівання нервової системи, підвищують чутливість організму до катехоламінів. Гормони щитовидної залози трийодтиронін (Т 3) і тироксин (Т 4) виробляються і секретуються щитовидною залозою у відповідь на тиреотропний гормон (ТТГ) з передньої частини гіпофіза. Синтез амінокислот, отриманих гормонами T 3 і T 4, вимагає йоду. Недостатня кількість йоду в раціоні може привести до зоба, кретинізму і багатьох інших порушень.
паращитовидні залози
До кінця цього розділу ви зможете:
- Опишіть розташування і будову паращитовидних залоз
- Опишіть гормональний контроль рівня кальцію в крові
- Обговоріть фізіологічну реакцію дисфункції паращитовидної залози
Паращитовидні залози - це крихітні, круглі структури, які зазвичай виявляються вбудованими в задню поверхню щитовидної залози (рис. 1. Паращитовидні залози). Товста сполучнотканинна капсула відокремлює залози від тканини щитовидної залози. У більшості людей чотири паращитовидних залози, але зрідка їх більше в тканині шиї або грудної клітини. Функція одного типу паращитовидних клітин, оксіфільних клітин, не зрозуміла. Первинними функціональними клітинами паращитовидних залоз є головні клітини. Ці епітеліальні клітини виробляють і секретують паратиреоїдний гормон (ПТГ), основний гормон, який бере участь у регуляції рівня кальцію в крові.

Паращитовидні залози виробляють і виділяють ПТГ, пептидний гормон, у відповідь на низький рівень кальцію в крові (рис. Паратиреоїдний гормон у підтримці гомеостазу кальцію в крові). Секреція ПТГ викликає вивільнення кальцію з кісток шляхом стимуляції остеокластів, які виділяють ферменти, що руйнують кістку і виділяють кальцій в інтерстиціальну рідину. ПТГ також пригнічує остеобласти, клітини беруть участь у відкладенні кісток, тим самим щадячи в крові кальцій. ПТГ викликає підвищену реабсорбцію кальцію (і магнію) в ниркових канальцях з фільтрату сечі. Крім того, ПТГ ініціює вироблення стероїдного гормону кальцитріолу (також відомого як 1,25-дигідроксивітамін D), який є активною формою вітаміну D 3, в нирках. Кальцитріол потім стимулює підвищене всмоктування харчового кальцію кишечником. Петля негативного зворотного зв'язку регулює рівень ПТГ, при цьому підвищення рівня кальцію в крові гальмує подальше вивільнення ПТГ.

Аномально висока активність паращитовидної залози може спричинити гіперпаратиреоз - розлад, викликаний перевиробництвом ПТГ, що призводить до надмірної реабсорбції кальцію з кістки. Гіперпаратиреоз може значно знизити щільність кісткової тканини, приводячи до спонтанних переломів або деформацій. У міру підвищення рівня кальцію в крові проникність клітинної мембрани до натрію знижується, а чуйність нервової системи знижується. При цьому в тканині і органах організму можуть накопичуватися відкладення кальцію, погіршуючи їх функціонування.
На відміну від цього, аномально низький рівень кальцію в крові може бути викликаний дефіцитом паратиреоїдних гормонів, званим гіпопаратиреозом, який може розвинутися після травми або операції за участю щитовидної залози. Низький вміст кальцію в крові підвищує проникність мембрани до натрію, що призводить до посмикування м'язів, судоми, спазми або судоми. Важкий дефіцит може паралізувати м'язи, включаючи ті, що беруть участь у диханні, і може призвести до летального результату.
Коли рівень кальцію в крові високий, кальцитонін виробляється і секретується парафолікулярними клітинами щитовидної залози. Як обговорювалося раніше, кальцитонін пригнічує активність остеокластів, зменшує всмоктування харчового кальцію в кишечнику і сигналізує ниркам реабсорбувати менше кальцію, в результаті чого більша кількість кальцію виділяється з сечею.
Огляд глави
Кальцій необхідний для різних важливих фізіологічних процесів, включаючи нервово-м'язове функціонування; таким чином, рівень кальцію в крові тісно регулюється. Паращитовидні залози - це невеликі структури, розташовані на задній щитовидній залозі, які виробляють паращитовидний гормон (ПТГ), який регулює рівень кальцію в крові. Низький рівень кальцію в крові викликає вироблення і секрецію ПТГ. На відміну від цього, підвищений рівень кальцію в крові пригнічує секрецію ПТГ і запускає секрецію гормону щитовидної залози кальцитоніну. Недовиробництво ПТГ може призвести до гіпопаратиреозу. На відміну від цього, перевиробництво ПТГ може призвести до гіперпаратиреозу.
Надниркових залоз
До кінця цього розділу ви зможете:
- Опишіть розташування і будову надниркових залоз
- Визначте гормони, що виробляються корою надниркових залоз і мозком надниркових залоз, і узагальнити їх клітини-мішені та ефекти
Наднирники - це клини залізистої і нейроендокринної тканини, що прилягають до верхівки нирок фіброзною капсулою (рис. 1. Надниркових залоз). Наднирники мають багате кровопостачання і відчувають одну з найвищих показників кровотоку в організмі. Їх обслуговують кілька артерій, що розгалужуються від аорти, включаючи надниркову і ниркову артерії. Кров надходить до кожного наднирника в корі надниркових залоз, а потім стікає в мозок надниркових залоз. Гормони надниркових залоз виділяються в кровообіг через ліву і праву надниркові вени.

Наднирники складаються з зовнішньої кори залозистої тканини і внутрішнього мозку нервової тканини. Сама кора ділиться на три зони: клубочкову зону, фасцикулярну зону та сітчасту зону. Кожен регіон виділяє свій набір гормонів.
Кора надниркових залоз, як компонент осі гіпоталамо-гіпофізарно-надниркових залоз (ГПА), виділяє стероїдні гормони, важливі для регуляції тривалої реакції на стрес, артеріального тиску та об'єму крові, поглинання та зберігання поживних речовин, балансу рідини та електролітів та запалення. Вісь ГПА передбачає стимуляцію вивільнення гормону адренокортикотропного гормону (АКТГ) з гіпофіза гіпоталамусом. Потім АКТГ стимулює кору надниркових залоз виробляти гормон кортизол. Про цей шлях буде більш детально розказано нижче.
Мозок надниркових залоз - це нейроендокринна тканина, що складається з постгангліонарних нейронів симпатичної нервової системи (SNS). Це дійсно розширення вегетативної нервової системи, яка регулює гомеостаз в організмі. Симпатомедуллярний (SAM) шлях включає стимуляцію мозку імпульсами від гіпоталамуса через нейрони з грудного спинного мозку. Мозок стимулюється до виділення амінних гормонів адреналіну та норадреналіну.
Однією з основних функцій надниркових залоз є реагування на стрес. Стрес може бути як фізичним, так і психологічним, або і тим і іншим. Фізичні навантаження включають піддавання організму травмам, ходьбу на вулиці в холодних і вологих умовах без пальто або неправильне харчування. До психологічних навантажень відносять сприйняття фізичної загрози, бійку з коханою людиною або просто поганий день в школі.
Організм по-різному реагує на короткочасний стрес та довгостроковий стрес за схемою, відомою як синдром загальної адаптації (ГАЗ). Перша стадія ГАЗ називається тривожною реакцією. Це короткочасний стрес, реакція боротьби чи втечі, опосередкована гормонами адреналіну та норадреналіну з мозку надниркових залоз через шлях SAM. Їх функція полягає в підготовці організму до екстремальних фізичних навантажень. Як тільки цей стрес знімається, організм швидко приходить в норму. Розділ на мозковому мозку надниркових залоз охоплює цю відповідь більш детально.
Якщо стрес незабаром не знімається, організм пристосовується до стресу на другій стадії, яка називається стадією опору. Наприклад, якщо людина голодує, організм може посилати сигнали в шлунково-кишковий тракт, щоб максимально засвоювати поживні речовини з їжі.
Однак, якщо стрес триває довше, організм реагує симптомами, зовсім іншими, ніж реакція боротьби чи втечі. Під час стадії виснаження люди можуть почати страждати депресією, придушенням їх імунної відповіді, сильною втомою або навіть смертельним інфарктом. Ці симптоми опосередковані гормонами кори надниркових залоз, особливо кортизолом, що виділяються в результаті сигналів від осі ГПА.
Гормони надниркових залоз також мають кілька функцій, пов'язаних зі стресом, включаючи підвищення рівня натрію та глюкози в крові, які будуть детально описані нижче.
кора надниркових залоз
Кора надниркових залоз складається з декількох шарів клітин, що зберігають ліпіди, які відбуваються в трьох структурно різних областях. Кожен з цих регіонів виробляє різні гормони.
Гормони клубочків зони
Найбільш поверхневою областю кори надниркових залоз є зона гломерулози, яка виробляє групу гормонів, які спільно називають мінералокортикоїдами через їх вплив на мінерали організму, особливо натрій і калій. Ці гормони необхідні для рідинного і електролітного балансу.
Альдостерон є основним мінералокортикоїдом. Він важливий в регуляції концентрації іонів натрію і калію в сечі, поті, слині. Наприклад, він виділяється у відповідь на підвищений К + крові, низький рівень Na +, низький кров'яний тиск або низький об'єм крові. У відповідь альдостерон збільшує виведення К + і затримку Na +, що в свою чергу збільшує обсяг крові і артеріальний тиск. Його секреція спонукає, коли CRH з гіпоталамуса запускає вивільнення АКТГ з передньої частини гіпофіза.
Альдостерон також є ключовим компонентом ренін-ангіотензин-альдостеронової системи (РААС), в якій спеціалізовані клітини нирок виділяють фермент ренін у відповідь на низький об'єм крові або низький кров'яний тиск. Ренін потім каталізує перетворення білка крові ангіотензиногену, що виробляється печінкою, в гормон ангіотензин I. Ангіотензин I перетворюється в легенях в ангіотензин II ангіотензинперетворюючим ферментом (АПФ). Ангіотензин II виконує три основні функції:
- Ініціювання вазоконстрикції артеріол, зменшення кровотоку
- Стимулювання ниркових канальців для реабсорбції NaCl та води, збільшення об'єму крові
- Сигналізація кори надниркових залоз про виділення альдостерону, ефекти якого в подальшому сприяють затримці рідини, відновленню артеріального тиску і обсягу крові
Для осіб з гіпертонічною хворобою або високим кров'яним тиском доступні препарати, які блокують вироблення ангіотензину II. Ці препарати, відомі як інгібітори АПФ, блокують фермент АПФ від перетворення ангіотензину I в ангіотензин II, тим самим пом'якшуючи здатність останнього підвищувати артеріальний тиск.
Гормони зони фасцикулята
Проміжною областю кори надниркових залоз є zona fasciculata, названа як така, оскільки клітини утворюють невеликі пучки (пучки), розділені крихітними кровоносними судинами. Клітини зони фасцикуляти виробляють гормони, звані глюкокортикоїдами через їх роль в метаболізмі глюкози. Найважливішим з них є кортизол, деякі з яких печінка перетворюється в кортизон. Глюкокортикоїдом, що виробляється в значно менших кількостях, є кортикостеро У відповідь на тривалі стресові фактори гіпоталамус виділяє CRH, що, в свою чергу, запускає вивільнення АКТГ переднім гіпофізом. АКТГ запускає вивільнення глюкокортикоїдів. Їх загальний ефект полягає в інгібуванні побудови тканин, одночасно стимулюючи розпад збережених поживних речовин для підтримки достатніх запасів палива. В умовах тривалого стресу, наприклад, кортизол сприяє катаболізму глікогену до глюкози, катаболізму збережених тригліцеридів в жирні кислоти і гліцерин, катаболізму м'язових білків в амінокислоти. Потім ця сировина може бути використана для синтезу додаткової глюкози та кетонів для використання в якості палива для організму. Гіпокамп, який є частиною скроневої частки кори головного мозку і важливий у формуванні пам'яті, має високу чутливість до рівня стресу через безліч глюкокортикоїдних рецепторів.
Ви, мабуть, знайомі з рецептом та безрецептурними препаратами, що містять глюкокортикоїди, такими як ін'єкції кортизону в запалені суглоби, преднізонові таблетки та інгалятори на основі стероїдів, що використовуються для лікування важкої астми, та креми гідрокортизону, що застосовуються для полегшення сверблячих шкірних висипань. Ці препарати відображають ще одну роль кортизолу - зниження регуляції імунної системи, що гальмує запальну реакцію.
Гормони зони ретикуларіса
Найглибшою областю кори надниркових залоз є Zona reticularis, яка виробляє невелику кількість класу стероїдних статевих гормонів, званих андрогенами. У період статевого дозрівання і більшої частини дорослого життя андрогени виробляються в статевих залозах. Андрогени, що виробляються в зоні reticularis, доповнюють гонад андрогенів. Вони виробляються у відповідь на АКТГ з передньої частини гіпофіза і перетворюються в тканині в тестостерон або естрогени. У дорослих жінок вони можуть сприяти статевому потягу, але їх функція у дорослих чоловіків недостатньо вивчена. У жінок після менопаузи, у міру зниження функцій яєчників, основним джерелом естрогенів стають андрогени, що виробляються zona reticularis.
Мозок надниркових залоз
Як зазначалося раніше, кора надниркових залоз виділяє глюкокортикоїди у відповідь на тривалий стрес, такий як важке захворювання. Навпаки, мозок надниркових залоз виділяє свої гормони у відповідь на гострий короткочасний стрес, опосередкований симпатичною нервовою системою (СНС).
Медуллярна тканина складається з унікальних постгангліонових нейронів SNS, які називаються клітинами хромаффіну, які мають великі і неправильної форми, і виробляють нейромедіатори адреналін (також називається адреналіном) та норадреналін (або норадреналін). Адреналін виробляється у більшій кількості - приблизно 4 до 1 співвідношення з норадреналіном - і є більш потужним гормоном. Оскільки клітини хромаффіну виділяють адреналін та норадреналін у системний кровотік, де вони широко подорожують і впливають на віддалені клітини, вони вважаються гормонами. Похідні з амінокислоти тирозину, вони хімічно класифікуються як катехоламіни.
Секреція медуллярного адреналіну та норадреналіну контролюється нервовим шляхом, який походить від гіпоталамуса у відповідь на небезпеку або стрес (шлях SAM). І адреналін, і норадреналін сигналізують клітинам печінки та скелетних м'язів перетворювати глікоген в глюкозу, що призводить до підвищення рівня глюкози в крові. Ці гормони збільшують частоту серцевих скорочень, пульс та артеріальний тиск, щоб підготувати організм до боротьби зі сприйнятою загрозою або тікати від неї. Крім того, шлях розширює дихальні шляхи, підвищуючи рівень кисню в крові. Це також викликає розширення судин, ще більше збільшуючи оксигенацію важливих органів, таких як легені, мозок, серце та скелетні м'язи. У той же час він запускає звуження судин до судин, які обслуговують менш важливі органи, такі як шлунково-кишковий тракт, нирки та шкіра, і знижує регулювання деяких компонентів імунної системи. Інші ефекти включають сухість у роті, втрату апетиту, розширення зіниць та втрату периферичного зору. Основні гормони надниркових залоз зведені в табл. (Гормони надниркових залоз).
| Гормони надниркових залоз | |||
|---|---|---|---|
| Надниркових залоз | супутні гормони | Хімічний клас | Ефект |
| кора надниркових залоз | Альдостерон | Стероїдні | Підвищує рівень Na + в крові |
| кора надниркових залоз | Кортизол, кортикостерон, кортизон | Стероїдні | Підвищення рівня глюкози в крові |
| Мозок надниркових залоз | Адреналін, норадреналін | Амін | Стимулюйте реакцію бій чи втечу |
Розлади за участю надниркових залоз
Кілька порушень викликаються порушенням регуляції гормонів, що виробляються наднирковими залозами. Наприклад, хвороба Кушинга - це розлад, що характеризується високим рівнем глюкози в крові і накопиченням ліпідних відкладень на обличчі і шиї. Викликається гіперсекрецією кортизолу. Найпоширенішим джерелом хвороби Кушинга є пухлина гіпофіза, яка виділяє кортизол або АКТГ в аномально великих кількостях. Інші поширені ознаки хвороби Кушинга включають розвиток місяцеподібного обличчя, буйволиного горба на потилиці, швидке збільшення ваги та випадання волосся. Хронічно підвищений рівень глюкози також пов'язаний з підвищеним ризиком розвитку діабету 2 типу. Крім гіперглікемії, хронічно підвищені глюкокортикоїди порушують імунітет, стійкість до інфекції та пам'ять, і можуть призвести до швидкого набору ваги та випадання волосся.
На відміну від цього, гіпосекреція кортикостероїдів може призвести до хвороби Аддісона, рідкісного розладу, яке викликає низький рівень глюкози в крові та низький рівень натрію в крові. Ознаки та симптоми хвороби Аддісона розпливчасті і характерні для інших розладів, що ускладнює діагностику. Вони можуть включати загальну слабкість, біль у животі, втрату ваги, нудоту, блювоту, пітливість і тягу до солоної їжі.
Огляд глави
Надниркові залози, розташовані вище кожної нирки, складаються з двох областей: кори надниркових залоз і мозкового мозку надниркових залоз. Кора надниркових залоз - зовнішній шар залози - виробляє мінералокортикоїди, глюкокортикоїди та андрогени. Мозок надниркових залоз в ядрі залози виробляє адреналін і норадреналін.
Наднирники опосередковують короткочасну реакцію на стрес і довгострокову реакцію на стрес. Сприйнята загроза призводить до секреції адреналіну та норадреналіну з мозкового мозку надниркових залоз, які опосередковують відповідь «боротьба чи втеча». Тривала реакція на стрес опосередкована секрецією CRH з гіпоталамуса, який запускає АКТГ, що, в свою чергу, стимулює секрецію кортикостероїдів з кори надниркових залоз. Мінералокортикоїди, головним чином альдостерон, викликають затримку натрію та рідини, що збільшує об'єм крові та артеріальний тиск.
Шишкоподібна залоза
До кінця цього розділу ви зможете:
- Опишіть розташування і будову шишкоподібної залози
- Обговоріть функцію мелатоніну
Нагадаємо, що гіпоталамус, що входить до складу проміжного мозку, сидить нижнім і кілька переднім таламусом. Неповноцінним, але дещо заднім таламусом є шишкоподібна залоза, крихітна ендокринна залоза, функції якої не зовсім ясні. Відомо, що клітини пінеалоцитів, що складають шишкоподібну залозу, виробляють і виділяють амінний гормон мелатонін, який отримують з серотоніну.
Секреція мелатоніну змінюється залежно від рівня світла, отриманого з навколишнього середовища. Коли фотони світла стимулюють сітківки очей, нервовий імпульс направляється в область гіпоталамуса, звану супрахіазматичним ядром (СКН), що важливо в регуляції біологічних ритмів. Від СКН нервовий сигнал переноситься в спинний мозок і в кінцевому підсумку в шишкоподібну залозу, де гальмується вироблення мелатоніну. В результаті рівень мелатоніну в крові падає, сприяючи неспання. На відміну від цього, оскільки рівень світла знижується - наприклад, увечері, вироблення мелатоніну збільшується, підвищуючи рівень крові та викликаючи сонливість.
Виділення мелатоніну може впливати на циркадні ритми організму, темні світлові коливання, які впливають не тільки на сонливість і неспання, а й апетит і температуру тіла. Цікаво, що у дітей рівень мелатоніну вище, ніж у дорослих, що може перешкоджати вивільненню гонадотропінів з передньої частини гіпофіза, тим самим гальмуючи початок статевого дозрівання. Нарешті, антиоксидантна роль мелатоніну є предметом сучасних досліджень.
Реактивний відставання виникає, коли людина подорожує через кілька часових поясів і відчуває сонливість вдень або неспання вночі. Подорож через кілька часових поясів значно порушує світло-темний цикл, регульований мелатоніном. Для синтезу мелатоніну може знадобитися до декількох днів, щоб пристосуватися до світло-темних моделей у новому середовищі, що призводить до затримки струменя. Деякі повітряні мандрівники приймають добавки мелатоніну, щоб викликати сон.
Огляд глави
Шишкоподібна залоза являє собою ендокринну структуру проміжного мозку, і розташовується нижче і ззаду таламуса. Він складається з пінеалоцитів. Ці клітини виробляють і виділяють гормон мелатонін у відповідь на низький рівень освітленості. Високий рівень мелатоніну в крові викликає сонливість. Реактивний відставання, спричинений подорожами через кілька часових поясів, відбувається тому, що синтез мелатоніну займає кілька днів, щоб адаптуватися до світло-темних моделей у новому середовищі.
Гонад і плацентарні гормони
До кінця цього розділу ви зможете:
- Визначте найважливіші гормони, що виробляються яєчками та яєчниками
- Назвіть гормони, що виробляються плацентою, і станьте їх функції
У цьому розділі коротко обговорюється гормональна роль статевих залоз - чоловічих яєчок і жіночих яєчників - які виробляють статеві клітини (сперматозоїди та яйцеклітини) і виділяють гормони гонади. Ролі гонадотропінів, що виділяються з передньої гіпофіза (ФСГ і ЛГ), обговорювалися раніше.
Первинним гормоном, що виробляється чоловічими яєчками, є тестостерон, стероїдний гормон, важливий для розвитку чоловічої репродуктивної системи, дозрівання сперматозоїдів та розвитку чоловічих вторинних статевих ознак, таких як поглиблений голос, волосся на тілі та збільшення м'язової маси. Цікаво, що тестостерон виробляється і в жіночих яєчниках, але на значно зниженому рівні. Крім того, яєчка виробляють пептидний гормон інгібін, який пригнічує секрецію ФСГ з передньої частини гіпофіза. ФСГ стимулює сперматогенез.
Первинними гормонами, що виробляються яєчниками, є естрогени, до складу яких входять естрадіол, естріол, естрон. Естрогени відіграють важливу роль у більшій кількості фізіологічних процесів, включаючи розвиток жіночої репродуктивної системи, регуляцію менструального циклу, розвиток жіночих вторинних статевих ознак, таких як збільшення жирової тканини і розвиток тканини молочної залози, а також підтримання вагітності. Ще одним значним гормоном яєчників є прогестерон, який сприяє регуляції менструального циклу і важливий при підготовці організму до вагітності, а також підтримці вагітності. Крім того, гранульозні клітини фолікулів яєчників виробляють інгібін, який, як і у чоловіків, пригнічує секрецію ФСГ. На початкових етапах вагітності всередині матки розвивається орган під назвою плацента. Плацента постачає кисень і поживні речовини плоду, виводить продукти життєдіяльності, виробляє і виділяє естрогени і прогестерон. Плацента також виробляє хоріонічний гонадотропін людини (ХГЧ). Гормон ХГЧ сприяє синтезу прогестерону і знижує імунну функцію матері, щоб захистити плід від імунного відторгнення. Він також виділяє плацентарний лактоген людини (hPL), який відіграє певну роль у підготовці грудей до лактації, і релаксин, який, як вважають, допомагає пом'якшити та розширити лобковий симфіз під час підготовки до пологів. Гормони, що контролюють розмноження, зведені в таблиці (Репродуктивні гормони).
| Репродуктивні гормони | |||
|---|---|---|---|
| Гонад | супутні гормони | Хімічний клас | Ефект |
| яєчка | Тестостерон | Стероїдні | Стимулює розвиток чоловічих вторинних статевих ознак і вироблення сперми |
| яєчка | Інгібін | Протеїн | Пригнічує вивільнення ФСГ з гіпофіза |
| яєчники | Естрогени і прогестерон | Стероїдні | Стимулюють розвиток жіночих вторинних статевих ознак і готують організм до пологів |
| Плацента | Хоріонічний гонадотропін людини | Протеїн | Сприяє синтезу прогестерону під час вагітності та пригнічує імунну відповідь проти плоду |
Анаболічні стероїди
Ендокринна система може експлуатуватися в незаконних або неетичних цілях. Яскравим прикладом цього є використання стероїдних препаратів професійними спортсменами.
Зазвичай використовується для підвищення продуктивності, Анаболічні стероїди синтетичні версії чоловічого статевого гормону, тестостерону. Підвищуючи природний рівень цього гормону, спортсмени відчувають збільшення м'язової маси. Синтетичні версії людського гормону росту також використовуються для нарощування м'язової маси.
Використання препаратів підвищення продуктивності заборонено всіма основними колегіальними та професійними спортивними організаціями в Сполучених Штатах, оскільки вони надають несправедливу перевагу спортсменам, які приймають їх. Крім того, препарати можуть викликати значні і небезпечні побічні ефекти. Наприклад, анаболічний стероїд використання може підвищити рівень холестерину, підвищити кров'яний тиск, і пошкодити печінку. Змінений рівень тестостерону (як занадто низький, так і занадто високий) були причетні до спричинення структурних пошкоджень серця та збільшення ризику серцевих аритмій, серцевих нападів, застійної серцевої недостатності та раптової смерті. Парадоксально, стероїди можуть мати фемінізуючий ефект у чоловіків, у тому числі зморщені яєчка і збільшені тканини молочної залози. У жінок їх використання може викликати маскулінізуючі ефекти, такі як збільшений клітор і ріст волосся на обличчі. У обох статей їх використання може сприяти підвищеній агресії (широко відомої як «roid-rage»), депресії, порушенню сну, сильним акне та безпліддям.
Огляд глави
Чоловіча і жіноча репродуктивна система регулюється фолікулостимулюючим гормоном (ФСГ) і лютеїнізуючим гормоном (ЛГ), що виробляються передньою часткою гіпофіза у відповідь на гонадотропін-рилізинг гормон (ГнРГ) з гіпоталамуса. У чоловіків ФСГ стимулює дозрівання сперматозоїдів, яке гальмується гормоном інгібіном. Стероїдний гормон тестостерон, тип андрогену, виділяється у відповідь на ЛГ і відповідає за дозрівання і підтримку чоловічої статевої системи, а також розвиток чоловічих вторинних статевих ознак. У самок ФСГ сприяє дозріванню яйцеклітин, а ЛГ сигналізує про секрецію жіночих статевих гормонів, естрогенів і прогестерону. Обидва ці гормони важливі в розвитку і підтримці жіночої репродуктивної системи, а також підтримці вагітності. Плацента розвивається під час ранньої вагітності, і виділяє кілька гормонів, важливих для підтримки вагітності.
Ендокринна підшлункова
До кінця цього розділу ви зможете:
- Опишіть розташування та структуру підшлункової залози, а також морфологію та функцію острівців підшлункової залози
- Порівняйте та порівняйте функції інсуліну та глюкагону
Підшлункова залоза - це довгий стрункий орган, велика частина якого розташована ззаду від нижньої половини шлунка (рис. 1. Підшлункова залоза). Хоча це перш за все екзокринна залоза, що виділяє різноманітні травні ферменти, підшлункова залоза має ендокринну функцію. Її панкреатичні острівці - скупчення клітин, раніше відомі як острівці Лангерганса - секретують гормони глюкагон, інсулін, соматостатин та поліпептид підшлункової залози (PP).

Клітини та секреції панкреатичних острівців
Острівці підшлункової залози містять чотири різновиди клітин:
- Альфа-клітина виробляє гормон глюкагон і становить приблизно 20 відсотків кожного острівця. Глюкагон відіграє важливу роль у регуляції глюкози в крові; низький рівень глюкози в крові стимулює її вивільнення.
- Бета-клітина виробляє гормон інсулін і становить приблизно 75 відсотків кожного острівця. Підвищений рівень глюкози в крові стимулює викид інсуліну.
- Дельта-клітина становить чотири відсотки острівцевих клітин і виділяє пептидний гормон соматостатин. Нагадаємо, що соматостатин також виділяється гіпоталамусом (як GHIH), а шлунок і кишечник також виділяють його. Інгібуючий гормон, панкреатичний соматостатин пригнічує вивільнення як глюкагону, так і інсуліну.
- На клітинку РР припадає близько одного відсотка острівцевих клітин і виділяє поліпептидний гормон підшлункової залози. Вважається, що він відіграє певну роль у апетиті, а також у регуляції екзокринних та ендокринних виділень підшлункової залози. Поліпептид підшлункової залози, що виділяється після їжі, може зменшити подальше споживання їжі; однак він також виділяється у відповідь на голодування.
Регуляція рівня глюкози в крові інсуліном і глюкагоном
Глюкоза необхідна для клітинного дихання і є кращим паливом для всіх клітин організму. Організм отримує глюкозу від розщеплення вуглеводсодержащих продуктів і напоїв, які ми споживаємо. Глюкоза, яка не відразу засвоюється клітинами для палива, може зберігатися печінкою і м'язами у вигляді глікогену, або перетворюватися в тригліцериди і зберігатися в жировій тканині. Гормони регулюють як зберігання, так і утилізацію глюкози в міру необхідності. Рецептори, розташовані в підшлунковій залозі, відчувають рівень глюкози в крові, а згодом клітини підшлункової залози виділяють глюкагон або інсулін для підтримки нормального рівня.
глюкагон
Рецептори в підшлунковій залозі можуть відчувати зниження рівня глюкози в крові, наприклад, в періоди голодування або під час тривалих пологів або фізичних вправ (рис. Гомеостатична регуляція рівня глюкози в крові). У відповідь альфа-клітини підшлункової залози виділяють гормон глюкагон, який надає кілька ефектів:
- Він стимулює печінку перетворювати свої запаси глікогену назад в глюкозу. Ця відповідь відома як глікогеноліз. Потім глюкоза виділяється в циркуляцію для використання клітинами організму.
- Він стимулює печінку забирати амінокислоти з крові і перетворювати їх в глюкозу. Ця відповідь відома як глюконеогенез.
- Він стимулює ліполіз, розпад збережених тригліцеридів на вільні жирні кислоти і гліцерин. Частина вільного гліцерину, що виділяється в кров, подорожує до печінки, яка перетворює її в глюкозу. Це теж форма глюконеогенезу.
Вжиті разом ці дії підвищують рівень глюкози в крові. Активність глюкагону регулюється за допомогою механізму негативного зворотного зв'язку; підвищення рівня глюкози в крові гальмує подальше вироблення і секрецію глюкагону.

Інсулін
Основна функція інсуліну полягає в полегшенні поглинання глюкози в клітини організму. Еритроцити, а також клітини мозку, печінки, нирок і слизової оболонки тонкої кишки не мають інсулінових рецепторів на своїх клітинних мембранах і не вимагають інсуліну для поглинання глюкози. Хоча всі інші клітини організму потребують інсуліну, якщо вони мають приймати глюкозу з крові, клітини скелетних м'язів та жирові клітини є основними мішенями інсуліну.
Наявність їжі в кишечнику запускає вивільнення гормонів шлунково-кишкового тракту, таких як глюкозозалежний інсулінотропний пептид (раніше відомий як шлунковий інгібіторний пептид). Це, в свою чергу, початковий тригер вироблення та секреції інсуліну бета-клітинами підшлункової залози. Як тільки відбувається всмоктування поживних речовин, отриманий сплеск рівня глюкози в крові додатково стимулює секрецію інсуліну
Точно, як інсулін сприяє засвоєнню глюкози, не зовсім зрозуміло. Однак інсулін, як видається, активує рецептор тирозинкінази, викликаючи фосфорилювання багатьох субстратів всередині клітини. Ці численні біохімічні реакції сходяться, щоб підтримувати рух внутрішньоклітинних бульбашок, що містять фасилітаційні транспортери глюкози, до клітинної мембрани. За відсутності інсуліну ці транспортні білки зазвичай повільно переробляються між клітинною мембраною та внутрішньою частиною клітин. Інсулін запускає швидкий рух пулу бульбашок транспортера глюкози до клітинної мембрани, де вони зливаються і піддають переносники глюкози до позаклітинної рідини. Потім транспортери переміщують глюкозу шляхом полегшеної дифузії всередину клітини.
Інсулін також знижує рівень глюкози в крові, стимулюючи гліколіз, метаболізм глюкози для генерації АТФ. Більш того, він стимулює печінку перетворювати надлишок глюкози в глікоген для зберігання, і він пригнічує ферменти, що беруть участь в глікогенолізі і глюконеогенезі. Нарешті, інсулін сприяє синтезу тригліцеридів і білка. Секреція інсуліну регулюється за допомогою механізму негативного зворотного зв'язку. У міру зниження рівня глюкози в крові подальше вивільнення інсуліну гальмується. Гормони підшлункової залози зведені в табл. (Гормони підшлункової залози).
| Гормони підшлункової залози | ||
|---|---|---|
| супутні гормони | Хімічний клас | Ефект |
| Інсулін (бета-клітини) | Протеїн | Знижує рівень глюкози в крові |
| Глюкагон (альфа-клітини) | Протеїн | Підвищує рівень глюкози в крові |
| Соматостатин (дельта-клітини) | Протеїн | Пригнічує вивільнення інсуліну та глюкагону |
| Поліпептид підшлункової залози (РР клітини) | Протеїн | Роль в апетиті |
Ендокринна система: цукровий діабет
Дисфункція вироблення та секреції інсуліну, а також реакція цільових клітин на інсулін можуть призвести до стану, званого цукровим діабетом. Все частіше зустрічається захворювання, цукровий діабет діагностується у понад 18 мільйонів дорослих у США та понад 200 000 дітей. Підраховано, що до 7 мільйонів більше дорослих мають стан, але не були діагностовані. Крім того, приблизно 79 мільйонів людей у США, за оцінками, мають переддіабет - стан, при якому рівень глюкози в крові аномально високий, але ще недостатньо високий, щоб його можна було класифікувати як діабет.
Розрізняють дві основні форми цукрового діабету. Цукровий діабет 1 типу - аутоімунне захворювання, що вражає бета-клітини підшлункової залози. Визнано, що певні гени підвищують сприйнятливість. Бета-клітини людей з діабетом 1 типу не виробляють інсулін; таким чином, синтетичний інсулін необхідно вводити шляхом ін'єкцій або інфузій. На цю форму діабету припадає менше п'яти відсотків усіх випадків діабету.
Цукровий діабет 2 типу становить приблизно 95 відсотків усіх випадків. Він придбаний, і такі фактори способу життя, як неправильне харчування, бездіяльність та наявність переддіабету, значно збільшують ризик людини. Близько 80-90 відсотків людей з діабетом 2 типу мають зайву вагу або ожиріння. При діабеті 2 типу клітини стають стійкими до впливу інсуліну. У відповідь підшлункова залоза збільшує свою секрецію інсуліну, але з часом бета-клітини виснажуються. У багатьох випадках діабет 2 типу можна змінити помірною втратою ваги, регулярними фізичними навантаженнями та споживанням здорової дієти; однак, якщо рівень глюкози в крові неможливо контролювати, діабетик врешті-решт потребує інсуліну.
Два ранніх прояви діабету - надмірне сечовипускання і надмірна спрага. Вони демонструють, як поза контролем рівень глюкози в крові впливає на роботу нирок. Нирки відповідають за фільтрацію глюкози з крові. Надмірна глюкоза крові втягує воду в сечу, і в результаті людина усуває аномально велику кількість солодкої сечі. Використання води для розведення сечі залишає організм зневодненим, і тому людина незвично і постійно спрагне. Людина також може відчувати постійний голод, оскільки клітини організму не в змозі отримати доступ до глюкози в крові.
Згодом стійко високий рівень глюкози в крові травмує тканини по всьому організму, особливо кровоносних судин і нервів. Запалення і травмування оболонки артерій призводять до атеросклерозу і підвищеного ризику інфаркту та інсульту. Пошкодження мікроскопічних кровоносних судин нирки погіршує роботу нирок і може призвести до ниркової недостатності. Пошкодження кровоносних судин, які обслуговують очі, може привести до сліпоти. Пошкодження кровоносних судин також зменшує кровообіг кінцівок, тоді як пошкодження нервів призводить до втрати чутливості, яка називається нейропатією, особливо в руках і ногах. Разом ці зміни збільшують ризик травм, інфекції та загибелі тканин (некрозу), сприяючи високій частоті ампутацій пальця ноги, стопи та гомілки у людей з діабетом. Неконтрольований діабет також може призвести до небезпечної форми метаболічного ацидозу під назвою кетоацидоз. Позбавлені глюкози, клітини все частіше покладаються на жирові запаси для палива. Однак у стані дефіциту глюкози печінка змушена використовувати альтернативний шлях обміну ліпідів, що призводить до збільшення вироблення кетонових тіл (або кетонів), які є кислими. Нарощування кетонів у крові викликає кетоацидоз, який, якщо його не лікувати, може призвести до небезпечної для життя «діабетичної коми». Разом ці ускладнення роблять діабет сьомою провідною причиною смерті в Сполучених Штатах.
Діабет діагностується, коли лабораторні тести виявляють, що рівень глюкози в крові вище норми, стан називається гіперглікемією. Лікування цукрового діабету залежить від типу, тяжкості стану, здатності пацієнта вносити зміни в спосіб життя. Як зазначалося раніше, помірна втрата ваги, регулярні фізичні навантаження, вживання цілющої дієти здатні знизити рівень глюкози в крові. Деякі пацієнти з діабетом 2 типу можуть не в змозі контролювати своє захворювання за допомогою цих змін способу життя, і їм буде потрібно медикаментозне лікування. Історично склалося, що першою лінією лікування діабету 2 типу був інсулін. Досягнення досліджень призвели до альтернативних варіантів, включаючи ліки, що підсилюють функцію підшлункової залози.
Огляд глави
Підшлункова залоза має і екзокринну, і ендокринну функції. Типи клітин підшлункової залози включають альфа-клітини, які виробляють глюкагон; бета-клітини, які виробляють інсулін; дельта-клітини, які виробляють соматостатин; і РР-клітини, які виробляють поліпептид підшлункової залози. Інсулін і глюкагон беруть участь в регуляції метаболізму глюкози. Інсулін виробляється бета-клітинами у відповідь на високий рівень глюкози в крові. Він підсилює поглинання глюкози і утилізацію клітинами-мішенями, а також зберігання надлишку глюкози для подальшого використання. Дисфункція вироблення інсуліну або резистентності клітин-мішеней до впливу інсуліну викликає цукровий діабет, розлад, що характеризується високим рівнем глюкози в крові. Гормон глюкагон виробляється і секретується альфа-клітинами підшлункової залози у відповідь на низький рівень глюкози в крові. Глюкагон стимулює механізми, що підвищують рівень глюкози в крові, такі як катаболізм глікогену в глюкозу.
Органи з вторинними ендокринними функціями
До кінця цього розділу ви зможете:
- Визначте органи з вторинною ендокринною функцією, гормон, який вони виробляють, і його наслідки
У своєму вивченні анатомії та фізіології ви вже стикалися з декількома з багатьох органів тіла, які мають вторинні ендокринні функції. Тут ви дізнаєтеся про гормонопродукуючу діяльність серця, шлунково-кишкового тракту, нирок, скелета, жирової тканини, шкіри, вилочкової залози.
Серце
Коли організм відчуває збільшення обсягу крові або тиску, клітини стінки передсердь серця розтягуються. У відповідь спеціалізовані клітини в стінці передсердь виробляють і виділяють пептидний гормон передсердний натрійуретичний пептид (АНП). АНП сигналізує ниркам про зменшення реабсорбції натрію, тим самим зменшуючи кількість води, реабсорбованої з фільтрату сечі, і зменшуючи обсяг крові. Інші дії АНП включають пригнічення секреції реніну і ініціювання ренін-ангіотензин-альдостеронової системи (РААС) і вазодилатацію. Тому ANP сприяє зниженню артеріального тиску, обсягу крові та рівня натрію в крові.
шлунково-кишкового тракту
Ендокринні клітини шлунково-кишкового тракту розташовуються в слизовій оболонці шлунка і тонкого кишечника. Деякі з цих гормонів виділяються у відповідь на прийом їжі та допомогу в травленні. Прикладом гормону, що виділяється клітинами шлунка, є гастрин, пептидний гормон, що виділяється у відповідь на здуття шлунка, який стимулює вивільнення соляної кислоти. Секретин - пептидний гормон, що виділяється тонким кишечником, коли кислий хімус (частково перетравлена їжа і рідина) рухається зі шлунка. Він стимулює виділення бікарбонату з підшлункової залози, який буферує кислий хімус, і пригнічує подальшу секрецію соляної кислоти шлунком. Холецистокінін (ССК) - ще один пептидний гормон, що виділяється з тонкої кишки. Він сприяє секреції ферментів підшлункової залози і вивільненню жовчі з жовчного міхура, обидва з яких полегшують травлення. Інші гормони, що виробляються клітинами кишечника, допомагають метаболізму глюкози, наприклад, стимулюючи бета-клітини підшлункової залози до секреції інсуліну, зменшуючи секрецію глюкагону з альфа-клітин або підвищуючи чутливість клітин до інсуліну.
Нирки
Нирки беруть участь в декількох складних ендокринних шляхах і виробляють певні гормони. Зниження припливу крові до нирок стимулює їх до вивільнення ферменту реніну, запускаючи систему ренін-ангіотензин-альдостерону (РААС) та стимулюючи реабсорбцію натрію і води. Реабсорбція збільшує кровотік і артеріальний тиск. Нирки також відіграють певну роль у регулюванні рівня кальцію в крові за рахунок вироблення кальцитріолу з вітаміну D 3, який виділяється у відповідь на секрецію паратиреоїдного гормону (ПТГ). Крім того, нирки виробляють гормон еритропоетин (ЕПО) у відповідь на низький рівень кисню. ЕПО стимулює вироблення еритроцитів (еритроцитів) в кістковому мозку, тим самим збільшуючи доставку кисню до тканин. Можливо, ви чули про ЕПО як про препарат, що підвищує продуктивність (у синтетичній формі).
Скелет
Хоча кістка вже давно визнана мішенню для гормонів, лише недавно дослідники визнали, що сам скелет виробляє не менше двох гормонів. Фактор росту фібробластів 23 (FGF23) виробляється кістковими клітинами у відповідь на підвищення в крові рівня вітаміну D 3 або фосфату. Це запускає нирки, щоб пригнічувати утворення кальцитріолу з вітаміну D 3 і збільшити виведення фосфору. Остеокальцин, що виробляється остеобластами, стимулює бета-клітини підшлункової залози для збільшення вироблення інсуліну. Він також діє на периферичні тканини для підвищення їх чутливості до інсуліну та утилізації глюкози.
Жирова тканина
Жирова тканина виробляє і виділяє кілька гормонів, які беруть участь в ліпідному обміні і зберіганні. Одним з важливих прикладів є лептин, білок, що виробляється жировими клітинами, який циркулює в кількостях, прямо пропорційних рівню жиру в організмі. Лептин виділяється у відповідь на споживання їжі і діє шляхом зв'язування з нейронами мозку, які беруть участь у споживанні та витраті енергії. Зв'язування лептину виробляє відчуття ситості після їжі, тим самим знижуючи апетит. Також виявляється, що зв'язування лептину з рецепторами мозку запускає симпатичну нервову систему регулювати кістковий обмін, збільшуючи відкладення коркової кістки. Адипонектин - ще один гормон, синтезований жировими клітинами - здається, знижує клітинну резистентність до інсуліну та захищає кровоносні судини від запалення та атеросклерозу. Його рівні нижчі у людей, які страждають ожирінням, і зростають після втрати ваги.
Шкіра
Шкіра функціонує як ендокринний орган при виробленні неактивної форми вітаміну D 3, холекальциферолу. Коли холестерин, присутній в епідермісі, піддається впливу ультрафіолету, він перетворюється в холекальциферол, який потім потрапляє в кров. У печінці холекальциферол перетворюється на проміжний продукт, який подорожує до нирок і далі перетворюється в кальцитріол, активну форму вітаміну D 3. Вітамін D важливий у різних фізіологічних процесах, включаючи всмоктування кальцію в кишечнику і функції імунної системи. У деяких дослідженнях низький рівень вітаміну D був пов'язаний з підвищеним ризиком раку, важкої астми та розсіяного склерозу. Дефіцит вітаміну D у дітей викликає рахіт, а у дорослих - остеомаляцію, яка характеризується погіршенням кісткової тканини.
тимус
Вилочкова залоза - це орган імунної системи, який більший і активніший у дитинстві та ранньому дитинстві, і починає атрофуватися з віком. Його ендокринна функція - вироблення групи гормонів, званих тимозинами, які сприяють виробленню та диференціації Т-лімфоцитів, які є імунними клітинами. Хоча роль тимозинів ще недостатньо вивчена, зрозуміло, що вони сприяють імунній відповіді. Тимозини були виявлені в тканині, відмінних від вилочкової залози, і мають широкий спектр функцій, тому тимозини не можна строго класифікувати як тимічні гормони.
Печінка
Печінка відповідає за секрецію щонайменше чотирьох важливих гормонів або попередників гормонів: інсуліноподібного фактора росту (соматомедину), ангіотензиногену, тромбопоетину та гепсидину. Інсуліноподібний фактор росту-1 є негайним стимулом для росту в організмі, особливо кісток. Ангіотензиноген є попередником ангіотензину, згаданого раніше, який підвищує артеріальний тиск. Тромбопоетин стимулює вироблення тромбоцитів крові. Гепцидини блокують вивільнення заліза з клітин організму, допомагаючи регулювати гомеостаз заліза в наших рідинях організму. Основні гормони цих інших органів зведені в таблиці (Органи з вторинними ендокринними функціями та їх основні гормони).
| Органи з вторинними ендокринними функціями та їх основними гормонами | ||
|---|---|---|
| Орган | Основні гормони | Ефекти |
| Серце | Передсердний натрійуретичний пептид (АНП) | Зменшує об'єм крові, артеріальний тиск і концентрацію Na + |
| шлунково-кишкового тракту | Гастрин, секретин та холецистокінін | Сприяння перетравленню їжі та буферизації шлункових кислот |
| шлунково-кишкового тракту | Глюкозозалежний інсулінотропний пептид (GIP) і глюкагоноподібний пептид 1 (GLP-1) | Стимулюють бета-клітини підшлункової залози до виділення інсуліну |
| Нирки | Ренін | Стимулює вивільнення альдостерону |
| Нирки | Кальцитріол | Допомагає в абсорбції Са 2+ |
| Нирки | еритропоетин | Запускає утворення еритроцитів в кістковому мозку |
| Скелет | ФГФ23 | Пригнічує вироблення кальцитріолу і збільшує екскрецію фосфатів |
| Скелет | Остеокальцин | Підвищує вироблення інсуліну |
| Жирова тканина | Лептин | Сприяє ситості сигналів в мозку |
| Жирова тканина | Адипонектин | Знижує резистентність до ін |
| Шкіра | холекальциферол | Модифікований з утворенням вітаміну D |
| Тимус (та інші органи) | Тимозини | Крім усього іншого, допомагає у виробленні Т-лімфоцитів імунної системи. |
| Печінка | Інсуліноподібний фактор росту-1 | Стимулює тілесний ріст |
| Печінка | ангіотензиноген | Підвищує артеріальний тиск |
| Печінка | Тромбопоетин | Причини підвищення тромбоцитів |
| Печінка | Гепцидин | Блокує викид заліза в рідини організму |
Огляд глави
Деякі органи мають вторинну ендокринну функцію. Наприклад, стінки передсердь серця виробляють гормон передсердний натрійуретичний пептид (АНП), шлунково-кишковий тракт виробляє гормони гастрин, секретин і холецистокінін, які допомагають травленню, а нирки виробляють еритропоетин (ЕПО), який стимулює утворення еритроцитів. Навіть кістка, жирова тканина, шкіра мають вторинні ендокринні функції.
Розвиток і старіння ендокринної системи
До кінця цього розділу ви зможете:
- Опишіть ембріональні витоки ендокринної системи
- Обговорити вплив старіння на ендокринну систему
Ендокринна система виникає з усіх трьох зародкових зародкових шарів. Ендокринні залози, які виробляють стероїдні гормони, такі як статеві залози та кора надниркових залоз, виникають з мезодерми. Навпаки, ендокринні залози, що виникають з ентодерми та ектодерми, виробляють амін, пептид та білкові гормони. Гіпофіз виникає з двох різних областей ектодерми: передній гіпофіз виникає з оральної ектодерми, тоді як задній гіпофіз виникає з нервової ектодерми біля основи гіпоталамуса. Шишкоподібна залоза також виникає з ектодерми. Дві структури надниркових залоз виникають з двох різних зародкових шарів: кори надниркових залоз з мезодерми і мозку надниркових залоз з нервових клітин ектодерми. Ентодерма дає початок щитовидної і паращитовидної залоз, а також підшлункової залози і вилочкової залози.
У міру старіння організму відбуваються зміни, які впливають на ендокринну систему, іноді змінюючи виробництво, секрецію та катаболізм гормонів. Наприклад, структура передньої гіпофіза змінюється у міру зменшення васкуляризації і збільшення вмісту сполучної тканини зі збільшенням віку. Ця перебудова впливає на вироблення гормонів залози. Наприклад, кількість людського гормону росту, який виробляється зменшується з віком, в результаті чого зниження м'язової маси зазвичай спостерігається у літніх людей.
Наднирники також зазнають змін у міру старіння організму; у міру збільшення фіброзної тканини вироблення кортизолу та альдостерону зменшується. Цікаво, що вироблення та секреція адреналіну та норадреналіну залишаються нормальними протягом усього процесу старіння.
Відомим прикладом процесу старіння, що впливає на ендокринну залозу, є менопауза і зниження функції яєчників. Зі збільшенням віку яєчники зменшуються як в розмірах, так і в вазі і стають прогресивно менш чутливими до гонадотропінів. Це поступово викликає зниження рівня естрогену і прогестерону, що призводить до менопаузи і неможливості розмноження. Низький рівень естрогенів та прогестерону також пов'язаний з деякими захворювальними станами, такими як остеопороз, атеросклероз та гіперліпідемія, або аномальний рівень ліпідів у крові.
Рівень тестостерону також знижується з віком, стан називається андропауза (або вірупауза); однак, це зниження є набагато менш драматичним, ніж зниження естрогенів у жінок, і набагато більш поступовим, рідко впливає на виробництво сперми до глибокої старості. Хоча це означає, що чоловіки зберігають свою здатність до батька дітей десятиліттями довше, ніж жінки, кількість, якість та рухливість їх сперми часто зменшуються.
У міру старіння організму щитовидна залоза виробляє менше гормонів щитовидної залози, викликаючи поступове зниження швидкості основного обміну речовин. Нижча швидкість метаболізму зменшує вироблення тепла тіла і підвищує рівень жирових відкладень. Паратиреоїдні гормони, з іншого боку, збільшуються з віком. Це може бути через зниження рівня кальцію в їжі, викликаючи компенсаторне збільшення паратиреоїдного гормону. Однак підвищення рівня паратиреоїдних гормонів у поєднанні зі зниженням рівня кальцитоніну (та естрогенів у жінок) може призвести до остеопорозу, оскільки ПТГ стимулює демінералізацію кісток для підвищення рівня кальцію в крові. Зверніть увагу, що остеопороз часто зустрічається як у літніх чоловіків, так і у жінок.
Збільшення віку також впливає на метаболізм глюкози, оскільки рівень глюкози в крові зростає швидше і займає більше часу, щоб повернутися до норми у літніх людей. Крім того, підвищення непереносимості глюкози може відбуватися через поступове зниження чутливості до клітинного інсуліну. Майже 27 відсотків американців у віці 65 років і старше хворіють на діабет.
Огляд глави
Ендокринна система бере свій початок з усіх трьох зародкових шарів ембріона, включаючи ентодерму, ектодерму та мезодерму. Загалом, різні класи гормонів виникають з різних зародкових шарів. Старіння впливає на ендокринні залози, потенційно впливаючи на вироблення гормонів і секрецію, і може спричинити захворювання. Вироблення гормонів, таких як гормон росту людини, кортизол, альдостерон, статеві гормони та гормони щитовидної залози, зменшується з віком.
Ліцензія
Цей твір створено компанією OpenStax-CNX і ліцензовано на умовах Ліцензії Creative Commons Із Зазначенням Авторства 3.0. http://cnx.org/content/m46535/1.3/