14.4: Ентропія
- Page ID
- 74816
навчальні цілі
- Обчислити загальну зміну ентропії для системи в оборотному процесі
У цьому і наступних атомах ми будемо вивчати ентропію. Вивчаючи його, ми побачимо, що напрями, пов'язані з другим законом - наприклад, передача тепла від гарячого до холодного - пов'язані з тенденцією в природі до невпорядкованості систем і для того, щоб менше енергії було доступним для використання в якості роботи. Ентропія системи насправді може бути показана як міра її розладу та недоступності енергії для роботи.
Визначення ентропії
Ми можемо побачити, як визначається ентропія, згадуючи наше обговорення двигуна Карно. Ми зазначили, що для циклу Карно, а отже, і для будь-яких оборотних процесів, Q c/Q h =T с/T h. Перестановка термінів дає\(\mathrm{\frac{Q_c}{T_c}=\frac{Q_h}{T_h}}\) для будь-якого оборотного процесу. Q c і Q h - абсолютні значення тепловіддачі при температурах T c і T h відповідно. Це співвідношення Q/T визначається як зміна ентропії ΔS для оборотного процесу,
\[\mathrm{ΔS=(\dfrac{Q}{T})_{rev},}\]
де Q - тепловіддача, яка є позитивною для передачі тепла в і негативною для передачі тепла з, а T - абсолютна температура, при якій відбувається оборотний процес. Одиницею СІ для ентропії є джоулі на кельвін (J/K). Якщо температура змінюється під час процесу, то зазвичай хорошим наближенням (для невеликих змін температури) приймати T як середню температуру, уникаючи необхідності використовувати інтегральне числення для пошуку ΔS.
Визначення ΔS суворо справедливо лише для оборотних процесів, таких як використовується в двигуні Карно. Однак ми можемо знайти ΔS саме навіть для реальних, незворотних процесів. Причина полягає в тому, що ентропія S системи, як і внутрішня енергія U, залежить тільки від стану системи, а не від того, як вона досягла цієї умови. Ентропія - це власність держави. Таким чином, зміна ентропії ΔS системи між станом один і другий стан однакова незалежно від того, як відбувається зміна. Нам просто потрібно знайти або уявити оборотний процес, який переводить нас з першого стану в стан два і обчислити ΔS для цього процесу. Це буде зміна ентропії для будь-якого процесу, що переходить від стану першого до другого стану.

Зміна ентропії: Коли система переходить від стану першого до стану два, її ентропія змінюється на однакову величину ΔS, незалежно від того, чи йде гіпотетичний оборотний шлях або реальний незворотний шлях.
Приклад
Тепер давайте подивимося на зміну ентропії двигуна Карно і його теплових резервуарів за один повний цикл. Гарячий резервуар має втрату ентропії Δsh=−Q h /T h, тому що з нього відбувається тепловіддача (пам'ятайте, що при передачі тепла назовні, то Q має негативний знак). Холодний резервуар має коефіцієнт посилення ентропії ΔS c = Q с/T c, тому що в нього відбувається тепловіддача. (Ми припускаємо, що водойми досить великі, щоб їх температури були постійними.) Тому загальна зміна ентропії становить
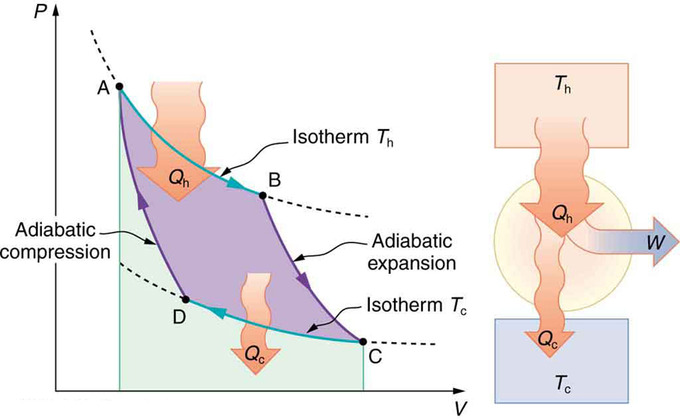
PV діаграма для циклу Карно: PV діаграма для циклу Карно, що використовує лише оборотні ізотермічні та адіабатичні процеси. Тепловіддача Qh відбувається в робочу речовину під час ізотермічного тракту АВ, який відбувається при постійній температурі Th. Тепловіддача Qc відбувається з робочої речовини під час ізотермічного тракту CD, який відбувається при постійній температурі Tc. Чистий робочий вихід W дорівнює площі всередині шляху ABCDA. Також показана схема двигуна Карно, що працює між гарячим і холодним резервуарами при температурах Th і Tc.
\[\mathrm{ΔS_{tot}=ΔS_h+ΔS_c.}\]
Таким чином, оскільки ми знаємо, що Q h/T h = Q c/T c для двигуна Карно,
\[\mathrm{ΔS_{tot}=−\dfrac{Q_h}{T_h}+\dfrac{Q_c}{T_c}=0.}\]
Цей результат, який має загальну обґрунтованість, означає, що загальна зміна ентропії для системи в будь-якому оборотному процесі дорівнює нулю.
Статична інтерпретація ентропії
Згідно з другим законом термодинаміки, розлад набагато частіше, ніж порядок.
навчальні цілі
- Розрахуйте кількість мікростанів для простих конфігурацій
Різні способи формулювання другого закону термодинаміки розповідають, що відбувається, а не чому це відбувається. Чому тепловіддача повинна відбуватися тільки від гарячого до холодного? Чому Всесвіт повинен ставати все більш безладним? Відповідь полягає в тому, що це питання величезної ймовірності. Розлад просто набагато більш імовірний, ніж порядок. Щоб проілюструвати цей факт, ми розглянемо деякі випадкові процеси, починаючи з підкидання монет.
Метання монет
Які можливі результати кидання 5 монет? На кожну монету можна посадити або голови, або хвости. У великих масштабах нас турбує лише загальна кількість орелів і хвостів, а не того порядку, в якому з'являються голови і хвости. Наступна таблиця показує всі можливості разом з номерами можливих конфігурацій (або мікростану; детальний опис кожного елемента системи). Наприклад, 4 голови та 1 екземпляр хвоста можуть зустрічатися на 5 різних конфігураціях, при цьому будь-яка з 5 монет показує хвіст, а всі інші голови. (ХХХХТ, ХХТХ, ХТХХ, ТХХХ)
- 5 голів, 0 хвостів: 1 мікростан
- 4 головки, 1 хвіст: 5 мікростанів
- 3 голови, 2 хвоста: 10 мікростанів
- 2 голови, 3 хвоста: 10 мікростанів
- 1 голова, 4 хвости: 5 мікростанів
- 0 голови, 5 хвостів: 1 мікростан
Зауважимо, що всі ці висновки ґрунтуються на вирішальному припущенні, що кожен мікростан однаково вірогідний. В іншому випадку аналіз буде помилковим.
Дві найбільш впорядковані можливості - 5 голів або 5 хвостів. (Вони більш структуровані, ніж інші.) Вони також найменш вірогідні, лише 2 з 32 можливостей. Найбільш безладними можливостями є 3 голови і 2 хвоста і його зворотний. (Вони найменш структуровані.) Найбільш безладні можливості також є найбільш імовірними, з 20 з 32 можливостей для 3 голів та 2 хвостів та їх зворотного. Якщо ми почнемо з впорядкованого масиву, як 5 голів, і кидаємо монети, дуже ймовірно, що в результаті ми отримаємо менш впорядкований масив, оскільки 30 з 32 можливостей менш впорядковані. Тож навіть якщо ви починаєте з упорядкованого стану, існує сильна тенденція переходити від порядку до розладу, від низької ентропії до високої ентропії. Зворотне може статися, але це малоймовірно.
Цей результат стає драматичним для великих систем. Розглянемо, що станеться, якщо у вас є 100 монет замість всього 5. Найбільш впорядковані домовленості (найбільш структуровані) - це 100 голів або 100 хвостів. Найменш впорядкований (найменш структурований) - це 50 голів і 50 хвостів. Існує лише 1 спосіб (1 мікростан), щоб отримати максимально впорядковане розташування з 100 голів. Загальна кількість різних способів 100 монет можуть бути кинуті - це вражаюче великий 1,27 × 10 30. Тепер, якщо ми почнемо з впорядкованого макродержави, як 100 голів, і кидаємо монети, є віртуальна впевненість, що ми отримаємо менш впорядкований макростан. Якщо ви кидали монети один раз в секунду, ви могли б очікувати отримати або 100 голів або 100 хвостів один раз в 2 × 10 22 років! На відміну від цього, є 8% шанс отримати 50 голів, 73% шанс отримати від 45 до 55 голів, і 96% шанс отримати від 40 до 60 голів. Розлад дуже імовірний.
Реальний газ
Фантастичне зростання шансів на користь розладу, який ми бачимо в переході від 5 до 100 монет триває, оскільки кількість суб'єктів у системі збільшується. В обсязі 1 м 3 в газі присутні приблизно 10 23 молекули (або на порядок числа Авогадро). Найбільш ймовірними умовами (або макростаном) для газу є ті, які ми бачимо весь час - випадковий розподіл атомів у просторі з розподілом швидкостей Максвелла-Больцмана у випадкових напрямках, як передбачено кінетичною теорією, як показано в (а). Це найбільш безладний і найменш структурований стан, який ми можемо собі уявити.
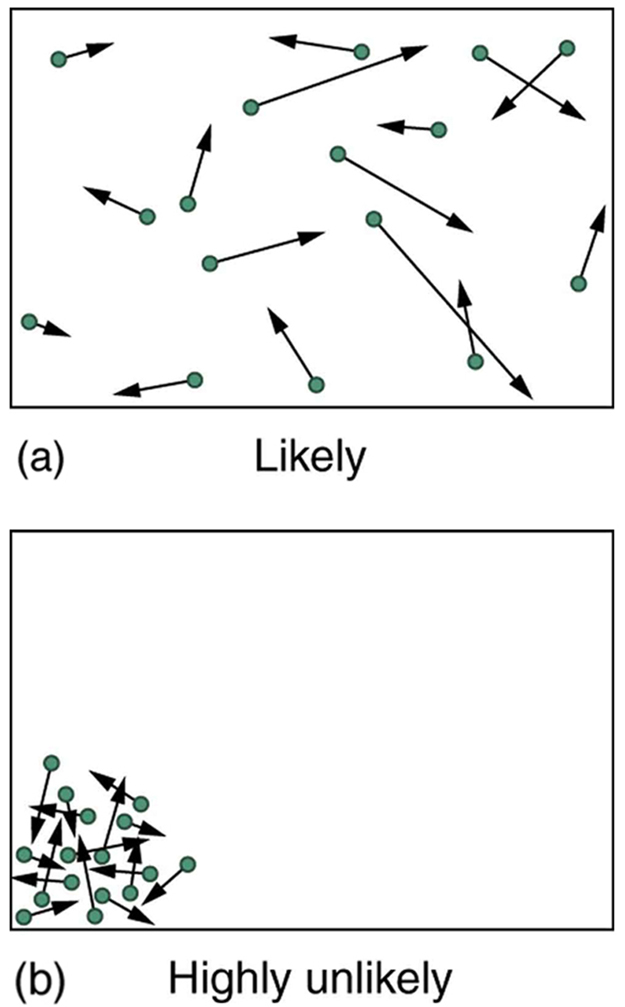
Кінетична теорія: (а) Звичайний стан газу в контейнері - це безладне, випадкове розподіл атомів або молекул з розподілом швидкостей Максвелла-Больцмана. Настільки малоймовірно, що ці атоми або молекули коли-небудь опиниться в одному куті контейнера, що це може бути неможливо. (б) При передачі енергії газ може бути змушений в один кут і його ентропія значно зменшується. Але залишившись в спокої, вона спонтанно збільшить свою ентропію і повернеться до нормальних умов, тому що вони безмірно більш імовірні.
На відміну від цього, один тип дуже впорядкованого і структурованого макростану має всі атоми в одному кутку контейнера з однаковими швидкостями. Існує дуже мало способів досягти цього (дуже мало мікростанів, відповідних йому), і тому це надзвичайно навряд чи коли-небудь відбудеться. (Див. (b).) Дійсно, настільки малоймовірно, що у нас є закон, який говорить про те, що це неможливо, який ніколи не спостерігалося порушувати—другий закон термодинаміки.
Наказ до розладу
Ентропія є мірою розладу, тому підвищена ентропія означає більше розладу в системі.
навчальні цілі
- Обговорити ентропію і розлад всередині системи
Ентропія - міра розладу. Це поняття спочатку постулював Людвіг Больцман в 1800-х роках. Наприклад, танення брили льоду означає прийняття високоструктурованої і впорядкованої системи молекул води і перетворення її в безладну рідину, в якій молекули не мають фіксованих положень. Відзначається велике збільшення ентропії в процесі.
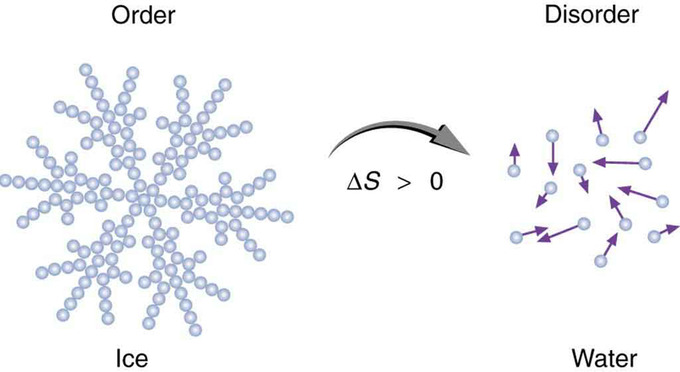
Ентропія льоду: Коли лід тане, він стає більш невпорядкованим і менш структурованим. Систематичне розташування молекул в кристалічній структурі замінюється більш випадковим і менш впорядкованим рухом молекул без фіксованих місць або орієнтацій. Його ентропія збільшується через те, що в нього відбувається тепловіддача. Ентропія - міра розладу.
Приклад\(\PageIndex{1}\):
Як приклад, припустимо, що ми змішуємо рівні маси води спочатку при двох різних температурах, скажімо, 20.0º C і 40.0º C. Результат - вода з проміжною температурою 30,0º С.
- Збільшилася ентропія.
- Деяка енергія стала недоступною для виконання роботи.
- Система стала менш впорядкованою.
Ентропія, енергія та розлад
Давайте подумаємо над кожним з результатів. По-перше, ентропія зросла з тієї ж причини, що і в наведеному вище прикладі. Змішування двох водойм має такий же ефект, як і тепловіддача від гарячого і така ж передача тепла в холодну. Змішування зменшує ентропію гарячої води, але збільшує ентропію холодної води на більшу кількість, виробляючи загальне збільшення ентропії.
По-друге, як тільки дві маси води змішуються, є тільки одна температура - ви не можете запустити з ними тепловий двигун. Енергія, яка могла бути використана для запуску теплового двигуна, тепер недоступна для роботи.
По-третє, суміш менш впорядкована, або використовувати інший термін, менш структурований. Замість того, щоб мати дві маси при різних температурах і з різним розподілом молекулярних швидкостей, ми тепер маємо єдину масу з рівномірною температурою.
Ці три результати - ентропія, недоступність енергії та розлад - не тільки пов'язані, але насправді є еквівалентними.
Тепло Смерть
Ентропія Всесвіту постійно збільшується і призначена для термодинамічної рівноваги, званої тепловою смертю Всесвіту.
навчальні цілі
- Опишіть процеси, що призводять до теплової загибелі Всесвіту
У ранньому, енергійному Всесвіті вся матерія і енергія були легко взаємозамінні і ідентичні за своєю природою. Гравітація зіграла життєво важливу роль у молодій Всесвіті. Хоча це, можливо, здавалося безладним, існувала величезна потенційна енергія для роботи - вся майбутня енергія у Всесвіті.
У міру дорослішання Всесвіту виникали перепади температур, які створювали більше можливостей для роботи. Зірки гарячіші, ніж планети, наприклад, які тепліші за крижані астероїди, які тепліше, ніж вакуум простору між ними. Більшість з них охолоджуються від їх зазвичай бурхливих пологів, в цей час вони були забезпечені власною енергією — ядерною енергією у випадку зірок, вулканічною енергією на Землі та інших планетах тощо. Без додаткового енергопостачання, однак, їх дні нумеруються.
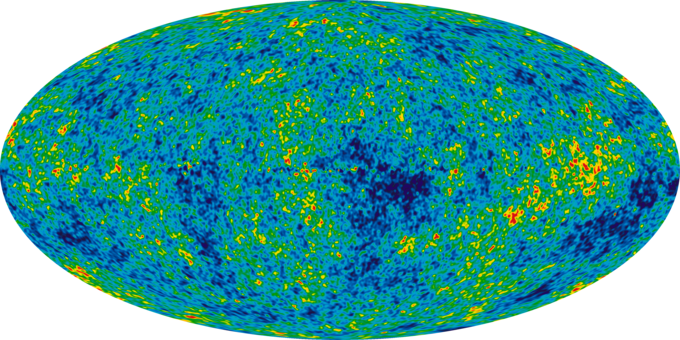
Всесвіт немовляти: Зображення дитячої всесвіту виявляє коливання температури (показані як колірні відмінності), які відповідають насінню, які виросли, щоб стати галактиками.
Зі збільшенням ентропії все менше енергії у Всесвіті є доступною для роботи. На Землі ми все ще маємо великі запаси енергії, такі як викопне та ядерне паливо; великомасштабні перепади температур, які можуть забезпечити енергію вітру; геотермальні енергії через різницю температур в шарах Землі; і приливні енергії завдяки великій кількості рідкої води. Оскільки вони використовуються, певна частка енергії, яку вони містять, ніколи не може бути перетворена на виконання роботи. Зрештою, все паливо буде вичерпано, всі температури вирівняються, і теплові двигуни не можуть функціонувати, або виконувати роботу буде неможливо.
Оскільки Всесвіт є замкнутою системою, то ентропія Всесвіту постійно збільшується, і тому доступність енергії для виконання роботи постійно зменшується. Врешті-решт, коли всі зірки померли, всі форми потенційної енергії були використані, і всі температури зрівнялися (залежно від маси Всесвіту, або при дуже високій температурі після загального скорочення, або дуже низькій, безпосередньо перед тим, як вся активність припиниться), можливості не буде виконання роботи.
Так чи інакше, Всесвіт призначений для термодинамічної рівноваги - максимальної ентропії. Це часто називають тепловою смертю Всесвіту, і буде означати закінчення всієї діяльності. Однак чи Всесвіт стискається і нагрівається, або продовжує розширюватися і охолоджуватися, кінець не близький. Розрахунки чорних дір говорять про те, що ентропія може легко тривати не менше 10 100 років.
Живі системи та еволюція
Можливо зниження ентропії однієї частини Всесвіту за умови збільшення повної зміни ентропії Всесвіту.
навчальні цілі
- Сформулюйте умови, що дозволяють знизити ентропію в одній частині Всесвіту
Деякі люди неправильно розуміють другий закон термодинаміки, заявлений з точки зору ентропії, щоб сказати, що процес еволюції життя порушує цей закон. Згодом складні організми еволюціонували від набагато простіших предків, представляючи собою велике зниження ентропії біосфери Землі. Це факт, що живі організми еволюціонували, щоб бути високоструктурованими і набагато нижчими за ентропією, ніж речовини, з яких вони ростуть. Але завжди можливо зниження ентропії однієї частини Всесвіту за умови збільшення повної зміни ентропії Всесвіту. У формі рівняння ми можемо записати це як
\[\mathrm{ΔS_{tot}=ΔS_{sys}+ΔS_{env}>0.}\]
Таким чином ΔS sys може бути негативним до тих пір, поки ΔS env є позитивним і більшим за величиною.
Як система може зменшити свою ентропію? Необхідна передача енергії. Якщо я збираю залізну руду з землі і перетворю її на сталь і будую міст, моя робота (і використана енергія) зменшила ентропію цієї системи. Енергія, що надходить від Сонця, може зменшити ентропію локальних систем на Землі - тобто ΔS sys є негативним. Але загальна ентропія решти Всесвіту збільшується на більшу величину - тобто ΔS env позитивний і більший за величиною. Таким чином, ΔS tot >0, а другий закон термодинаміки не порушується.
Кожен раз, коли завод зберігає деяку сонячну енергію у вигляді хімічної потенційної енергії, або висхідний потік теплого повітря піднімає ширяючу птицю, Землю можна розглядати як тепловий двигун, що працює між гарячим резервуаром, що постачається Сонцем, і холодним резервуаром, що постачається темним космічним простором - тепловим двигуном високої складності, спричиняючи локальне зниження ентропії, оскільки використовує частину теплопередачі від Сонця у глибокий космос. Однак спостерігається велике загальне збільшення ентропії в результаті цієї масивної тепловіддачі. Невелика частина цього теплообміну зберігається в структурованих системах на Землі, виробляючи набагато менші локальні зниження ентропії.
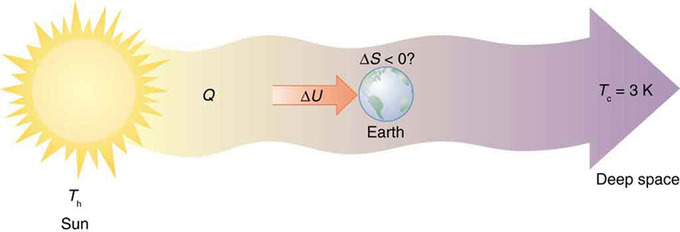
Ентропія Землі: Ентропія Землі може зменшуватися в процесі перехоплення невеликої частини теплопередачі від Сонця в глибокий космос. Ентропія для всього процесу значно збільшується, тоді як Земля стає більш структурованою з живими системами та накопиченою енергією в різних формах.
Переглянуто глобальне потепління
Другий закон термодинаміки може допомогти пояснити глобальне потепління за останні 250 років.
навчальні цілі
- Охарактеризуйте вплив тепла, що скидається в навколишнє середовище, на температуру атмосфери Землі
Другий закон термодинаміки може допомогти пояснити, чому за останні 250 років спостерігалося підвищення температури Землі (часто його називають «Глобальним потеплінням»), і багато професіоналів стурбовані тим, що збільшення ентропії Всесвіту є реальною загрозою для навколишнього середовища.

Глобальна температура суші та океану: Глобальна середня зміна температури суші та океану від 1880 - 2012 років відносно середнього значення 1951 - 1980. Чорна лінія - це середнє річне, а червона лінія - п'ятирічне середнє значення. Зелені смуги показують оцінки невизначеності.
Коли двигун працює, тепло надходить від теплового бака більшої температури до радіатора меншої температури. У перервах між цими станами тепловий потік перетворюється в корисну енергію за допомогою теплових двигунів. Однак, оскільки ці двигуни працюють, багато тепла втрачається в навколишнє середовище через неефективність. У двигуні Карно, який є найефективнішим теоретичним двигуном, заснованим на циклі Карно, максимальний ККД дорівнює одному мінус температурі радіатора (T c), поділеній на температуру джерела тепла (T h).
\[\mathrm{(Eff_c=1−\dfrac{T_c}{T_h}).}\]
Це співвідношення показує, що для досягнення більшої ефективності повинна бути найбільша різниця в температурі. Це викликає два важливих моменти: оптимізовані радіатори знаходяться на абсолютному нулі, і чим довше двигуни скидають тепло в ізольовану систему, тим менш ефективними стануть двигуни.
На жаль, для ефективності двигуна, повсякденне життя ніколи не працює в абсолютному нулі. У середньому двигуні автомобіля лише 14% до 26% палива, яке вкладається, фактично використовується для того, щоб автомобіль рухався вперед. Це означає, що від 74% до 86% втрачається тепло або використовується для живлення аксесуарів. За даними Міністерства енергетики США, від 70% до 72% тепла, що виробляється при спалюванні палива, - це тепло, втрачене двигуном. Зайве тепло, втрачене двигуном, потім виділяється в радіатор, який у випадку з багатьма сучасними двигунами був би атмосферою Землі. Оскільки більше тепла скидається в навколишнє середовище, температура атмосфери (або радіатора) Землі буде збільшуватися. З ентропією навколишнього середовища постійно зростає, пошук нових, більш ефективних технологій і нових нетеплових двигунів став пріоритетом.
Теплове забруднення
Теплове забруднення - це погіршення якості води будь-яким процесом, який змінює температуру води навколишнього середовища.
навчальні цілі
- Визначити фактори, що призводять до теплового забруднення та його екологічного впливу
Теплове забруднення - це погіршення якості води будь-яким процесом, який змінює температуру води навколишнього середовища. Частою причиною теплового забруднення є використання води в якості теплоносія, наприклад, електростанціями і промисловими виробниками. Коли вода, що використовується в якості теплоносія, повертається в природне середовище при більш високій температурі, зміна температури зменшує надходження кисню і впливає на склад екосистеми.
Як ми дізналися в нашому Atom на «Теплові двигуни», всі теплові двигуни вимагають теплопередачі, досягається шляхом забезпечення (і підтримки) різниці температур між джерелом тепла двигуна і радіатором. Вода, при своїй високій теплоємності, надзвичайно добре працює в якості теплоносія. Але це означає, що охолоджуюча вода повинна постійно поповнюватися для підтримки її охолоджуючої здатності.

Градирня: Це градирня на електростанції Gustav Knepper, Дортмунд, Німеччина. Охолоджуюча вода циркулює всередині вежі.
Екологічні ефекти
Підвищена температура води зазвичай знижує рівень розчиненого кисню води. Це може завдати шкоди водним тваринам, таким як риби, земноводні та інші водні організми. Підвищена швидкість метаболізму може призвести до меншої кількості ресурсів; більш адаптовані організми, що рухаються, можуть мати перевагу перед організмами, які не звикли до більш теплої температури. Як наслідок, харчові ланцюги старого та нового середовища можуть бути скомпрометовані. Деякі види риб уникають сегментів струмка або прибережних районів, прилеглих до теплового скиду. Біорізноманіття може зменшитися в результаті. Багато водних видів також не зможуть розмножуватися при підвищених температурах.
Деякі можуть припустити, що охолоджуючи нагріту воду, ми можемо виправити проблему теплового забруднення. Однак, як ми зазначали в нашому попередньому Atom на тему «Теплові насоси та холодильники», робота, необхідна для додаткового охолодження, призводить до більшого відводу тепла в навколишнє середовище. Тому це робить ситуацію ще гірше.
Ключові моменти
- Це співвідношення Q/T визначається як зміна ентропії ΔS для оборотного процесу: ΔS = (QT) RevΔs =( QT) reVΔs = (QT) rev.
- Ентропія - це власність держави. Тому зміна ентропії ΔS системи між двома станами однакова незалежно від того, як відбувається зміна.
- Загальна зміна ентропії для системи в будь-якому оборотному процесі дорівнює нулю.
- Кожен мікростан однаково вірогідний на прикладі кидання монети. Однак, як макростан, існує сильна тенденція до виникнення найбільш невпорядкованого стану.
- При киданні 100 монет, якщо монети кидаються один раз кожну секунду, ви могли б очікувати, щоб отримати або всі 100 голів або всі 100 хвостів один раз в 2 × 10 22 років.
- Молекули в газі слідують за розподілом швидкостей Максвелла-Больцмана у випадкових напрямках, що є найбільш безладним і найменш структурованим станом з усіх можливостей.
- Змішування двох систем може зменшити ентропію однієї системи, але збільшити ентропію іншої системи на більшу кількість, виробляючи загальне збільшення ентропії.
- Після змішування води при двох різних температурах енергія в системі, яка могла бути використана для запуску теплового двигуна, тепер недоступна для роботи. Також процес зробив всю систему більш менш структурованою.
- Ентропія, недоступність енергії та розлад не тільки пов'язані, але насправді по суті еквівалентні.
- У ранньому, енергійному Всесвіті вся матерія і енергія були легко взаємозамінні і ідентичні за своєю природою.
- Зі збільшенням ентропії все менше енергії у Всесвіті є доступною для роботи.
- Всесвіту призначена термодинамічна рівновага —максимальна ентропія. Це часто називають тепловою смертю Всесвіту, і буде означати закінчення всієї діяльності.
- Живі організми еволюціонували, щоб бути високоструктурованими і набагато нижчими за ентропією, ніж речовини, з яких вони ростуть.
- Система може зменшити її ентропію за умови збільшення повної зміни ентропії Всесвіту: ΔStot=ΔsSys+ΔSEnV>0ΔStot=ΔsSys+ΔSEnV>0.
- Землю можна розглядати як тепловий двигун, що працює між гарячим резервуаром, що постачається Сонцем, і холодним резервуаром, що постачається темним космічним простором.
- У міру роботи теплових двигунів багато тепла втрачається в навколишнє середовище через неефективність.
- Навіть в двигуні Карно, який є найефективнішим теоретичним двигуном, є тепловтрати, що визначаються співвідношенням температури двигуна і його навколишнього середовища.
- Оскільки більше тепла скидається в навколишнє середовище, температура атмосфери Землі буде збільшуватися.
- Всі теплові двигуни вимагають тепловіддачі, що досягається шляхом забезпечення (і підтримки) різниці температур між джерелом тепла двигуна і радіатором. Охолоджуюча вода зазвичай використовується для підтримки різниці температур.
- Підвищена температура води зазвичай знижує рівень розчиненого кисню води, впливаючи на склад екосистеми.
- Охолодження нагрітої води не є рішенням для термічного забруднення, оскільки для охолодження потрібна додаткова робота, що призводить до більшого вихлопу тепла в навколишнє середовище.
Ключові умови
- Цикл Карно: Теоретичний термодинамічний цикл. Це найефективніший цикл перетворення заданої кількості теплової енергії в роботу.
- оборотний: Здатний повернутися в початковий стан без споживання вільної енергії і збільшення ентропії.
- розлад: Відсутність деякої симетрії або кореляції в багаточастинковій системі.
- Розподіл Максвелла-Больцмана: Розподіл, що описує швидкості частинок в газах, де частинки вільно рухаються, не взаємодіючи один з одним, за винятком дуже коротких пружних зіткнень, в яких вони можуть обмінюватися імпульсом і кінетичною енергією.
- ентропія: Міра того, наскільки рівномірно розподіляється енергія (або якась аналогічна властивість) в системі.
- геотермальна: Відноситься до теплової енергії, що видобувається з водойм у надрах Землі.
- астероїд: природний твердий об'єкт, який менше планети і не комета, що обертається навколо зірки.
- Цикл Карно: Теоретичний термодинамічний цикл. Це найефективніший цикл перетворення заданої кількості теплової енергії в роботу.
- абсолютний нуль: найхолодніша можлива температура: нуль за шкалою Кельвіна і приблизно -273,15° C і -459.67° F Повна відсутність тепла; температура, при якій рух всіх молекул припиниться.
- тепловий двигун: Будь-який пристрій, який перетворює теплову енергію в механічну роботу.
- тепловий насос: пристрій, який передає тепло від чогось при більш низькій температурі до чогось при більш високій температурі, виконуючи роботу.
ЛІЦЕНЗІЇ ТА АВТОРСТВА
CC ЛІЦЕНЗОВАНИЙ КОНТЕНТ, РАНІШЕ ДІЛИВСЯ
- Курація та доопрацювання. Надано: Boundless.com. Ліцензія: CC BY-SA: Із Зазначенням Авторства
CC ЛІЦЕНЗОВАНИЙ ВМІСТ, СПЕЦИФІЧНА АТРИБУЦІЯ
- Коледж OpenStax, Коледж фізики. 17 вересня 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42237/latest...ol11406/latest. Ліцензія: CC BY: Зазначення авторства
- оборотний. Надано: Вікісловник. Розташований за адресою: uk.wiktionary.org/wiki/оборотний. Ліцензія: CC BY-SA: Із Зазначенням Авторства
- Цикл Карно. Надано: Вікіпедія. Розташований за адресою: uk.wikipedia.org/wiki/Carnot%20 Цикл. Ліцензія: CC BY-SA: Із Зазначенням Авторства
- Коледж OpenStax, Коледж фізики. 13 лютого 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42235/latest...ol11406/latest. Ліцензія: CC BY: Зазначення авторства
- Коледж OpenStax, Коледж фізики. 13 лютого 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42237/latest...ol11406/latest. Ліцензія: CC BY: Зазначення авторства
- Коледж OpenStax, Коледж фізики. 17 вересня 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42238/latest...ol11406/latest. Ліцензія: CC BY: Зазначення авторства
- Розподіл Максвелла Больцмана. Надано: Вікіпедія. Розташований за адресою: uk.wikipedia.org/wiki/Максвелл... 20 дистрибутив. Ліцензія: CC BY-SA: Із Зазначенням Авторства
- розлад. Надано: Вікіпедія. Розташовано за адресою: uk.wikipedia.org/Wiki/Розлад. Ліцензія: CC BY-SA: Із Зазначенням Авторства
- Коледж OpenStax, Коледж фізики. 13 лютого 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42235/latest...ol11406/latest. Ліцензія: CC BY: Зазначення авторства
- Коледж OpenStax, Коледж фізики. 13 лютого 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42237/latest...ol11406/latest. Ліцензія: CC BY: Зазначення авторства
- Коледж OpenStax, Коледж фізики. 13 лютого 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42238/latest...ol11406/latest. Ліцензія: CC BY: Зазначення авторства
- Коледж OpenStax, Коледж фізики. 17 вересня 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42237/latest...ol11406/latest. Ліцензія: CC BY: Зазначення авторства
- розлад. Надано: Вікіпедія. Розташовано за адресою: uk.wikipedia.org/Wiki/Розлад. Ліцензія: CC BY-SA: Із Зазначенням Авторства
- ентропія. Надано: Вікіпедія. Розташовано за адресою: uk.wikipedia.org/wiki/Ентропія. Ліцензія: CC BY-SA: Із Зазначенням Авторства
- Коледж OpenStax, Коледж фізики. 13 лютого 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42235/latest...ol11406/latest. Ліцензія: CC BY: Зазначення авторства
- Коледж OpenStax, Коледж фізики. 13 лютого 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42237/latest...ol11406/latest. Ліцензія: CC BY: Зазначення авторства
- Коледж OpenStax, Коледж фізики. 13 лютого 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42238/latest...ol11406/latest. Ліцензія: CC BY: Зазначення авторства
- Коледж OpenStax, Коледж фізики. 13 лютого 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42237/latest...ol11406/latest. Ліцензія: CC BY: Зазначення авторства
- Коледж OpenStax, Коледж фізики. 17 вересня 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42237/latest...ol11406/latest. Ліцензія: CC BY: Зазначення авторства
- ентропія. Надано: Вікіпедія. Розташовано за адресою: uk.wikipedia.org/wiki/Ентропія. Ліцензія: CC BY-SA: Із Зазначенням Авторства
- астероїд. Надано: Вікісловник. Розташований за адресою: uk.wiktionary.org/wiki/астероїд. Ліцензія: CC BY-SA: Із Зазначенням Авторства
- геотермальні. Надано: Вікісловник. Розташований за адресою: uk.wiktionary.org/wiki/геотермальна. Ліцензія: CC BY-SA: Із Зазначенням Авторства
- Коледж OpenStax, Коледж фізики. 13 лютого 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42235/latest...ol11406/latest. Ліцензія: CC BY: Зазначення авторства
- Коледж OpenStax, Коледж фізики. 13 лютого 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42237/latest...ol11406/latest. Ліцензія: CC BY: Зазначення авторства
- Коледж OpenStax, Коледж фізики. 13 лютого 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42238/latest...ol11406/latest. Ліцензія: CC BY: Зазначення авторства
- Коледж OpenStax, Коледж фізики. 13 лютого 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42237/latest...ol11406/latest. Ліцензія: CC BY: Зазначення авторства
- Тепло смерті Всесвіту. Надано: Вікіпедія. Розташований за адресою: uk.wikipedia.org/wiki/Heat_de... f_the_universe. Ліцензія: CC BY: Зазначення авторства
- Коледж OpenStax, Коледж фізики. 17 вересня 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42237/latest...ol11406/latest. Ліцензія: CC BY: Зазначення авторства
- ентропія. Надано: Вікіпедія. Розташовано за адресою: uk.wikipedia.org/wiki/Ентропія. Ліцензія: CC BY-SA: Із Зазначенням Авторства
- Коледж OpenStax, Коледж фізики. 13 лютого 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42235/latest...ol11406/latest. Ліцензія: CC BY: Зазначення авторства
- Коледж OpenStax, Коледж фізики. 13 лютого 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42237/latest...ol11406/latest. Ліцензія: CC BY: Зазначення авторства
- Коледж OpenStax, Коледж фізики. 13 лютого 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42238/latest...ol11406/latest. Ліцензія: CC BY: Зазначення авторства
- Коледж OpenStax, Коледж фізики. 13 лютого 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42237/latest...ol11406/latest. Ліцензія: CC BY: Зазначення авторства
- Тепло смерті Всесвіту. Надано: Вікіпедія. Розташований за адресою: uk.wikipedia.org/wiki/Heat_de... f_the_universe. Ліцензія: CC BY: Зазначення авторства
- Коледж OpenStax, Коледж фізики. 13 лютого 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42237/latest...ol11406/latest. Ліцензія: CC BY: Зазначення авторства
- абсолютний нуль. Надано: Вікісловник. Розташований за адресою: uk.wiktionary.org/wiki/absolute_zero. Ліцензія: CC BY-SA: Із Зазначенням Авторства
- Ентропія і навколишнє середовище. Надано: Вікіпедія. Розташований за адресою: uk.wikipedia.org/wiki/Ентропія... he_environment. Ліцензія: CC BY-SA: Із Зазначенням Авторства
- Цикл Карно. Надано: Вікіпедія. Розташований за адресою: uk.wikipedia.org/wiki/Carnot%20 Цикл. Ліцензія: CC BY-SA: Із Зазначенням Авторства
- Коледж OpenStax, Коледж фізики. 13 лютого 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42235/latest...ol11406/latest. Ліцензія: CC BY: Зазначення авторства
- Коледж OpenStax, Коледж фізики. 13 лютого 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42237/latest...ol11406/latest. Ліцензія: CC BY: Зазначення авторства
- Коледж OpenStax, Коледж фізики. 13 лютого 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42238/latest...ol11406/latest. Ліцензія: CC BY: Зазначення авторства
- Коледж OpenStax, Коледж фізики. 13 лютого 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42237/latest...ol11406/latest. Ліцензія: CC BY: Зазначення авторства
- Тепло смерті Всесвіту. Надано: Вікіпедія. Розташований за адресою: uk.wikipedia.org/wiki/Heat_de... f_the_universe. Ліцензія: CC BY: Зазначення авторства
- Коледж OpenStax, Коледж фізики. 13 лютого 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42237/latest...ol11406/latest. Ліцензія: CC BY: Зазначення авторства
- Глобальне потепління. Надано: Вікіпедія. Розташовано за адресою: uk.wikipedia.org/wiki/global_warming. Ліцензія: CC BY: Зазначення авторства
- Теплове забруднення. Надано: Вікіпедія. Розташовано за адресою: uk.wikipedia.org/wiki/Термальне забруднення. Ліцензія: CC BY-SA: Із Зазначенням Авторства
- тепловий двигун. Надано: Вікісловник. Розташований за адресою: uk.wiktionary.org/wiki/heat_engine. Ліцензія: CC BY-SA: Із Зазначенням Авторства
- тепловий насос. Надано: Вікісловник. Розташований за адресою: uk.wiktionary.org/wiki/heat_pump. Ліцензія: CC BY-SA: Із Зазначенням Авторства
- Коледж OpenStax, Коледж фізики. 13 лютого 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42235/latest...ol11406/latest. Ліцензія: CC BY: Зазначення авторства
- Коледж OpenStax, Коледж фізики. 13 лютого 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42237/latest...ol11406/latest. Ліцензія: CC BY: Зазначення авторства
- Коледж OpenStax, Коледж фізики. 13 лютого 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42238/latest...ol11406/latest. Ліцензія: CC BY: Зазначення авторства
- Коледж OpenStax, Коледж фізики. 13 лютого 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42237/latest...ol11406/latest. Ліцензія: CC BY: Зазначення авторства
- Тепло смерті Всесвіту. Надано: Вікіпедія. Розташований за адресою: uk.wikipedia.org/wiki/Heat_de... f_the_universe. Ліцензія: CC BY: Зазначення авторства
- Коледж OpenStax, Коледж фізики. 13 лютого 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42237/latest...ol11406/latest. Ліцензія: CC BY: Зазначення авторства
- Глобальне потепління. Надано: Вікіпедія. Розташовано за адресою: uk.wikipedia.org/wiki/global_warming. Ліцензія: CC BY: Зазначення авторства
- Теплове забруднення. Надано: Вікіпедія. Розташовано за адресою: uk.wikipedia.org/wiki/Термальне забруднення. Ліцензія: CC BY: Зазначення авторства
