13.1: Вступ
- Page ID
- 74870
цілі навчання
- Розрізняють три режими теплопередачі
Введення в тепло- і теплообмін
Енергія може існувати в багатьох формах і тепло є одним з найбільш інтригуючих. Тепло часто приховане, так як воно існує лише під час транзиту, і передається цілим рядом чітко різних методів. Теплопередача зачіпає кожен аспект нашого життя і допомагає нам зрозуміти, як функціонує Всесвіт. Це пояснює холод, який ми відчуваємо ясною вітряною ніччю, або чому ядро Землі ще не охололо. Цей модуль визначає та досліджує тепловіддачу, його ефекти та методи передачі тепла. Ці теми є фундаментальними, а також практичними, і часто будуть згадуватися в модулі попереду.
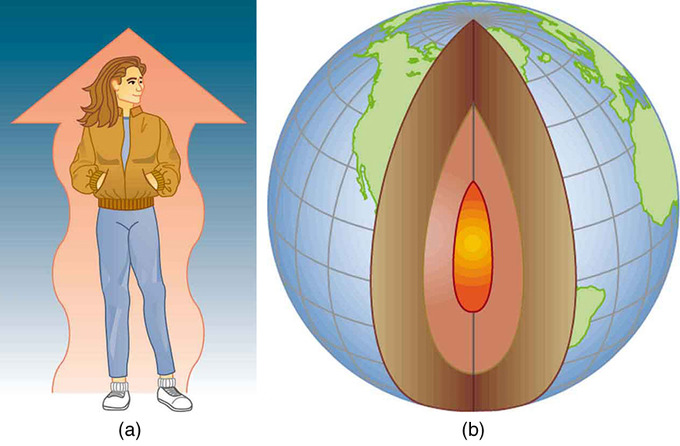
Приклади передачі тепла: (а) Охолоджуючий ефект ясної вітряної ночі виробляється вітром та радіаційною передачею тепла в холодний космічний простір. (б) Колись були великі суперечки щодо віку Землі, але зараз загальноприйнято мати близько 4,5 мільярдів років. Значна частина суперечок зосереджена на розплавлених надрах Землі. Згідно з нашим розумінням тепловіддачі, якщо Земля дійсно така стара, її центр давно повинен був охолонути. Відкриття радіоактивності в гірських породах виявило джерело енергії, що утримує надр Землі розплавленим, незважаючи на передачу тепла на поверхню, а звідти в холодний космічний простір.
Визначення
Шотландський фізик Джеймс Клерк Максвелл у своїй класичній теорії тепла 1871 року був одним з багатьох, хто почав спиратися на вже усталену ідею, що тепло - це щось спільне з матерією в русі. Це була та сама ідея, яку висунув сер Бенджамін Томпсон у 1798 році, який сказав, що він лише слідує за роботою багатьох інших. Однією з рекомендованих книг Максвелла була «Тепло як режим руху» Джона Тиндалла. Максвелл окреслив чотири положення для визначення теплоти:
- Це те, що може бути перенесено від одного тіла до іншого.
- Це вимірна величина, і, таким чином, розглядається математично.
- Його не можна розглядати як речовину, оскільки вона може бути перетворена на щось, що не є речовиною, наприклад, механічну роботу.
- Тепло - одна з форм енергії.
У наступних розділах ми будемо більш суворо визначати тепло, приділяючи особливу увагу тому, як його можна виміряти та кількісно оцінити.
Оцінка кількості теплоти
Кількість тепла, що передається деяким процесом, може бути або безпосередньо виміряно, або визначено побічно за допомогою розрахунків на основі інших величин. Пряме вимірювання здійснюється за допомогою калориметрії і є первинною емпіричною основою уявлення про кількість тепла, що передається в процесі. Передане тепло вимірюється змінами в тілі відомих властивостей, наприклад, підвищенням температури, зміною обсягу або довжини або зміною фази, наприклад, танення льоду. Непрямі оцінки кількості теплоти, що передається, спираються на закон збереження енергії, і, зокрема, на перший закон термодинаміки (досліджено в наступних розділах). Непряма оцінка є основним підходом багатьох теоретичних досліджень кількості теплоти, що передається.
Методи теплопередачі
Після визначення та кількісної оцінки тепловіддачі та його впливу на фізичні системи ми обговоримо методи, за допомогою яких здійснюється передача тепла. Так багато процесів передбачають тепловіддачу, так що важко уявити ситуацію, коли не відбувається тепловіддача. І все ж кожен процес, що передбачає передачу тепла, відбувається лише трьома методами:
- Провідність - це передача тепла через нерухому речовину фізичним контактом (речовина нерухома в макроскопічному масштабі - ми знаємо, що відбувається тепловий рух атомів і молекул при будь-якій температурі вище абсолютного нуля.) Тепло, що передається між електричним пальником печі і дном каструлі, є передається провідністю.
- Конвекція - це передача тепла макроскопічним рухом рідини. Цей вид перенесення відбувається в припливно-повітряної печі і в погодних системах, наприклад.
- Теплопередача випромінюванням відбувається при випромінюванні або поглинанні мікрохвиль, інфрачервоного випромінювання, видимого світла або іншої форми електромагнітного випромінювання. Очевидний приклад - потепління Землі Сонцем. Менш очевидний приклад - теплове випромінювання від людського організму.
Тепло як передача енергії
Тепло - це мимовільна передача енергії за рахунок різниці температур.
цілі навчання
- Визначте СІ та загальні одиниці теплової енергії
Тепло як передача енергії
Розглянемо два об'єкти при різних температурах, які зведені разом. Енергія передається від більш гарячого об'єкта до більш холодного, поки обидва об'єкти не досягнуть теплової рівноваги (тобто обидва стають однаковою температурою). Як передається ця енергія? Жодна робота не виконується жодним об'єктом, тому що ніяка сила не діє через відстань. Передача енергії викликана різницею температур, і припиняється, як тільки температури дорівнюють. Це спостереження призводить до наступного визначення тепла: Тепло - це мимовільна передача енергії за рахунок різниці температур.

Теплообмін і рівновага: (а) Безалкогольний напій і лід мають різні температури, T1 і T2, і не знаходяться в тепловій рівновазі. (б) Коли безалкогольному напою та льоду дозволяють взаємодіяти, енергія передається до тих пір, поки вони не досягнуть однакової температури T, досягаючи рівноваги. Тепловіддача відбувається за рахунок різниці температур. Насправді, оскільки безалкогольний напій і лід стикаються з навколишнім повітрям і лавкою, рівноважна температура буде однаковою для обох.
Де найбільше втрачається тепла? : Використовуйте рухливі термометри, щоб виявити, де будинок має погану ізоляцію.
Теплообмін: Короткий вступ до теплопередачі для студентів.
Тепло часто плутають з температурою. Наприклад, можна сказати, що спека була нестерпною, коли ми насправді маємо на увазі, що температура була високою. Тепло - це форма енергії, тоді як температура - ні. Помилка виникає тому, що ми чутливі до потоку тепла, а не до температури.
Одиниці
Завдяки тому, що тепло є формою енергії, воно має одиницю СІ джоуля (Дж). Калорія (кал) - це загальна одиниця енергії, визначена як енергія, необхідна для зміни температури 1,00 г води на 1,00° C - зокрема, між 14,5° C і 15,5° C, оскільки існує невелика залежність від температури. Ще однією поширеною одиницею тепла є кілокалорія (ккал), яка є енергією, необхідною для зміни температури 1,00 кг води на 1,00ºC. Оскільки маса часто вказується в кілограмах, зазвичай використовується кілокалорія. Харчові калорії (враховуючи позначення Cal, а іноді їх називають «великою калорією») насправді є кілокалоріями (1kilocalorie = 1000 калорій), що не легко визначити з маркування упаковки в Сполучених Штатах, але частіше зустрічається в Європі та в інших місцях. У деяких інженерних галузях широко використовується британська теплова одиниця (BTU), що дорівнює приблизно 1,055 кіло-джоулів.

Малюнок 1 Еквівалентність тепла та роботи: Схематичне зображення експерименту Джоуля, який встановив еквівалентність тепла та роботи
Загальна кількість енергії, що передається у вигляді тепла, умовно записується як Q для алгебраїчних цілей. Тепло, що виділяється системою в навколишнє середовище, за умовністю є негативною величиною (Q < 0); коли система поглинає тепло з оточення, воно є позитивним (Q > 0).
Механічний еквівалент тепла
Також можна змінювати температуру речовини, виконуючи роботу. Робота може передавати енергію в систему або з неї. Таке усвідомлення допомогло встановити той факт, що тепло є формою енергії. Джеймс Прескотт Джоуль (1818—1889) провів багато експериментів для встановлення механічного еквівалента тепла - роботи, необхідної для отримання тих же ефектів, що і теплопередача. З точки зору одиниць, використовуваних для цих двох термінів, найкращим сучасним значенням для цієї еквівалентності є 1.000 ккал = 4186 Дж. Ми розглядаємо це рівняння як перетворення між двома різними одиницями енергії.
На малюнку 1 показана одна з найвідоміших експериментальних установок Джоуля для демонстрації механічного еквівалента тепла. Це продемонструвало, що робота і тепло можуть виробляти однакові ефекти, і допомогло встановити принцип збереження енергії. Гравітаційна потенційна енергія (ПЕ) (робота, виконана гравітаційною силою) перетворюється в кінетичну енергію (КЕ), а потім рандомізується в'язкістю і турбулентністю в підвищену середню кінетичну енергію атомів і молекул в системі, виробляючи підвищення температури. Його внесок в область термодинаміки був настільки значним, що одиниця СІ енергії була названа його ім'ям.
Тепло, що додається або видаляється з системи, змінює її внутрішню енергію (концепцію ми обговоримо в наступному розділі) і, отже, її температуру. Таке підвищення температури спостерігається під час варіння. Однак додавання тепла не обов'язково підвищує температуру. Прикладом може служити танення льоду; тобто коли речовина змінюється з однієї фази на іншу. Робота, виконана над системою або системою, також може змінювати внутрішню енергію системи. Джоуль продемонстрував, що температуру системи можна збільшити за допомогою перемішування. Якщо кубик льоду натирається об шорстку поверхню, робота проводиться силою тертя. Система має чітко визначену внутрішню енергію, але ми не можемо сказати, що вона має певний «вміст тепла» або «вміст роботи». Використовуємо словосполучення «теплопередача», щоб підкреслити її природу.
Внутрішня енергія
Внутрішня енергія системи - це сума всієї кінетичної та потенційної енергії в системі.
цілі навчання
- Висловлюйте внутрішню енергію в терміні кінетичної та потенційної енергії
Внутрішня енергія
Джеймс Джоуль показав, що і тепло, і робота можуть виробляти однакову зміну внутрішньої енергії речовини, встановлюючи принцип механічної еквівалентності тепла. Тепло - це величина, яка виключно описує енергію, що передається. Немає сенсу говорити про загальне «тепло», яке містить об'єкт або система. Однак система містить кількісну кількість енергії, яка називається внутрішньою енергією системи. Внутрішня енергія системи - це величина, яка змінюється з додаванням або відніманням роботи або тепла. Вона тісно пов'язана з температурою.
Визначення
Внутрішня енергія - це енергія, необхідна для створення системи, виключаючи енергію, необхідну для витіснення її оточення. Внутрішня енергія має дві складові: кінетичну енергію і потенційну енергію. Кінетична енергія складається з усієї енергії, що включає рухи частинок, що складають систему, включаючи трансляцію, вібрацію та обертання. Потенційна енергія пов'язана зі статичними складовими речовини, статичною електричною енергією атомів всередині молекул або кристалів та енергією з хімічних зв'язків. Рівняння, що описує загальну внутрішню енергію системи, є таким чином:
\[\mathrm{U=U_{kinetic}+U_{potential}.}\]
Ми також можемо думати про внутрішню енергію як про суму всіх енергетичних станів кожного компонента в системі:
\[\mathrm{U=∑_iE_i.}\]
При будь-якій кінцевій температурі кінетична і потенційна енергії постійно перетворюються один в одного, але загальна енергія залишається постійною в ізольованій системі. Кінетична енергетична частина внутрішньої енергії дає підвищення температури системи. Ми можемо використовувати статистичну механіку, щоб пов'язати (дещо) випадкові рухи частинок у системі із середньою кінетичною енергією ансамблю частинок, і, таким чином, емпірично виміряною величиною, вираженою як температура.
Ми бачимо, що внутрішня енергія - це велика властивість: вона залежить від розмірів системи або від кількості речовини, яке вона містить.
У більшості випадків нас не хвилює сумарна кількість внутрішньої енергії в системі, так як рідко буває зручно або необхідно розглядати всі енергії, що належать системі. Швидше, нас набагато більше цікавить зміна внутрішньої енергії, враховуючи деяку передачу роботи або тепла. Це може виражатися у вигляді:
\[\mathrm{ΔU=Q+W_{mech}+W_{other}.}\]
Q - це тепло, що додається до системи, а W mech - це механічна робота, що виконується оточенням через зміни тиску або обсягу в системі. Всі інші збурення та енергії, додані іншими процесами, такими як електричний струм, введений в електронну схему, підсумовуються як термін W extra.
Малу зміну внутрішньої енергії системи можна обчислити, враховуючи нескінченно малу кількість тепла ΔQ, що додається до системи мінус нескінченно малий обсяг роботи ΔW, виконаної системою:
\[\mathrm{dU=δQ−δW.}\]
Цей вислів є першим законом термодинаміки.

Сонце і внутрішня енергія: Ядерний синтез на сонці перетворює ядерну потенційну енергію в наявну внутрішню енергію і підтримує температуру Сонця дуже високою.
Ключові моменти
- Тепло - найважливіша концепція, яка торкається кожного аспекту нашого життя. Джеймс Клерк Максвелл встановив важливі принципи, які поєднуються у визначенні тепла.
- Кількість теплопередачі може бути прямо виміряна або оцінена побічно через науку калориметрії.
- Існує три режими теплопередачі: провідність, конвекція і випромінювання.
- Якщо два об'єкти різної температури зведені разом, енергія буде передаватися від більш гарячого об'єкта до більш холодного, поки обидва не будуть мати однакову температуру. Ця передача енергії відома як тепло.
- Тепло не слід плутати з температурою. Температура описує внутрішній стан об'єкта, тоді як тепло відноситься до енергії, що передається об'єкту або від нього.
- Оскільки тепло є формою енергії, його одиницею СІ є джоуль. Інші загальні одиниці теплової енергії включають калорійність і кілокалорію, рівні 4,186 і 4,186 джоулів відповідно.
- Оскільки тепло і робота пов'язані з передачею енергії, кожен з них може виробляти однакові ефекти. Поняття механічного еквівалента тепла зіграло важливу роль у встановленні принципу збереження енергії.
- Хоча система не містить «тепла», вона містить загальну кількість енергії, яка називається внутрішньою енергією.
- Внутрішня енергія - це енергія, необхідна для створення системи, мінус енергія, необхідна для витіснення її оточення.
- Більшу частину часу нас цікавить зміна внутрішньої енергії, а не загальної внутрішньої енергії.
- Перший закон термодинаміки\(\mathrm{dU=ΔQ−ΔW}\), описує невеликі зміни внутрішньої енергії.
Ключові умови
- теплопередача: Передача теплової енергії за допомогою провідності, конвекції або випромінювання.
- калориметрія: Наука вимірювання тепла, поглиненого або еволюціонуючого в ході хімічної реакції або зміни стану.
- кілокалорія: одиниця енергії, що не є SI, рівна 1000 калорій або 4,186 джоулів; дорівнює «калорійності» або «калорії», використовуваної в харчовому маркуванні. Символ: ккал.
- теплова рівновага: Дві системи знаходяться в тепловій рівновазі, якщо вони можуть передавати тепло між собою, але ні.
- механічний еквівалент тепла: Робота, необхідна для отримання тих же ефектів, що і теплопередача.
- внутрішня енергія: Сума всієї енергії, присутньої в системі, включаючи кінетичну та потенційну енергію; еквівалентно, енергія, необхідна для створення системи, виключаючи енергію, необхідну для витіснення її оточення.
- ізольована система: система, яка не взаємодіє зі своїм оточенням, тобто її загальна енергія та маса залишаються постійними.
ЛІЦЕНЗІЇ ТА АВТОРСТВА
CC ЛІЦЕНЗОВАНИЙ КОНТЕНТ, РАНІШЕ ДІЛИВСЯ
- Курація та доопрацювання. Надано: Boundless.com. Ліцензія: CC BY-SA: Із Зазначенням Авторства
CC ЛІЦЕНЗОВАНИЙ ВМІСТ, СПЕЦИФІЧНА АТРИБУЦІЯ
- Коледж OpenStax, Коледж фізики. 17 вересня 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42226/latest/?collection=col11406/1.7. Ліцензія: CC BY: Зазначення авторства
- Коледж OpenStax, Коледж фізики. 17 вересня 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42226/latest/?collection=col11406/1.7. Ліцензія: CC BY: Зазначення авторства
- Коледж OpenStax, Коледж фізики. 17 вересня 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42221/latest/?collection=col11406/1.7. Ліцензія: CC BY: Зазначення авторства
- Коледж OpenStax, Коледж фізики. 17 вересня 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42223/latest/?collection=col11406/1.7. Ліцензія: CC BY: Зазначення авторства
- Тепло. Надано: Вікіпедія. Розташовано за адресою: uk.wikipedia.org/wiki/Heat. Ліцензія: CC BY-SA: Із Зазначенням Авторства
- калориметрія. Надано: Вікісловник. Розташований за адресою: uk.wiktionary.org/wiki/калориметрія. Ліцензія: CC BY-SA: Із Зазначенням Авторства
- тепловіддача. Надано: Вікісловник. Розташований за адресою: uk.wiktionary.org/wiki/heat_transfer. Ліцензія: CC BY-SA: Із Зазначенням Авторства
- Коледж OpenStax, Коледж фізики. 15 жовтня 2012 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42221/latest/?collection=col11406/1.7. Ліцензія: CC BY: Зазначення авторства
- Коледж OpenStax, Коледж фізики. 18 вересня 2013 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42223/latest/?collection=col11406/1.7. Ліцензія: CC BY: Зазначення авторства
- Тепло. Надано: Вікіпедія. Розташовано за адресою: uk.wikipedia.org/wiki/Heat. Ліцензія: CC BY-SA: Із Зазначенням Авторства
- Безмежний. Надано: Безмежне навчання. Розташований за адресою: www.boundless.com//фізика/визначення/теплова рівновага - 2. Ліцензія: CC BY-SA: Із Зазначенням Авторства
- Безмежний. Надано: Безмежне навчання. Розташований за адресою: www.boundless.com//physics/визначення/механічний еквівалент-тепла. Ліцензія: CC BY-SA: Із Зазначенням Авторства
- кілокалорія. Надано: Вікісловник. Розташований за адресою: uk.wiktionary.org/wiki/кілокалорія. Ліцензія: CC BY-SA: Із Зазначенням Авторства
- Коледж OpenStax, Коледж фізики. 15 жовтня 2012 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42221/latest/?collection=col11406/1.7. Ліцензія: CC BY: Зазначення авторства
- Теплообмін. Знаходиться за адресою: http://www.youtube.com/watch?v=pEBwctL490M. Ліцензія: Суспільне надбання: Немає відомих авторських прав. Умови ліцензії: Стандартна ліцензія YouTube
- Коледж OpenStax, Коледж фізики. 13 жовтня 2012 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42223/latest/?collection=col11406/1.7. Ліцензія: CC BY: Зазначення авторства
- Коледж OpenStax, Коледж фізики. 13 жовтня 2012 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42223/latest/?collection=col11406/1.7. Ліцензія: CC BY: Зазначення авторства
- Внутрішня енергія. Надано: Вікіпедія. Знаходиться за адресою: http://en.Wikipedia.org/wiki/Internal_energy. Ліцензія: CC BY-SA: Із Зазначенням Авторства
- Безмежний. Надано: Безмежне навчання. Розташований за адресою: www.boundless.com//physic/визначення/внутрішня енергія. Ліцензія: CC BY-SA: Із Зазначенням Авторства
- ізольована система. Надано: Вікісловник. Розташований за адресою: uk.wiktionary.org/wiki/isolated_system. Ліцензія: CC BY-SA: Із Зазначенням Авторства
- Коледж OpenStax, Коледж фізики. 15 жовтня 2012 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42221/latest/?collection=col11406/1.7. Ліцензія: CC BY: Зазначення авторства
- Теплообмін. Знаходиться за адресою: http://www.youtube.com/watch?v=pEBwctL490M. Ліцензія: Суспільне надбання: Немає відомих авторських прав. Умови ліцензії: Стандартна ліцензія YouTube
- Коледж OpenStax, Коледж фізики. 13 жовтня 2012 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42223/latest/?collection=col11406/1.7. Ліцензія: CC BY: Зазначення авторства
- Коледж OpenStax, Коледж фізики. 13 жовтня 2012 року. Надається: OpenSTAX CNX. Знаходиться за адресою: http://cnx.org/content/m42223/latest/?collection=col11406/1.7. Ліцензія: CC BY: Зазначення авторства
- Тепло. Надано: Вікіпедія. Розташовано за адресою: uk.wikipedia.org/wiki/Heat. Ліцензія: Суспільне надбання: Немає відомих авторських прав
