19.3: Робота та тепло не є державними функціями
- Page ID
- 26672
Тепло і робота - це функції шляху
Heat (\(q\)) і work (\(w\)) - це функції шляху, а не функції стану:
- Вони залежні від шляху.
- Вони є передачею енергії → вони не властиві системі.
Функції, які залежать від пройденого шляху, такі як work (\(w\)) та теплота (\(q\)), називаються функціями шляху.
Реверсивний проти незворотних
Розглянемо поршень, який стискається при постійній температурі (ізотермічний) до половини його початкового об'єму:
- Почніть з балона 1 літр, як зовнішнього, так і внутрішнього тиску 1 бар.
- Притискаємо поршень в нерухомому положенні.
- Поставте балон в напірну камеру з\(P_{ext}=2\) брусом.
- Раптом потягніть за кілочок.
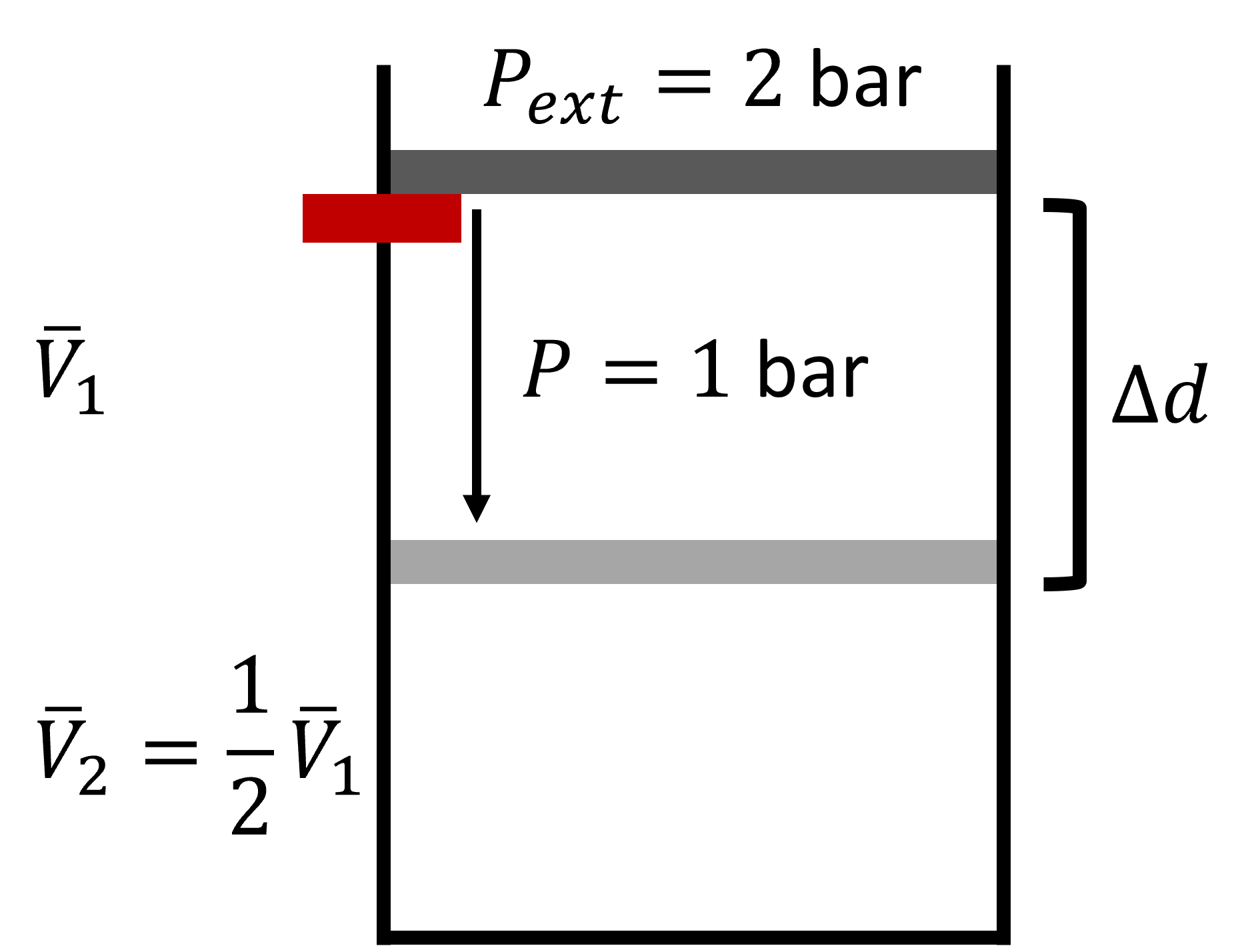
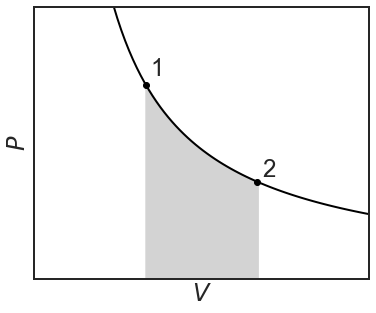
Поршень буде збивати до тих пір, поки внутрішній і зовнішній тиск знову врівноважуються і обсяг 1/2 л. Зверніть увагу, що зовнішній тиск підтримувався постійним на рівні 2 бар під час витягування кілочка і що внутрішній і зовнішній тиск не були збалансований на весь час. \(P-V\)На діаграмі ідеального газу,\(P\) є гіперболічна функція\(V\) під постійною температурою (ізотермічна), але це відноситься до внутрішнього тиску газу. Це зовнішній, який розраховує при обчислювальній роботі, і вони не обов'язково однакові. Поки\(P_{external}\) постійна, робота представлена прямокутником.
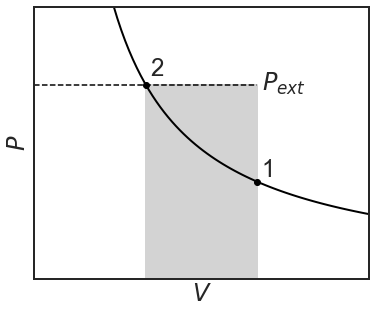
Обсяг виконуваної роботи дорівнює затіненої області і в рівнянні:
\[w=-\int^{V_2}_{V_1}{PdV}=-P_{ext}(V_2-V_1)=-P\Delta V \nonumber \]
Це являє собою максимальний обсяг роботи, який можна виконати для ізотермічного стиснення. Роботи ведуться по системі, тому загальна робота, що виконується, позитивна. Повторимо експеримент, але на цей раз поршень буде стискати оборотно на нескінченно малих кроках, де\(P_{ext}=P_{system}\):
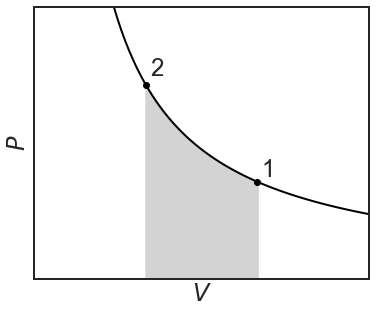
Для ідеального газу обсяг роботи, що виконується вздовж реверсивного стиснення, становить:
\[w=-\int^{V_2}_{V_1}{PdV}=-nRT\int^{V_2}_{V_1}{\frac{1}{V}}=-nRT\ln{\left(\frac{V_2}{V_1}\right)} \nonumber \]
Обсяг роботи, що виконується з двома системами, не однаковий на двох діаграмах (див. Сірі області). Робота - це не стан, а функція шляху, оскільки вона залежить від пройденого шляху. Ви можете сказати, яка велика різниця. В обох випадках система стискається з стану 1 в стан 2. Ключ - це слово раптово. Прив'язавши положення на місці для першого стиснення, ми створили ситуацію, коли зовнішній тиск вище внутрішнього (\(P_{ext}>P\)). Оскільки робота виконується раптово, витягуючи кілочок назовні, внутрішній тиск намагається наздогнати зовнішнє. Під час другого стиснення ми маємо\(P_{ext}=P\) в усі часи. Це трохи схоже на падіння зі скелі проти плавного ковзання вниз по пагорбу. Шляхом один називають незворотним шляхом, другий - оборотним.
Оборотний шлях - це шлях, який слідує за низкою станів у спокої (тобто силам дозволяється балансувати в будь-який час). У незворотному сили балансують лише в самому кінці процесу.
Зверніть увагу, що на оборотному ізотермічному стисненні проводиться менше роботи, ніж одноступінчаста незворотна ізотермічна компресія. Насправді мінімальний обсяг роботи, який можна виконати під час стиснення, завжди відбувається по оборотному шляху.
Ізотермічне розширення
Розглянемо поршень, який розширюється при постійній температурі (ізотермічний) до подвійного його початкового об'єму:
- Почніть з балона 1 літр в напірній камері з зовнішнім і внутрішнім тиском 2 бар.
- Притискаємо поршень в нерухомому положенні.
- Вийміть балон з напірної камери з P ext = 1 бар.
- Раптом потягніть за кілочок.

Поршень буде стріляти вгору до тих пір, поки внутрішній і зовнішній тиск знову врівноважуються і обсяг становить 2 л. Зверніть увагу, що зовнішній тиск підтримувався постійним на рівні 1 бар під час витягування кілочка і що внутрішній і зовнішній тиск не були збалансований на весь час.
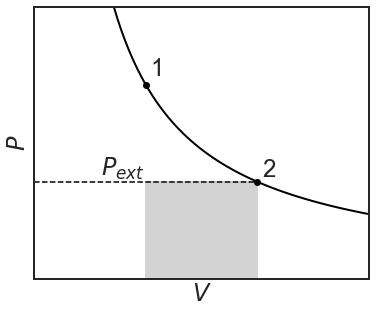
Обсяг незворотної роботи знову дорівнює затіненої області і рівнянню:
\[w=-P\Delta V=-P_{ext}(V_2-V_1)=-P\Delta V \nonumber \]
Це мінімальний обсяг робіт, який можна виконати для ізотермічного розширення. Роботи ведуться по системі, тому загальна робота, що виконується, негативна. Повторимо експеримент, але на цей раз поршень буде стискати оборотно на нескінченно малих кроках, де\(P_{ext}=P_{system}\):
Зверніть увагу, що виконується не тільки більше роботи, ніж одноступеневе необоротне ізотермічне розширення, але це той же обсяг роботи, що і оборотне ізотермічне стиснення. Це максимальний обсяг роботи, який можна виконати під час розширення.