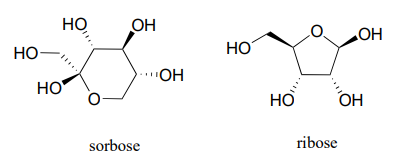
10.3: Геміацетали, гемікетали та гідрати
- Page ID
- 20719
Огляд
Одним з найважливіших прикладів реакції нуклеофільного приєднання в біохімії, і в хімії вуглеводів зокрема, є додавання спирту до кетону або альдегіду. Коли алкоголь додає до альдегіду, результат називається геміацеталь; коли спирт додає до кетону, отриманий продукт є гемікетал.
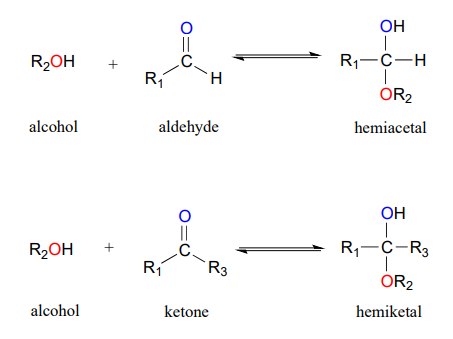
(Префікс 'hemi' (половина) використовується в кожному терміні, оскільки, як ми незабаром побачимо, може статися додавання другого спиртового нуклеофіла, в результаті чого утворюються види, які називаються ацеталями та кеталами.)
Перетворення спирту і альдегіду (або кетону) в геміацеталь (або гемікетал) є оборотним процесом. Узагальнений механізм процесу при фізіологічному рН показаний нижче.
Біохімічний механізм геміацетального утворення:
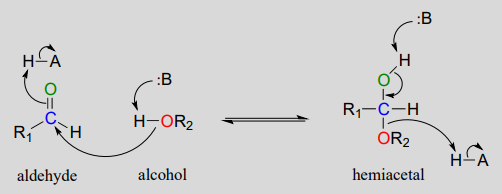
Взагалі геміацетали (і гемікетали) вище за енергією, ніж їх альдегідно-спиртові компоненти, тому рівновага для реакції лежить зліва. Однак, як ми незабаром побачимо в контексті глюкози та інших цукрів, п'ять- і шестичленні циклічні геміацетали значно нижчі за енергією і сприятливі при рівновазі: нагадаємо з глави 3 властиву стабільність п'яти- і шестичленних кілець.
Альдегіди і кетони, перебуваючи у водному розчині, існують в рівновазі зі своєю гідратною формою. Гідрат утворюється в результаті додавання молекули води до карбонільного вуглецю альдегіду або кетону.
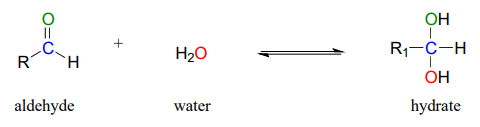
Хоча ви повинні знати, що альдегідні та кетонові групи можуть існувати значною мірою в їх гідратованих формах, коли у водному розчині (залежно від їх структури), вони зазвичай витягуються в їх негідратованій формі заради простоти.
Механізм, який ми щойно побачили для формування геміацеталів, застосовується до біохімічних реакцій, що відбуваються при фізіологічних\(pH\). Однак в органічній лабораторії утворення геміацеталів і гемікеталів зазвичай відбувається в присутності сильної кислоти. Кислота каталізує реакцію протонуванням карбонільного кисню, тим самим збільшуючи електрофільність карбонільного вуглецю. Зверніть увагу в механізмі нижче, що висококислі проміжні продукти намальовані, що було б нерозумно пропонувати для відповідних біохімічних механізмів, що відбуваються при фізіологічних\(pH\).
Кислотно-каталізоване утворення геміацеталів (небіологічне):
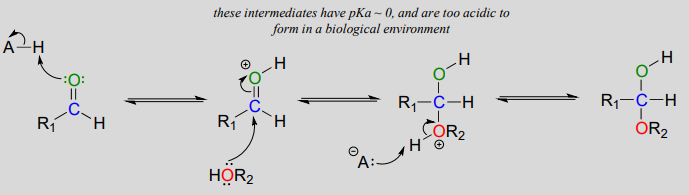
Цукор як внутрішньомолекулярні геміацетали та гемікетали
Як було сказано вище, реакції геміацеталів і гемікеталів є центральними в хімії вуглеводів. Нагадаємо, що молекули цукру зазвичай містять або альдегід, або кетонову функціональну групу, крім декількох алкогольних груп. Альдегідні цукру часто називають альдозами; кетонові цукру як кетози. Наприклад, глюкоза - це альдоза, а фруктоза - кетоза - їх структури намальовані нижче в проекції Фішера:
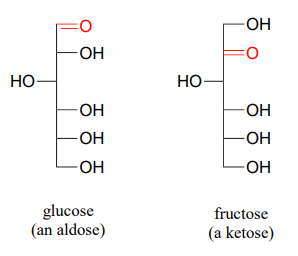
Який термін описує взаємозв'язок глюкози і фруктози (іншими словами, які вони ізомери)?
Глюкоза і фруктоза показані вище в їх формі з відкритим ланцюгом. Однак нагадаємо з розділу 1.3, що у водному розчині глюкоза, фруктоза та інші цукри п'яти-шести вуглеців швидко переходять між прямоланцюговими та циклічними формами. Це відбувається через утворення внутрішньомолекулярних геміацеталей і гемікеталів. Це просто означає, що група «R» алкоголю вже ковалентно приєднана до групи «R» альдегіду (R1 в нашому загальному механізмі).
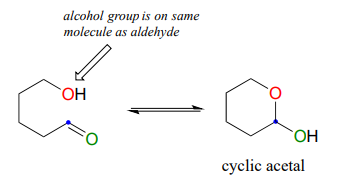
На відміну від більшості біохімічних реакцій, які ви побачите в цьому тексті, реакції циклізації цукру не каталізуються ферментами: вони відбуваються спонтанно і оборотно у водному розчині. Для більшості п'яти- і шестивуглецевих цукрів циклічні форми переважають в рівновазі.
Циклічна форма глюкози - це шестичленне кільце, з внутрішньомолекулярним геміацеталем, утвореним атакою гідроxl на вуглець #5 на альдегідний вуглець (вуглець #1, також називається аномерним вуглецем у вуглеводній термінології).
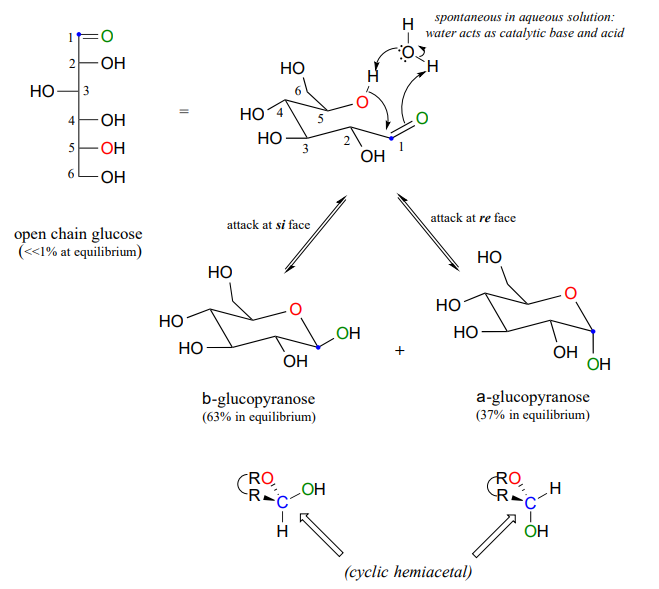
Циклічна форма глюкози називається глюкопіраноза. Як було розглянуто вище, нуклеофільна атака на планарну карбонільну групу може відбуватися на будь-якій грані площини, що призводить до двох різних стереохімічних результатів - в даному випадку до двох різних діастереомерів. У вуглеводній номенклатурі ці два діастереомери називаються аномерами a і b глюкопіранози.
Оскільки утворення глюкопіранози відбувається спонтанно без ферментного каталізу, не повинні утворюватися рівні кількості цих двох аномерів? Насправді цього не відбувається: в рівновазі майже вдвічі більше одного аномера, ніж іншого. Чому це? Пам'ятайте (розділ 3.2), що шестичленні кільця існують переважно в конформації стільця, і що нижча енергетична конформація стільця полягає в тому, що несприятливі взаємодії між замісниками мінімізуються - у більшості випадків це конформація, в якій більші замісники знаходяться в екваторіальне положення. У конформації нижньоенергетичного крісла основного b аномера глюкопіранози всі гідроксильні групи знаходяться в екваторіальному положенні, а в малій аномерній гідроксильній групі примусово в осьове положення. В результаті аномер вище за енергією, і менш рясний при рівновазі.
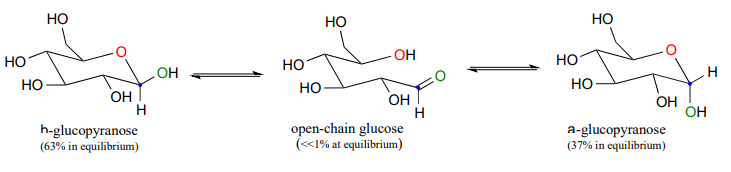
Намалюйте механізм перетворення а-глюкопіранози в глюкозу з відкритим ланцюгом.
Фруктоза у водному розчині утворює шестичленний циклічний гемікетал, який називається фруктопіранозою, коли гідроксильний кисень на вуглець #6 атакує кетоновий вуглець (вуглець #2, аномерний вуглець у фруктозі).
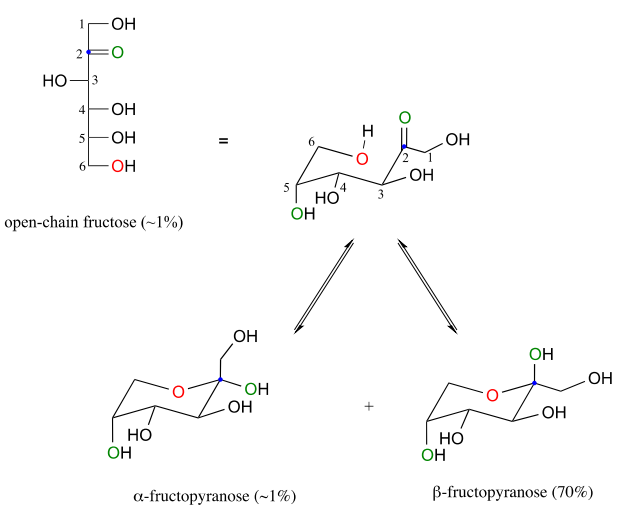
У цьому випадку аномер b сильно сприятливий в рівновазі співвідношенням 70:1, оскільки в мінорі a аномер громіздкіша\(CH_2OH\) група займає осьове положення.
Зверніть увагу на наведеному вище малюнку, що відсотки\(\alpha \) та\(\beta \) аномери, присутні в рівновазі, не складають 100%. Фруктоза також існує в розчині у вигляді п'ятичленного циклічного гемікеталу, іменованого в номенклатурі вуглеводів фруктофураноза. При утворенні фруктофуранози з фруктози з відкритим ланцюгом гідроксильна група на п'ятому вуглеці атакує кетон.
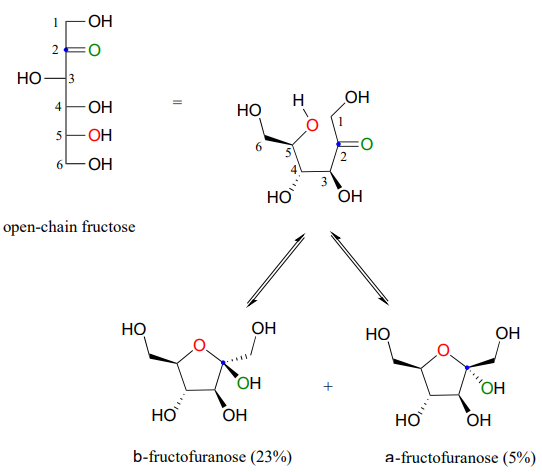
Тоді у водному розчині фруктоза існує у вигляді рівноважної суміші 70%\(\beta \) -фруктопіранози, 23%\(\beta \) -фруктофуранози, і менших відсотків відкритого ланцюга і циклічних\(\alpha \) -аномерів. \(\beta \)Піранозна форма фруктози є одним з найсолодших сполук відомих і є основним компонентом кукурудзяного сиропу з високим вмістом фруктози. Форма\(\beta \) -фураноза набагато менш солодка.
Хоча ми розглядали конкретні приклади глюкози та фруктози, інші п'ять- та шестивуглецеві моносахариди також існують у розчині як рівноважні суміші відкритих ланцюгів та циклічних геміацеталів та гемікеталів. Більш короткі моносахариди навряд чи піддаються аналогічним кільцеутворюючим реакціям, однак, через властиву нестійкості трьох і чотиричленних кілець.
- Визначте аномерний вуглець кожного з цукрів, показаних нижче, і вкажіть, чи показана структура є геміацетальною або гемікетальною.
- Намалюйте механізми циклізації форм з відкритим ланцюгом до показаних циклічних форм.