13.11: Комерційно важливі спирти
- Page ID
- 24092
На цій сторінці розглядається виробництво спиртів шляхом прямої гідратації алкенів, концентруючись головним чином на гідратації етену для отримання етанолу. Потім він порівнює цей метод з виготовленням етанолу шляхом бродіння.
Виготовлення спиртів з алкенів
Етанол виготовляється шляхом взаємодії етена з парою. Використовуваним каталізатором є твердий діоксид кремнію, покритий фосфорною (V) кислотою. Реакція оборотна.
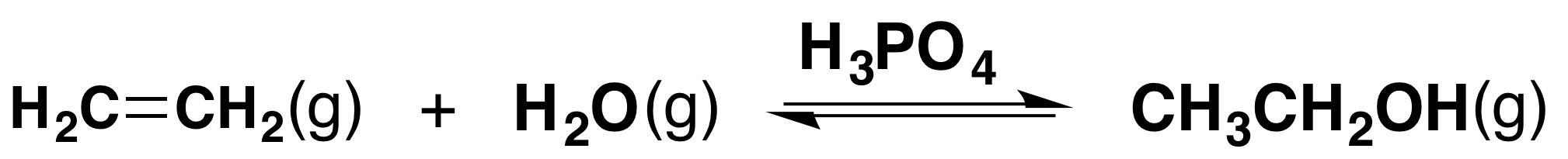

Лише 5% етена перетворюється в етанол при кожному проході через реактор. Видаляючи етанол з рівноважної суміші і переробляючи етен, можна досягти загальної конверсії 95%. Схема протікання реакції виглядає наступним чином:
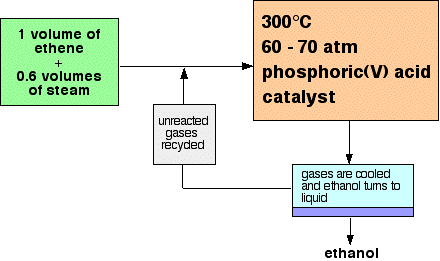
Виготовлення інших спиртів з алкенів
Деякі - але не всі - інші спирти можуть бути зроблені подібними реакціями. Використовуваний каталізатор і умови реакції будуть змінюватися від алкоголю до алкоголю. Причина того, що існує проблема з деякими спиртами, добре ілюструється спробою зробити алкоголь з пропену, CH 3 CH = CH 2. В принципі, існує два різних спирти, які можуть утворитися:
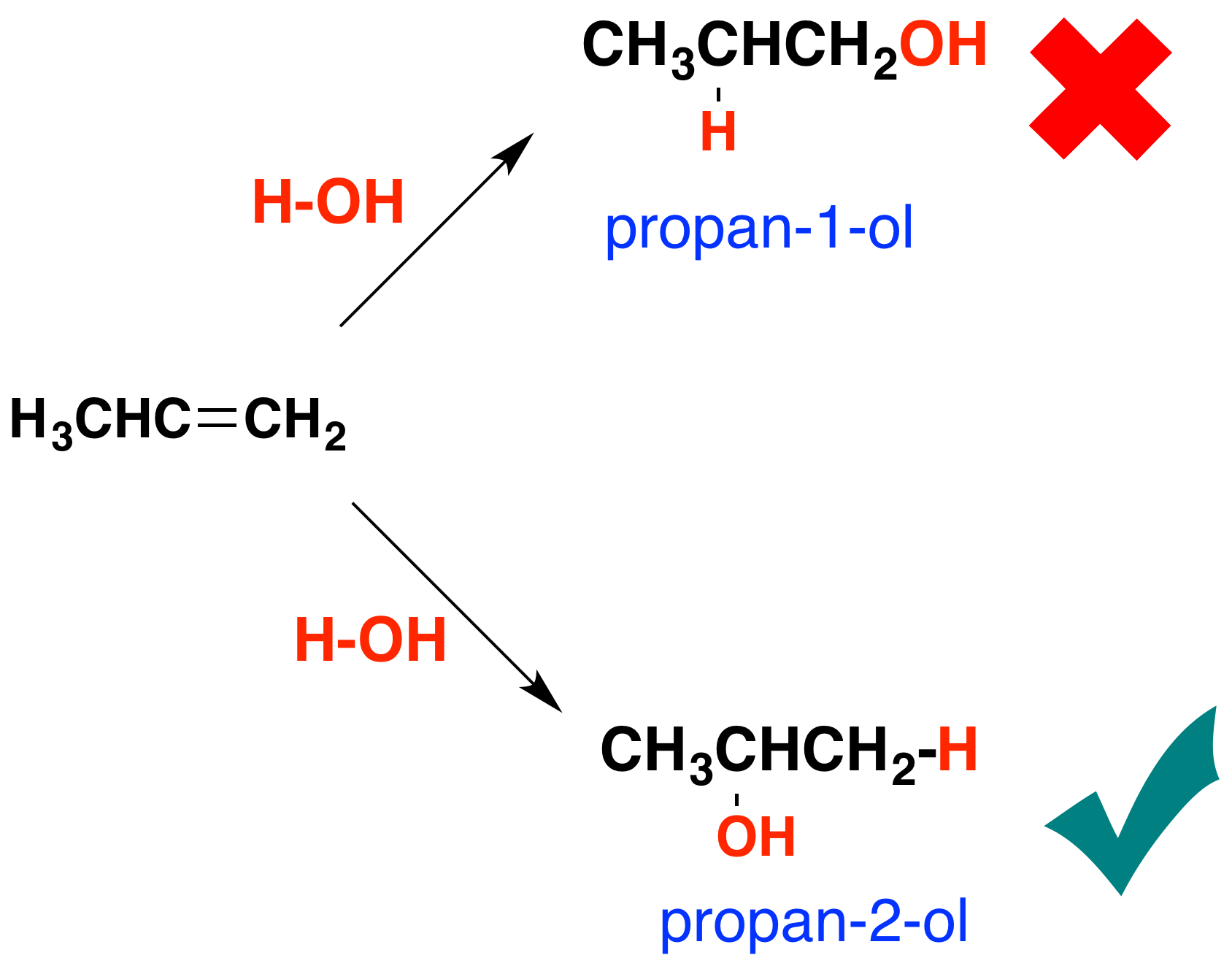
Ви можете очікувати отримати або пропан-1-ол або пропан-2-ол залежно від того, який шлях навколо води додає до подвійного зв'язку. На практиці те, що ви отримуєте - це пропан-2-ол. Якщо додати молекулу H-X через подвійний зв'язок вуглецево-вуглецевий, водень майже завжди приєднується до вуглецю з найбільшою кількістю воднів на ньому вже - в цьому випадку CH 2, а не CH. Ефект цього полягає в тому, що обов'язково будуть деякі спирти, які неможливо зробити, реагуючи алкенами з парою, оскільки додавання було б неправильним шляхом.
Виготовлення етанолу шляхом бродіння
Цей метод застосовується лише до етанолу, і ви не можете зробити будь-який інший алкоголь таким чином. Вихідний матеріал для процесу варіюється в широких межах, але, як правило, буде певна форма крохмалистого рослинного матеріалу, такого як кукурудза (США: кукурудза), пшениця, ячмінь або картопля. Крохмаль є складним вуглеводом, і інші вуглеводи також можуть використовуватися - наприклад, в лабораторії сахароза (цукор) зазвичай використовується для виробництва етанолу. Промислово це не мало б сенсу. Було б нерозумно вдосконалювати цукор, якби все, що ви збиралися використовувати його, - це бродіння. Однак немає причин, чому ви не повинні починати з оригінальної цукрової тростини.
Насамперед необхідно розбити складні вуглеводи на більш прості. Наприклад, якщо ви починали з крохмалю в зерні, як пшениця або ячмінь, зерно нагрівають гарячою водою для вилучення крохмалю, а потім нагрівають солодом. Солод - це пророщений ячмінь, який містить ферменти, які розщеплюють крохмаль на простіший вуглевод, який називається мальтозою\(C_{12}H_{22}O_{11}\). Мальтоза має ту ж молекулярну формулу, що і сахароза, але містить дві одиниці глюкози, з'єднані між собою, тоді як сахароза містить одну глюкозу і одну одиницю фруктози.
Потім додають дріжджі і суміш зберігають теплою (скажімо, 35° C) протягом, можливо, декількох днів, поки бродіння не завершиться. Повітря витримується поза сумішшю, щоб запобігти окисленню етанолу, виробленого до етанової кислоти (оцту). Ферменти в дріжджах спочатку перетворюють вуглеводи, такі як мальтоза або сахароза, в ще простіші, такі як глюкоза і фруктоза, обидва\(C_6H_{12}O_6\), а потім перетворюють їх у свою чергу в етанол і вуглекислий газ. Ви можете показати ці зміни як прості хімічні рівняння, але біохімія реакцій набагато, набагато складніше, ніж це припускає.
\[ C_{12}H_{22}O_{11} + H_2O \longrightarrow 2C_6H_{12}O_6 \]
\[ C_6H_{12}O_6 \longrightarrow 2CH_3CH_2OH + 2CO2\]
Дріжджі гинуть від концентрації етанолу, що перевищує близько 15%, і це обмежує чистоту етанолу, який може бути вироблений. Етанол відокремлюють від суміші шляхом фракційної перегонки з отриманням 96% чистого етанолу. З теоретичних причин (мінімальна температура кипіння азеотропа) видалити останні 4% води шляхом фракційної перегонки не можна.
| Бродіння | гідратація етену | |
|---|---|---|
| Тип процесу | Пакетний процес. Все кладуть в ємність і потім залишають до повного бродіння. Потім ця партія очищається і налаштована нова реакція. Це неефективно. | Безперервний процес потоку. Потік реагентів безперервно пропускається над каталізатором. Це більш ефективний спосіб виконання справ. |
| Швидкість реакції | Дуже повільно. | Дуже швидко. |
| Якість продукту | Виробляє дуже нечистий етанол, який потребує подальшої переробки | Виробляє набагато чистіший етанол. |
| Умови реакції | Використовує ніжні температури і атмосферний тиск. | Використовує високі температури та тиск, потребуючи великої кількості енергії. |
| Використання ресурсів | Використовує відновлювані ресурси на основі рослинної сировини. | Використовує кінцеві ресурси на основі сирої нафти. |