13.8: Металеорганічні реагенти
- Page ID
- 24101
Вступ
Реагент Гріньяра має формулу,\(\ce{RMgX}\) де\(\ce{X}\) є галогеном, і\(\ce{R}\) являє собою алкіл або аріл (на основі бензольного кільця) групу. Для цілей цієї сторінки ми візьмемо R як алкільну групу. Типовий реагент Гріньяра може бути\(\ce{CH3CH2MgBr}\). Літійорганічні реагенти мають хімічну формулу rLi. Типовим реагентом може бути\(\ce{CH3CH2Li}\).
Формування металоорганічних реагентів
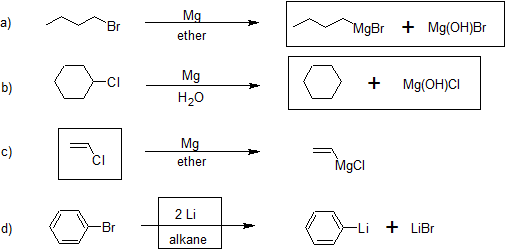
Багато металоорганічних реагентів є комерційно доступними, однак їх часто потрібно виготовити. Наступні рівняння ілюструють ці реакції для часто використовуваних металів літію і магнію (R може бути водневими або алкільними групами в будь-якій комбінації).
- Алкіл літієвий реагент
\[ \ce{R3C-X} + \ce{2Li} \rightarrow \ce{R3C-Li} + \ce{LiX}\]
- Реагент Гріньяра
\[\ce{R3C-X} + \ce{Mg} \rightarrow \ce{R3C-MgX}\]
- Органокупрат реагент
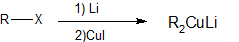
Реактивність галогенідів в цих реакціях зростає в порядку: Cl < Br < I і фториди зазвичай не використовуються. Алкілмагнієві галогеніди, описані в другій реакції, називаються Реагентами Гріньара після французького хіміка Віктора Гріньяра, який відкрив їх і отримав Нобелівську премію в 1912 році за цю роботу. Інші метали, згадані вище, реагують аналогічним чином, але Гріньяр і Алкі літієві реагенти найбільш широко використовуються. Хоча формули, намальовані тут для реагентів алкіл-літію і Гріньяра, відображають стехіометрію реакцій і широко використовуються в хімічній літературі, вони не точно зображують структурну природу цих чудових речовин. Суміші полімерних та інших супутніх і комплексних видів знаходяться в рівновазі в умовах, зазвичай використовуваних для їх приготування. Органокупрат реагенти мають обмежену реакційну здатність і будуть використовуватися для синтезу кетонів.
Металеорганічні реагенти - сильні нуклеофіли
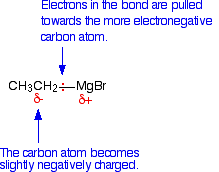
Зв'язок між атомом вуглецю і атомом металу полярна. Тому металоорганічні реагенти є сильними нуклеофілами. Використовуючи реагент Гріньяра як приклад, вуглець є більш електронегативним, ніж магній, тому сполучна пара електронів тягнеться до вуглецю, створюючи частковий негативний заряд. Реагенти Гріньяра - сильні нуклеофіли. Нуклеофільні атоми вуглецю дуже корисні для побудови вуглецевих ланцюгів у багатоступінчастому синтезі.
Реакції Гріньяра створюють можливість для реакцій заміщення на вінілових вуглецях. Цей шлях реакції дуже корисний, оскільки галогеніди вінілу не можуть реагувати механізмами SN1 та SN2.
Металоорганічні реагенти та протичні розчинники (як вода)
Все повинно бути ідеально сухим, оскільки металоорганічні реагенти вступають в реакцію з водою (див. Нижче) або будь-яким протонним розчинником. Реакції з використанням реагенту Гріньяра повинні використовувати ефір як розчинник. Літійорганічні реакції також вимагають апротних розчинників, але ефіри не потрібні, і алкани можуть використовуватися як розчинники. Отриману реакційну суміш використовують безпосередньо для наступної реакції. Відсутні процедури поділу та ізоляції між етапами реакції. Металоорганічні реагенти реагують з водою або будь-яким протонним розчинником для отримання алканів. З цієї причини все повинно бути дуже сухим під час приготування вище. Термін сухий означає, що немає води або інших протонованих розчинників. Є ще рідкий ефірний розчинник.
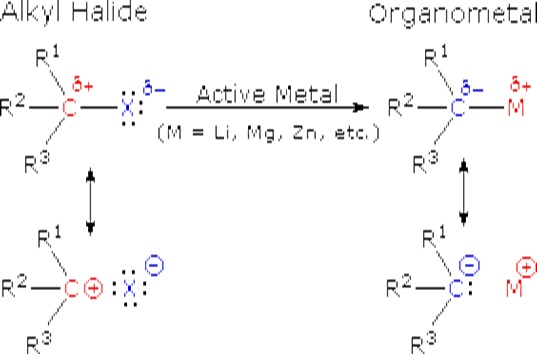
Необхідно використовувати відповідний розчинник. Для утворення алкілу літію зазвичай використовують пентан або гексан. Діетиловий ефір також може бути використаний, але наступний алкіл-літієвий реагент необхідно використовувати відразу після приготування через взаємодію з розчинником. Етиловий ефір або THF необхідні для утворення реагентів Гріньяра. Самотні парні електрони з двох ефірних молекул утворюють комплекс з магнієм в реагенті Гріньяра (Як показано нижче). Цей комплекс сприяє стабілізації металоорганогену і підвищує його здатність реагувати.
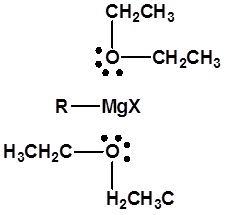
Ці реакції, очевидно, є реакціями заміщення, але їх не можна класифікувати як нуклеофільні заміни, як і попередні реакції алкілгалогенідів. Оскільки функціональний атом вуглецю був зменшений, полярність отриманої функціональної групи інвертується (спочатку електрофільний вуглець стає нуклеофільним). Ця зміна, показана нижче, робить реагенти алкілу літію та Гріньяра відмінними нуклеофілами та корисними реагентами в синтезі.
Приклад:
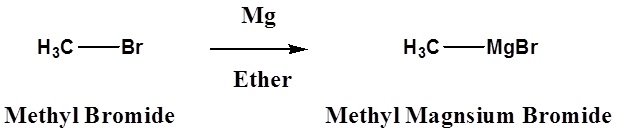
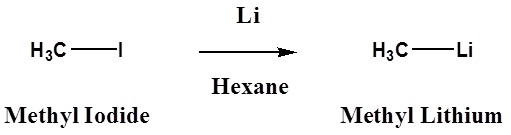
Загальні металоорганічні реагенти
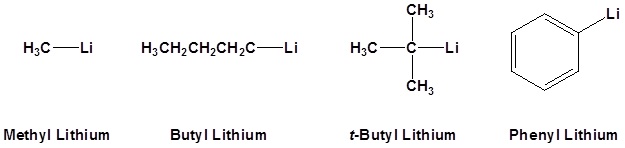
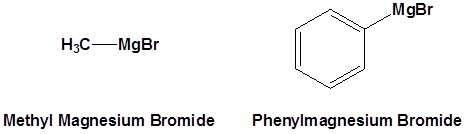
Вправи
13.
Передбачте продукт або вкажіть відсутній регент (и) у реакціях нижче.
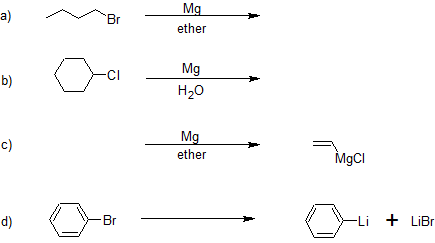
- Відповідь
-
13.