13.6: Синтез спиртів - огляд
- Page ID
- 24118
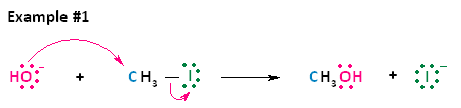
Спирти отримують реакціями S N 2 & S N 1 (сольволіз)
Алкілгалогеніди можуть бути перетворені в спирти за допомогою реакцій S N 2 з OH - як нуклеофіла. Субстрати, які піддаються заміщенню реакцією SN1, можуть бути перетворені на спирти, використовуючи воду як нуклеофіла (і це може бути навіть розчинник). Нагадаємо, що реакції S N 1 сприяють в полярних, протонних розчинниках.
Спирти з алкенів
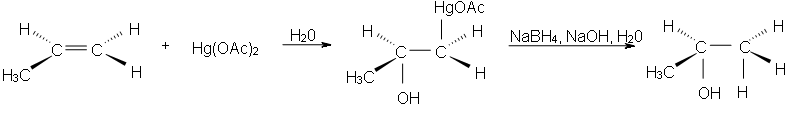
Оксимеркурація - це спеціальна електрофільна добавка. Він є антистереоспецифічним і регіоселективним. Регіоселективність - це процес, в якому замісники вибирають один напрямок, до якого він вважає за краще приєднуватися, над усіма іншими можливими напрямками. Хороша річ у цій реакції полягає в тому, що немає перебудови карбокатів через стабілізацію реактивного проміжного продукту. Подібна стабілізація спостерігається і при додаванні брому до алкенів.
Карбокатіонная перебудова - це процес, при якому проміжне з'єднання карбокатіону може утворювати більш стабільний іон. При переробці карбокатів реакція не зможе швидко гідратувати в м'яких умовах і вироблятися з високою врожайністю. Ця реакція дуже швидка і протікає з 90% врожайністю.
Гідроборація-Окислення - це двоступеневий шлях, який використовується для отримання спиртів. Реакція протікає антимарковниковим способом, де водень (з BH 3 або BHR 2) приєднується до більш заміщеного вуглецю, а бор приєднується до найменш заміщеного вуглецю в алкеновій зв'язці. Крім того, боран діє як кислота Льюїса, приймаючи два електрони в своїй порожній орбіталі p з алкена, який є багатим електронами. Цей процес дозволяє бору мати електронний октет. Дуже цікавою характеристикою цього процесу є те, що він не вимагає ніякої активації каталізатором. Механізм гідроборації має елементи як гідрування, так і електрофільного додавання, і це стереоспецифічний (син-додаток), що означає, що гідроборація відбувається на одній грані подвійного зв'язку, це призводить цис стереохімії.
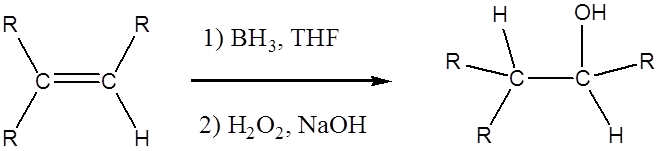
Діоли з алкенів 
Епоксиди можуть бути розщеплені водною кислотою, щоб дати гліколі, які часто є діастереомерними, з тими, які отримують реакцією сингідроксилювання, описаною вище. Перенесення протонів з кислотного каталізатора генерує кон'югатну кислоту епоксиду, яку атакують нуклеофіли, такі як вода, так само, як циклічний іон бромонію, описаний вище, зазнає реакції. Результатом є антигідроксилювання подвійного зв'язку, на відміну від синстереоселективності більш раннього методу. У наступному рівнянні ця процедура проілюстрована для цис-дизаміщеного епоксиду, який, звичайно, можна було б отримати з відповідного цис-алкена. Ця гідратація епоксиду не змінює ступінь окислення будь-яких атомів або груп.
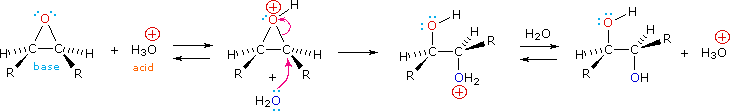
Тетроксид осмію окислює алкени, даючи гліколі через додавання синів. Гліколь, також відомий як віцинальний діол, являє собою з'єднання з двома -OH групами на сусідніх вуглець.
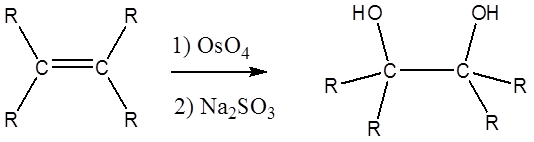
Реакція з\(OsO_4\) - це узгоджений процес, який має циклічний проміжний і ніяких перестановок. Vicinal сину дигідроксилювання доповнює послідовність епоксид-гідролізу, яка являє собою анти дигідроксилювання алкену. Коли алкен реагує з тетроксидом осмію, в продукті гліколю можуть утворюватися стереоцентри. Цис-алкени дають мезопродукти, а транс-алкени дають рацемічні суміші.