9.6: Гідратація - Гідроборація-Окислення
- Page ID
- 22834
Цілі навчання
- застосовувати принципи регіоселективності та стереоселективності до реакцій приєднання алкенів
- прогнозувати продукти, вказати реагенти та визначити найбільш ефективну реакцію для гідратації алкенів (кислотна каталізована гідратація; або оксимерція/демеркурація; або гідроборація/окислення)
Гідроборація-Окислення - це двоступеневий шлях, який використовується для отримання спиртів. Реакція протікає антимарковниковим способом, де водень (з\(\ce{BH3}\) або\(\ce{BHR2}\)) приєднується до більш заміщеного вуглецю і бор приєднується до найменш заміщеного вуглецю в алкеновому подвійному зв'язку. Крім того, буран діє як електрофіл, приймаючи два електрони в своїй порожній орбіталі p від алкена, який є багатим електроном. Цей процес дозволяє бору мати електронний октет. Дуже цікавою характеристикою цього процесу є те, що він не вимагає ніякої активації каталізатором. Механізм гідроборації має елементи як гідрування, так і електрофільного додавання, і це стереоспецифічний (син-додаток), що означає, що гідробірування відбувається на одній грані подвійного зв'язку, це призводить цис стереохімії.
Комплекс «Боран»
Дуже важливо розуміти будову і властивості молекули борана. Боран існує природним шляхом як дуже токсичний газ, і він існує як димер загальної формули\(\ce{B2H6}\) (диборан).
\[\ce{BH3→B2H6} \nonumber\]
Оскільки диборановий димер запалюється мимовільно в повітрі, він комерційно поширюється в ефірі або тетрагідрофуранових (THF) розчинами. У цих рішеннях буран може існувати як кислотно-лужний комплекс Льюїса, який дозволяє бору мати октет електронів.

Механізм
Крок #1: Гідроборація алкену
Додавання бурану до алкену ініціюється і протікає як узгоджена реакція, оскільки розрив зв'язку та утворення зв'язків відбуваються одночасно. Вакантна 2p орбіталь бору бере на себе роль електрофілу і приймає pi електрони з нуклеофільного алкену. Бор додає до менш заміщеного вуглецю алкену, який потім розміщує водень на більш заміщений вуглець. Обидва, бор і водень додають одночасно на одній грані подвійного зв'язку (син-додавання). При узгодженому механізмі не відбувається утворення карбокатиону.

Перехідний стан
.bmp)
* Зверніть увагу, що карбокатіон не утворюється. Тому ніякої перестановки не відбувається.
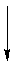

Важливо зазначити, що реакція триває ще два рази, поки всі три водні на борані не відреагували з алкенами, щоб створити проміжний проміжний R3B триалкілборану.
Крок #2: Окислення тріалкілборану перекисом водню
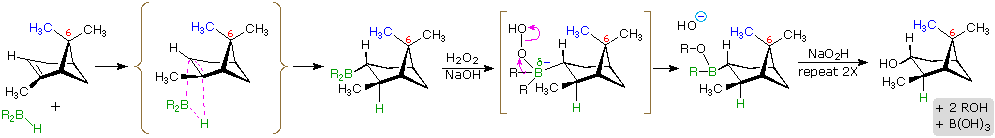
Перекис водню (\(\ce{HOOH}\)) є нуклеофілом у цій реакції, оскільки він є донором електронів новоутвореного триалкілборану, що утворився в результаті попереднього гідробірування.
\[\ce{HOOH + OH^{-} -> HOO^{-} + HOH}\]
.bmp)
У цій другій частині механізму перестановка групи R з її парою зв'язкових електронів з сусіднім киснем призводить до втрати гідроксид-іона.
Ще дві ці реакції з гідропероксидом будуть відбуватися для того, щоб дати тріалкілборат.

На завершальній стадії процесу окислення тріалкілборат реагує з водою з\(\ce{NaOH}\) отриманням спирту і борату натрію (\ ce {Na3bo3}\).
\[\ce{(RO3)B + 3NaOH -> 3OH + Na3BO3}\]
Якщо вам потрібні додаткові візуальні ефекти, які допоможуть вам зрозуміти механізм, натисніть на зовнішні посилання, надані в кінці цього розділу.
Стереохімія кроку гідроборації
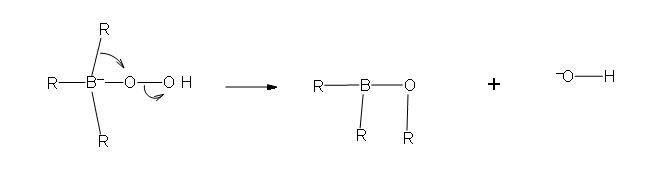
Реакція гідробірації є однією з небагатьох простих реакцій додавання, які протікають чисто в син-моді. Як зазначалося вище, це одноступінчаста реакція. Оскільки зв'язок вуглецю подвійного зв'язку з бором і воднем узгоджена, то випливає, що геометрія цього додавання повинна бути сином. Крім того, перестановки малоймовірні, оскільки дискретний проміжний проміжний проміжний продукт ніколи не утворюється. Ці особливості ілюструються для гідробірування α-пінену.
Оскільки процедура гідробірування найчастіше використовується для гідратації алкенів антимарковникова способом, нам також потрібно знати стереоселективність другої реакції окислення, яка замінює гідроксильну групу атомом бору. Незалежне дослідження показало, що ця реакція відбувається із збереженням конфігурації, тому загальне додавання води також синхронізується.
Гідроборація α-пінена також є приємним прикладом контролю стеричної перешкоди в хімічній реакції. У менш складних алкенах, використовуваних в попередніх прикладах, площина подвійного зв'язку часто була площиною симетрії, і додавання реагентів могло наближатися з однаковою легкістю з будь-якого боку. При цьому одна з метильних груп, пов'язаних з С-6 (забарвлена в синій колір у рівнянні) охоплює одну грань подвійного зв'язку, блокуючи будь-який підхід з цього боку. Тому всі реагенти, які додають до цього подвійного зв'язку, повинні наближатися з боку, протилежного цьому метилу.
Вправи
1. Намалюйте структуру лінії зв'язку продукту (ів) для цих наступних реакцій?
а)

б)
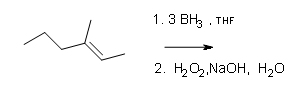
в)

2. Намалюйте структурні формули для спиртів, що виникають внаслідок гідробірації-окислення показаних алкенів.
а)

б) (Е) -3-метил-2-пентен
3. Випишіть реагенти або продукти (А-Д), показані в наступних схемах реакції.

- Відповідь
-
1.
а)
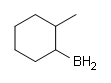
б)

в)

2.
а)

б)

3.
Посилання
- Волхардт, Пітер і Ніл Шор. Органічна хімія: будова і функції. 5-й. Нью-Йорк: W.H Фрімен і компанія, 2007.
- Фут, Крістофер, і Вільям Браун. Органічна хімія. 5-й. Белмонт, Каліфорнія: Брукс/Коул Сенгаге навчання, 2005.
- Брюіс, Паула Юрканіс. Органічна хімія. 5-й. КА. Прентіс Холл, 2006.
- Бергбрайтер Е. Девід та Девід П. Рейнвілл. Стереохімія гідробірування-окислення термінальних алкенів. Дж. Орг. Хім., 1976, 41 (18), с. 3031—3033
- Ілліч, Преддраг-Пітер; Рікерцен, Лукас С., Беккер Ерієнн. Полярна добавка до групи C = C: чому антимарковнікова гідроборація-окислення алкенів не є «анти-»? Журнал хімічної освіти., 2006, v83, n11, pg 1681-1685
