1.17: Рішення додаткових вправ
- Page ID
- 22776
Утворення облігацій: правило октету
1-1:
а) 6 в.е./2 ковалентні зв'язки
б) 4 в.е./4 ковалентні зв'язки
в) 7 в.е./1 ковалентний зв'язок
г) 6 v.e. /2 ковалентні зв'язки (також може розширити октет, щоб зробити 6 ковалентних зв'язків)
д) 1 в.е./1 ковалентний зв'язок
f) 3 в.е./3 ковалентні зв'язки
1-2:
(г) К +
1-3:
1-4:
(c) пКл
Льюїс Структури
1-5:
1-6:
а) Неон, 8 валентних електронів
б) Магній, 2 валентні електрони
в) Кисень, 6 валентних електронів
г) Бром, 7 валентних електронів
1-7:
1-8:
1-9: С.
Електронегативність і полярність зв'язку
1-10:
1-11:
а) немає дипольного моменту стрілки б/с неполярний
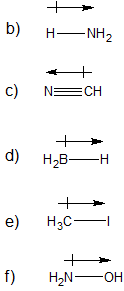
Офіційні збори
1-12:
1-13:
а) 0
б) -1
в) -2
1-14:
а) 0
б) -1
в) 0
г) +1
Іонні структури
1-15:
а) Na + і Cl -
б) Мг +2 і 2 Бр -
в) К + і НІ 3 -
г) Na + і Н 2 РО 4 -
1-16:
1-17:
а) ціанід натрію
б) СаС 2 О 4
в) гідроксид алюмінію
г) Сн 3 (РО 42)
д) ККЛО
Резонанс
1-18:
1-19:
Найбільш стійка резонансна структура має третинний карбокат. Ця третинна карбокація стабілізується гіперкон'югацією, а також двома можливими напрямками резонансу (порівняно з однією безпосередньою резонансною структурою для двох інших карбокатіонів).
1-20:
1-21:
При порівнянні депротонованих форм оцтової кислоти і етанолу, ацетату і етоксиду відповідно можна спостерігати, що ацетат делокалізує негативний заряд по всій карбоксилатної групі. Етоксид, однак, може утримувати негативний заряд лише на алкоксид, роблячи його кращою основою, але гірше як кислоту.
1-22:
Структурні, молекулярні та емпіричні формули
1-23:
1-24:
1-25:
Помилкові; емпіричні формули - це найпростіші співвідношення цілих чисел, які корисні для обчислення відсоткових складів атомів в молекулі. Однак, оскільки вони не дають абсолютної кількості атомів у молекулі, їх не можна використовувати для обчислення молекулярної маси молекули.
1-26:
а) С 2 Н 2 О
б) С 4 Н 3 Н
в) С 9 Ч 7 НІ
Кислоти та основи - Арреній, Бронстед-Лоурі та Льюїс
1-27:
Arrhenius: Arrhenius кислота - це вид, який пожертвує H+при розчиненні у воді. База Arrhenius - це вид, який руйнується, щоб дати OH- при розчиненні у воді.
Бронстед-Лоурі: Бронстед-Лоурі кислота - це вид, який буде жертвувати H+при розчиненні в розчині (не тільки у воді). Основа Бронстеда-Лоурі - це вид, який може приймати H+ в розчині (не тільки у воді).
Льюїс: Кислота Льюїса - це акцептор електронної пари. База Льюїса є донором електронної бази.
1-28:
Ка = 2,4 х 10 1
1-29:
Н 3 О + > ВЧ > Н 4 + > Н 2 О
1-30:
Н 2 -> Н 2 О > СН 3 СОО -> ГСО 4 -
1-31:
З'єднання А є більш міцною основою. З'єднання В є сильнішою кислотою.
1-32:
Група А захоче захопити H + більше, ніж група B. Оскільки C менш електронегативний, ніж N, він також не може стабілізувати негативний заряд і захоче захопити H +, щоб позбутися від заряду. (захопити = реагувати з)