6.5: Правила Уейда
- Page ID
- 17610
Кен Вейд (рис.\(\PageIndex{1}\)) розробив метод прогнозування форм скупчень бурану; однак він може бути використаний для широкого спектру заміщених боранів (таких як карборани), а також інших класів кластерних сполук.

Правила Уейда використовуються для раціоналізації форми скупчень бурану шляхом обчислення загальної кількості скелетних електронних пар (SEP), доступних для кластерного зв'язку. При використанні правил Уейда ключовим є розуміння структурних взаємозв'язків різних боран (рис.\(\PageIndex{2}\)).
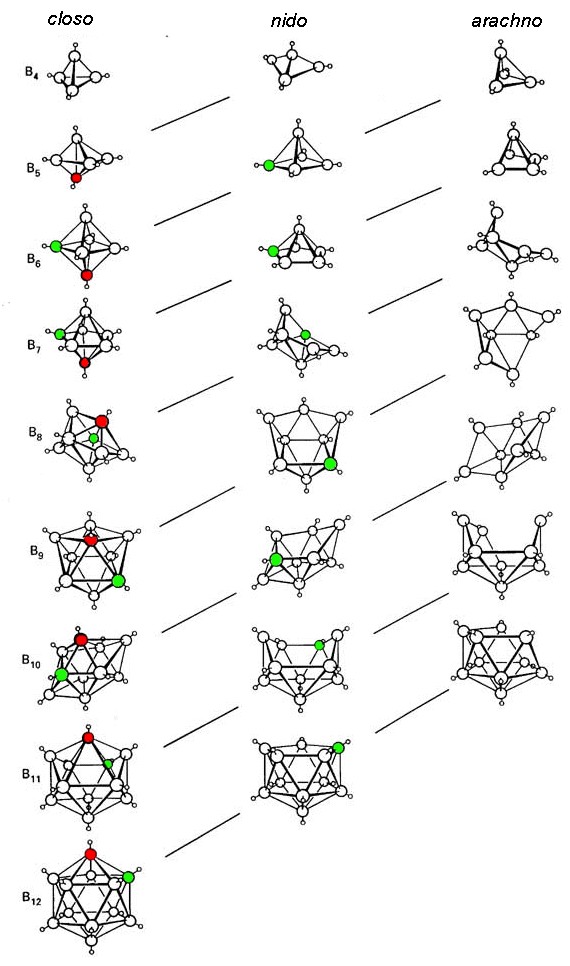
Загальна методика, якої слід дотримуватися при застосуванні правил Уейда, полягає в наступному:
- Визначте загальну кількість валентних електронів за хімічною формулою, тобто 3 електронів на B, і 1 електрон на H.
- Відніміть 2 електрони для кожної одиниці B-H (або C-H в карборані).
- Розділіть кількість інших електронів на 2, щоб отримати кількість скелетних електронних пар (SEP).
- Кластер з n вершинами (тобто n атомів бору) і n +1 SEP для зв'язку має тісну структуру.
- Кластер з n -1 вершинами (тобто n -1 атомами бору) і n +1 SEP для зв'язку має нідоструктуру.
- Кластер з n -2 вершинами (тобто n -2 атомами бору) і n +1 SEP для зв'язку має арахно-структуру.
- Кластер з n -3 вершинами (тобто n -3 атомами бору) і n +1 SEP для зв'язку має гіфоструктуру.
- Якщо кількість атомів бору (тобто n) більше, ніж n +1 SEP, то зайвий бор займає положення обмеження на трикутній фазі.
Яка структура Б 5 Н 11?
- Загальна кількість валентних електронів = (5 х В) + (11 х Н) = (5 х 3) + (11 х 1) = 26
- Кількість електронів для кожної одиниці B-H = (5 x 2) = 10
- Кількість скелетних електронів = 26 — 10 = 16
- Число СЕП = 16/2 = 8
- Якщо n +1 = 8 і n -2 = 5 атомів бору, то n = 7
- Структура n = 7 є п'ятикутною біпірамідою (рис.\(\PageIndex{2}\)), тому B 5 H 11 - арахно, засноване на п'ятикутній біпіраміді з відсутніми двома вершинами (рис.\(\PageIndex{3}\)).
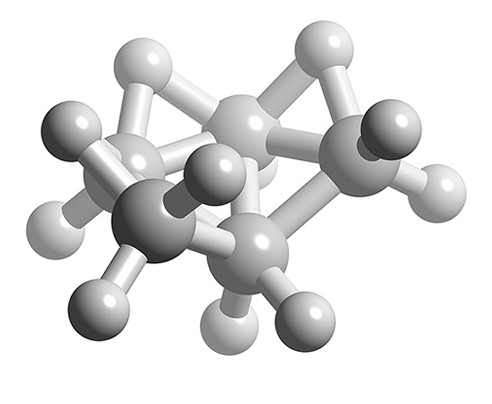
Яка структура Б 5 Н 9?
- Загальна кількість валентних електронів = (5 х В) + (9 х Н) = (5 х 3) + (9 х 1) = 24
- Кількість електронів для кожної одиниці B-H = (5 x 2) = 10
- Кількість скелетних електронів = 24 — 10 = 14
- Число СЕП = 14/2 = 7
- Якщо n +1 = 7 і n -1 = 5 атомів бору, то n = 6
- Структура n = 6 - восьмигранна (рис.\(\PageIndex{2}\)), тому B 5 H 9 - нідоструктура, заснована на восьмигранній структурі з відсутньою однією вершиною (рис.\(\PageIndex{4}\)).
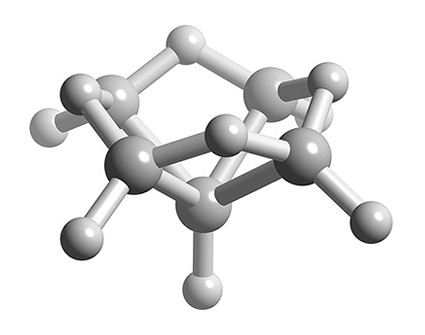
Приклад\(\PageIndex{1}\)
Яка структура Б 6 Н 6 2-?
Рішення
- Загальна кількість валентних електронів = (6 х В) + (3 х Н) = (6 х 3) + (6 х 1) + 2 = 26
- Кількість електронів для кожної одиниці B-H = (6 x 2) = 12
- Кількість скелетних електронів = 26 — 12 = 14
- Число СЕП = 14/2 = 7
- Якщо n +1 = 7 і n атомів бору, то n = 6
- Структура n = 6 - восьмигранна (рис.\(\PageIndex{2}\)), тому B 6 H 6 2- являє собою замкнуту структуру, засновану на восьмигранній структурі (рис.\(\PageIndex{5}\)).
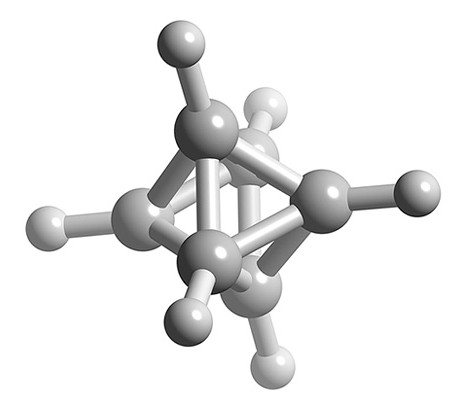
У таблиці\(\PageIndex{1}\) наведено зведення буранового кластера із загальною формулою B n H n x- та їх структурами, визначеними правилами Уейда.
| Тип | Базова формула | Приклад | Кількість вертикалей | Кількість вакансій | Кількість е- в B + заряду | Кількість склеювальних МО |
|---|---|---|---|---|---|---|
| Closo | Б н Н Н 2- | Б 6 Н 6 2- | п | 0 | 3м + 2 | п + 1 |
| Нідо | Б н Н Н 4- | Б 5 Ч 9 | п + 1 | 1 | 3н + 4 | п + 2 |
| Арачно | Б н Н Н 6- | Б 4 Ч 10 | п + 2 | 2 | 3 + 6 | п + 3 |
| Гіфо | Б н Н 8- | Б 5 Ч 11 2- | п + 3 | 3 | 3м + 8 | п + 4 |
Бібліографія
- Рудольф Р.В., Док. Хім. Рез., 1976, 9, 446.
- Уейд К.М., адв. ін.г. Хім. Радіохім. , 1976, 18, 1.
