5.1.3: Молекулярні орбіталі з d орбіталів
- Page ID
- 32803
У перехідних металах та інших більш важких елементах\(d\) орбіталі можуть поєднуватися з іншими орбіталями сумісної симетрії (та енергії), утворюючи молекулярні орбіталі. Як правило, існує три типи зв'язуючих та антизв'язуючих взаємодій, які можуть відбуватися з\(d\) орбіталями: сигма (\(\sigma\)), пі (\(\pi\)) та дельта (\(\delta\)) зв'язки.
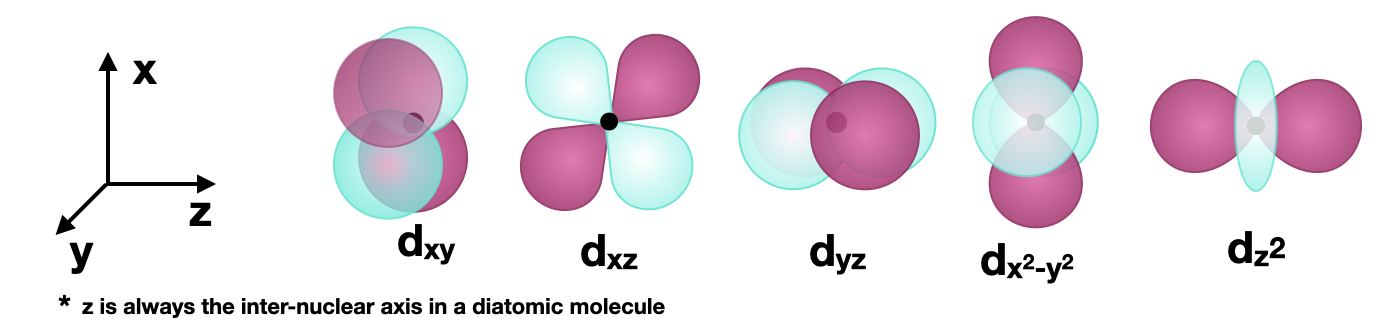 Малюнок\(\PageIndex{1}\): П'ять\(3d\) орбіталей показані. Орієнтація осей узгоджена, а\(z\) вісь горизонтальна для зручності нанесення скріплення уздовж\(z\) осі (див. приклади нижче). (CC-BY-SA; Кетрін Хаас)
Малюнок\(\PageIndex{1}\): П'ять\(3d\) орбіталей показані. Орієнтація осей узгоджена, а\(z\) вісь горизонтальна для зручності нанесення скріплення уздовж\(z\) осі (див. приклади нижче). (CC-BY-SA; Кетрін Хаас)З'єднання сигма (\(\sigma\)) з\(d\) орбіталями
\(\sigma\)зв'язки симетричні по відношенню до міжядерної осі (у двоатомної молекули це\(z\) вісь). Прикладом\(\sigma\) зв'язку, утвореного\(d\) орбіталями, є зв'язок двох\(d_{z^2}\) орбіталей (див. Рис.\(\PageIndex{2}\)). Якщо зв'язаний атом знаходиться в положенні, відмінному від\(z\) осі (наприклад, у восьмигранній геометрії), можуть утворитися і\(\sigma\) зв'язки. Наприклад, дві\(d_{x^2-y^2}\) орбіталі на атомах, з'єднаних уздовж\(y\) осей\(x\) або, також можуть утворювати\(\sigma\) зв'язок.
\(d\)орбіталі також можуть утворювати\(\sigma\) зв'язки з іншими типами орбіталей з відповідною симетрією. Прикладами орбіталів з відповідною симетрією є\(s\) орбітальні і певні\(p\) орбіталі на іншому атомі, як показано нижче на малюнку\(\PageIndex{2}\).
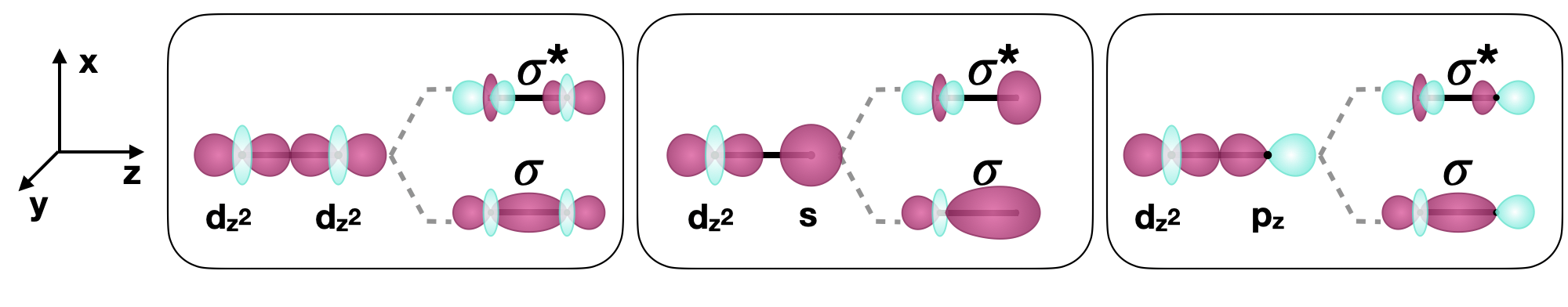 Малюнок\(\PageIndex{2}\): Вибрані приклади\(\sigma\) зв'язків за участю\(d\) орбіталів уздовж\(z\) міжядерної осі (показані жирною горизонтальною лінією) між двома атомами. (CC-BY-SA; Кетрін Хаас)
Малюнок\(\PageIndex{2}\): Вибрані приклади\(\sigma\) зв'язків за участю\(d\) орбіталів уздовж\(z\) міжядерної осі (показані жирною горизонтальною лінією) між двома атомами. (CC-BY-SA; Кетрін Хаас)Pi (\(\pi\)) склеювання з\(d\) орбіталями
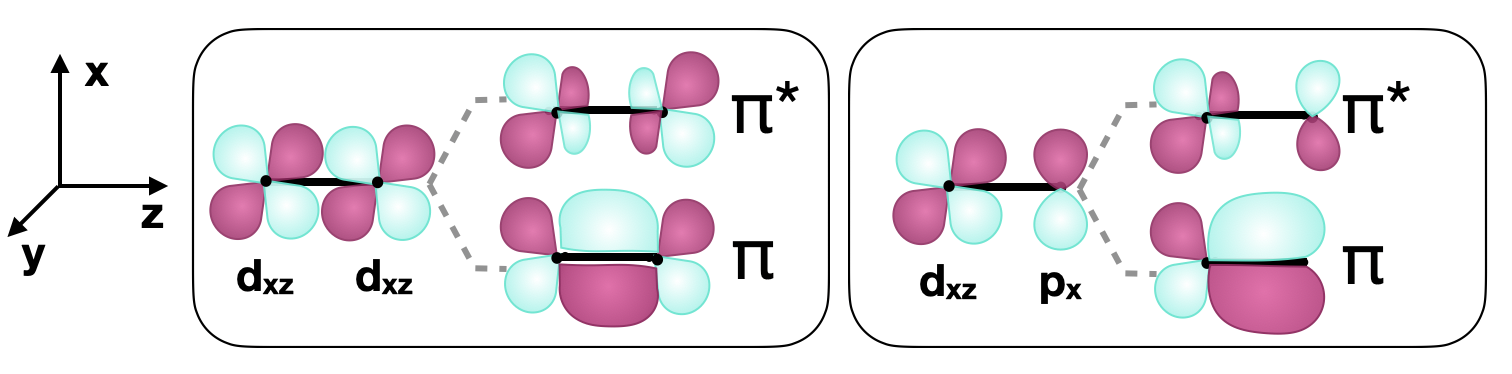
\(\pi\)зв'язки - це ті, з одним вузлом, який знаходиться в площині з міжядерної віссю. \(\pi\)Зв'язок може утворюватися між двома\(d\) орбіталями або між\(d\) орбіталями та іншими типами орбіталів з порівнянною симетрією. Прикладом\(\pi\) зв'язку між двома\(d\) орбіталями є те, що утворено двома\(d_{xz}\) орбіталями уздовж\(z\) осі (показано на малюнку\(\PageIndex{3}\)). \(d\)Орбіталі також можуть утворювати\(\pi\) зв'язки, використовуючи\(p\) орбіталі з сумісною симетрією, як показано на малюнку\(\PageIndex{3}\).
Дельта (\(\delta\)) склеювання з\(d\) орбіталями
\(\delta \)зв'язки - це ті з двома вузлами, які знаходяться в площині з міжядерної віссю. \(\delta\)зв'язки можуть утворюватися між двома\(d\) орбіталями з відповідною симетрією. Наприклад, коли два атоми зв'язуються уздовж\(z\) осі,\(d_{xy}\) орбіталі і дві\(d_{x^2-y^2}\) орбіталі можуть утворювати\(\delta\) зв'язки (рис.\(\PageIndex{4}\)).
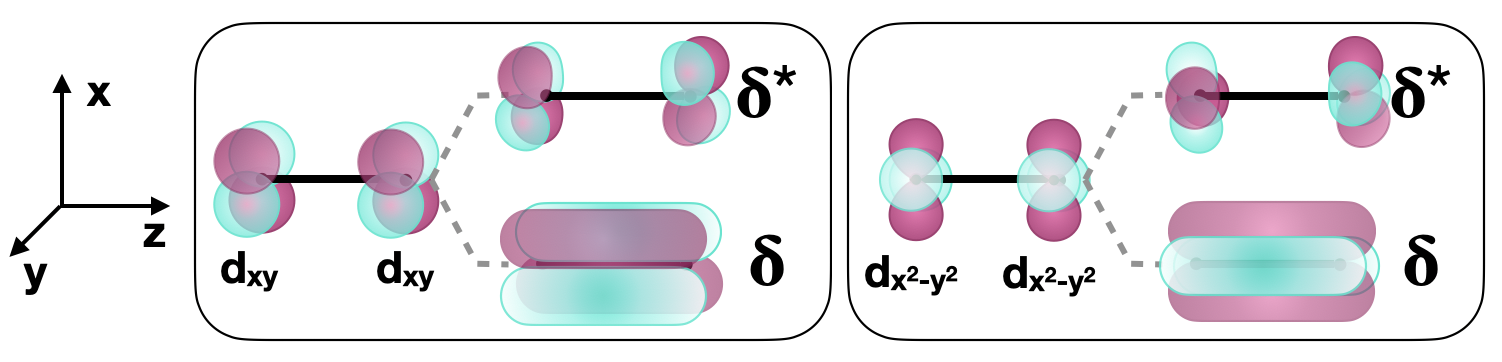
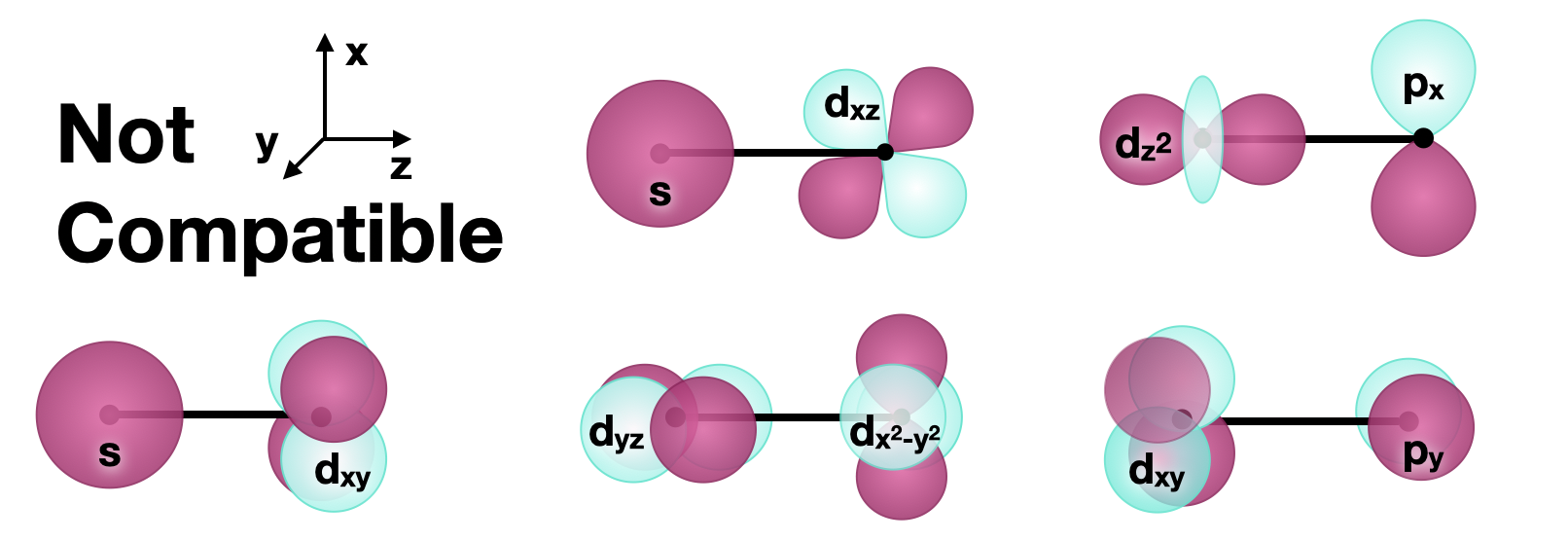
Несумісні орбіталі
У описі вище ми зосередилися на тому, як можуть утворюватися зв'язки (і антибонди) з\(d\) орбіталями. Усі зв'язкові та незв'язні взаємодії вимагають, щоб орбіталі мали сумісну симетрію для формування продуктивних взаємодій. Варто згадати, що орбіталі з симетрією, несумісною з\(d\) орбіталями, не матимуть зв'язуючих або антизв'язуючих взаємодій з\(d\) орбіталями. На малюнку нижче показано кілька наборів орбіталей, несумісних для склеювання.