14.5: Поліпронові кислоти
- Page ID
- 22818
- Розширити раніше введені концепції рівноваги на кислоти та основи, які можуть пожертвувати або приймати більше одного протона
Ми можемо класифікувати кислоти за кількістю протонів на молекулу, які вони можуть віддати в реакції. Кислоти\(\ce{HCl}\), такі як\(\ce{HNO3}\), і\(\ce{HCN}\) які містять один іонізуючий атом водню в кожній молекулі називаються монопротовими кислотами. Їх реакції з водою такі:
\[\ce{HCl}(aq)+\ce{H2O}(l)⟶\ce{H3O+}(aq)+\ce{Cl-}(aq) \nonumber \]
\[\ce{HNO3}(aq)+\ce{H2O}(l)⟶\ce{H3O+}(aq)+\ce{NO3-}(aq) \nonumber \]
\[\ce{HCN}(aq)+\ce{H2O}(l)⟶\ce{H3O+}(aq)+\ce{CN-}(aq) \nonumber \]
Незважаючи на те, що він містить чотири атоми водню, оцтову кислоту\(\ce{CH3CO2H}\), також є монопротичним, оскільки лише атом водню з карбоксильної групи (\(\ce{-COOH}\)) реагує з основами:

Точно так само монопротичні основи - це підстави, які приймуть єдиний протон.
Діпротові кислоти
Дипротові кислоти містять два іонізуваних атома водню на молекулу; іонізація таких кислот відбувається в два етапи. Перша іонізація завжди відбувається в більшій мірі, ніж друга іонізація. Наприклад, сірчана кислота, сильна кислота, іонізує наступним чином:
- Перша іонізація - це
\[ \ce{H2SO4}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{HSO4-}(aq) \nonumber \]
с\(K_{\ce a1} > 10^2;\: {complete\: dissociation}\).
- Друга іонізація - це
\[ \ce{HSO4-}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{SO4^{2−}}(aq) \nonumber \]
с\( K_{\ce a2}=1.2×10^{−2}\).
Цей поетапний процес іонізації відбувається для всіх поліпротових кислот. Коли ми робимо розчин слабкої дипротової кислоти, то отримуємо розчин, який містить суміш кислот. Вугільна кислота\(\ce{H2CO3}\), є прикладом слабкої дипротової кислоти. Перша іонізація вугільної кислоти дає іони гідронію і бікарбонатні іони в невеликих кількостях.
- Перша іонізація
\[\ce{H2CO3}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{HCO3-}(aq) \nonumber \]
із
\[K_{\ce{H2CO3}}=\ce{\dfrac{[H3O+][HCO3- ]}{[H2CO3]}}=4.3×10^{−7} \nonumber \]
Іон бікарбонату також може виступати в якості кислоти. Він іонізує і утворює іони гідронію і карбонатні іони в ще менших кількостях.
- Друга іонізація
\[\ce{HCO3-}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{CO3^2-}(aq) \nonumber \]
із
\[ K_{\ce{HCO3-}}=\ce{\dfrac{[H3O+][CO3^2- ]}{[HCO3- ]}}=4.7×10^{−11} \nonumber \]
\(K_{\ce{H2CO3}}\)більше, ніж\(K_{\ce{HCO3-}}\) в 10 4 рази, тому Н 2 СО 3 є домінуючим продуцентом іона гідронію в розчині. Це означає, що мало що\(\ce{HCO3-}\) утворюється при іонізації Н 2 СО 3 іонізується для отримання іонів гідронію (і карбонатних іонів), а концентрації Н 3 О + і\(\ce{HCO3-}\) практично рівні в чистому водному розчині Н 2 СО 3.
Якщо перша константа іонізації слабкої дипротової кислоти більше другої в рази не менше 20, доцільно обробити першу іонізацію окремо і розрахувати концентрації, отримані в результаті неї, до розрахунку концентрацій видів, що виникають в результаті подальшої іонізації. Це може значно спростити нашу роботу, оскільки з першої іонізації ми можемо визначити концентрацію Н 3 О + і сполучену основу, потім визначити концентрацію кон'югатної основи другої іонізації в розчині з концентраціями, визначеними першою іонізація.
Коли ми купуємо газовану воду (газовану воду), ми купуємо розчин вуглекислого газу у воді. Розчин кислий, оскільки СО 2 реагує з водою з утворенням вугільної кислоти, H 2 CO 3. Які бувають\(\ce{[H3O+]}\)\(\ce{[HCO3- ]}\), і\(\ce{[CO3^2- ]}\) в насиченому розчині СО 2 з початковим [Н 2 СО 3] = 0,033 М?
\[\ce{H2CO3}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{HCO3-}(aq) \hspace{20px} K_{\ce a1}=4.3×10^{−7} \label{step1} \tag{equilibrium step 1} \]
\[\ce{HCO3-}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{CO3^2-}(aq) \hspace{20px} K_{\ce a2}=4.7×10^{−11} \label{step2} \tag{equilibrium step 2} \]
Рішення
Як вказують константи іонізації, H 2 CO 3 є набагато сильнішою кислотою\(\ce{HCO3-}\), ніж, так\(\ce{H2CO3}\) є домінуючим продуцентом іона гідронію в розчині. Таким чином, є дві частини у вирішенні цієї проблеми:
- Використовуючи звичні чотири етапи, визначаємо концентрацію Н 3 О + і\(\ce{HCO3-}\) виробляється іонізацією Н 2 СО 3.
- Потім визначаємо концентрацію\(\ce{CO3^2-}\) в розчині з концентрацією Н 3 О + і\(\ce{HCO3-}\) визначаємо в (1).
Підсумовуємо:
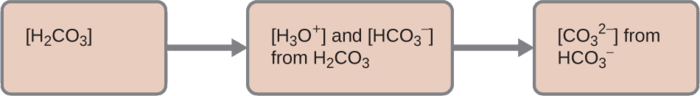
1. Перша іонізація: Визначте концентрації\(\ce{H3O+}\) і\(\ce{HCO3-}\).
Оскільки\ ref {step1} має набагато більше,\(K_{a1}=4.3×10^{−7}\) ніж\(K_{a2}=4.7×10^{−11}\) для\ ref {step2}, ми можемо сміливо ігнорувати другий крок іонізації і зосередитися лише на першому кроці (але вирішити його в наступній частині проблеми).
\[\ce{H2CO3}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{HCO3-}(aq) \hspace{20px} K_{\ce a1}=4.3×10^{−7} \nonumber \]
Що стосується іонізації будь-якої іншої слабкої кислоти:

Скорочена таблиця змін і концентрацій показує:
| Стіл ICE | \(\ce{H2CO3}(aq)\) | \(\ce{H2O}(l)\) | \( \ce{H3O+}(aq) \) | \(\ce{HCO3-}(aq)\) |
|---|---|---|---|---|
| I початковий (M) | \ (\ ce {H2CO3} (q)\)» style="вирівнювання тексту: центр; ">\(0.033 \:M\) | \ (\ ce {H2O} (л)\)» style="вирівнювання тексту: центр; ">- | \ (\ ce {H3O+} (q)\)» style="вирівнювання тексту: центр; ">\(0\) | \ (\ ce {HCO3-} (q)\)» style="вирівнювання тексту: центр; ">\(0\) |
| C Зміна (M) | \ (\ ce {H2CO3} (q)\)» style="вирівнювання тексту: центр; ">\(- x\) | \ (\ ce {H2O} (л)\)» style="вирівнювання тексту: центр; ">- | \ (\ ce {H3O+} (q)\)» style="вирівнювання тексту: центр; ">\(+x\) | \ (\ ce {HCO3-} (q)\)» style="вирівнювання тексту: центр; ">\(+x\) |
| Е рівновага (М) | \ (\ ce {H2CO3} (q)\)» style="вирівнювання тексту: центр; ">\(0.033 \:M - x\) | \ (\ ce {H2O} (л)\)» style="вирівнювання тексту: центр; ">- | \ (\ ce {H3O+} (q)\)» style="вирівнювання тексту: центр; ">\(x\) | \ (\ ce {HCO3-} (q)\)» style="вирівнювання тексту: центр; ">\( x\) |
Підстановка рівноважних концентрацій в константу рівноваги дає нам:
\[K_{\ce{H2CO3}}=\ce{\dfrac{[H3O+][HCO3- ]}{[H2CO3]}}=\dfrac{(x)(x)}{0.033−x}=4.3×10^{−7} \nonumber \]
Вирішення попереднього рівняння, що робить наші стандартні припущення, дає:
\[x=1.2×10^{−4} \nonumber \]
Таким чином:
\[\ce{[H2CO3]}=0.033\:M \nonumber \]
\[\ce{[H3O+]}=\ce{[HCO3- ]}=1.2×10^{−4}\:M \nonumber \]
2. Друга іонізація: Визначте концентрацію \(CO_3^{2-}\)в розчині при рівновазі.
Оскільки\ ref {step1} має набагато більше,\(K_a\) ніж\ ref {step2}, ми можемо умови рівноваги, обчислені з першої частини прикладу, як початкові умови для таблиці ICER для\ ref {step2}:
\[\ce{HCO3-}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{CO3^2-}(aq) \nonumber \]
| Стіл ICE | \(\ce{HCO3-}(aq)\) | \(\ce{H2O}(l)\) | \( \ce{H3O+}(aq) \) | \(\ce{CO3^2-}(aq)\) |
|---|---|---|---|---|
| I початковий (M) | \ (\ ce {HCO3-} (q)\)» style="вирівнювання тексту: центр; ">\(1.2×10^{−4}\:M\) | \ (\ ce {H2O} (л)\)» style="вирівнювання тексту: центр; ">- | \ (\ ce {H3O+} (q)\)» style="вирівнювання тексту: центр; ">\(1.2×10^{−4}\:M\) | \ (\ ce {CO3^2-} (aq)\)» style="вирівнювання тексту: центр; ">\(0\) |
| C Зміна (M) | \ (\ ce {HCO3-} (q)\)» style="вирівнювання тексту: центр; ">\(- y\) | \ (\ ce {H2O} (л)\)» style="вирівнювання тексту: центр; ">- | \ (\ ce {H3O+} (q)\)» style="вирівнювання тексту: центр; ">\(+y\) | \ (\ ce {CO3^2-} (aq)\)» style="вирівнювання тексту: центр; ">\(+y\) |
| Е рівновага (М) | \ (\ ce {HCO3-} (q)\)» style="вирівнювання тексту: центр; ">\(1.2×10^{−4}\:M - y\) | \ (\ ce {H2O} (л)\)» style="вирівнювання тексту: центр; ">- | \ (\ ce {H3O+} (q)\)» style="вирівнювання тексту: центр; ">\(1.2×10^{−4}\:M + y\) | \ (\ ce {CO3^2-} (aq)\)» style="вирівнювання тексту: центр; ">\( y\) |
\[ \begin{align*} K_{\ce{HCO3-}}&=\ce{\dfrac{[H3O+][CO3^2- ]}{[HCO3- ]}} \\[4pt] &=\dfrac{(1.2×10^{−4}\:M + y) (y)}{(1.2×10^{−4}\:M - y)} \end{align*} \nonumber \]
Щоб уникнути розв'язання квадратного рівняння, можна припустити\(y \ll 1.2×10^{−4}\:M \) так
\[K_{\ce{HCO3-}} = 4.7×10^{−11} \approx \dfrac{(1.2×10^{−4}\:M ) (y)}{(1.2×10^{−4}\:M)} \nonumber \]
Перевпорядкування для вирішення\(y\)
\[y \approx \dfrac{ (4.7×10^{−11})(1.2×10^{−4}\:M )}{ 1.2×10^{−4}\:M} \nonumber \]
\[[\ce{CO3^2-}]=y \approx 4.7×10^{−11} \nonumber \]
Підсумовуємо:
У частині 1 цього прикладу ми виявили, що\(\ce{H2CO3}\) в 0,033- М розчин іонізується незначно і при рівновазі\([\ce{H2CO3}] = 0.033\, M\)\([\ce{H3O^{+}}] = 1.2 × 10^{−4}\), і\(\ce{[HCO3- ]}=1.2×10^{−4}\:M\). У частині 2 ми визначили, що\(\ce{[CO3^2- ]}=5.6×10^{−11}\:M\).
Концентрація\(H_2S\) в насиченому водному розчині при кімнатній температурі становить приблизно 0,1 М. Розрахуйте\(\ce{[H3O+]}\)\(\ce{[HS^{−}]}\), і\(\ce{[S^{2−}]}\) в розчині:
\[\ce{H2S}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{HS-}(aq) \hspace{20px} K_{\ce a1}=8.9×10^{−8} \nonumber \]
\[\ce{HS-}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{S^2-}(aq) \hspace{20px} K_{\ce a2}=1.0×10^{−19} \nonumber \]
- Відповідь
-
\([\ce{H2S}] = 0.1 M\),\(\ce{[H3O+]} = [HS^{−}] = 0.0001\, M\),\([S^{2−}] = 1 × 10^{−19}\, M\)
Відзначимо, що концентрація сульфідного іона така ж, як і К а2. Це пов'язано з тим, що кожна наступна дисоціація відбувається в меншій мірі (так як кислота слабшає).
трипротинові кислоти
Трипротова кислота - це кислота, яка має три дисоціативних протони, які піддаються ступінчастої іонізації: Фосфорна кислота - типовий приклад:
- Перша іонізація - це
\[\ce{H3PO4}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{H2PO4-}(aq) \nonumber \]
с\(K_{\ce a1}=7.5×10^{−3} \).
- Друга іонізація - це
\[\ce{H2PO4-}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{HPO4^2-}(aq) \nonumber \]
с\( K_{\ce a2}=6.2×10^{−8} \).
- Третя іонізація -
\[\ce{HPO4^2-}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{PO4^3-}(aq) \nonumber \]
с\( K_{\ce a3}=4.2×10^{−13} \).
Як і у випадку з дипротовими кислотами, відмінності в константах іонізації цих реакцій говорять нам про те, що на кожному наступному етапі ступінь іонізації значно слабша. Це загальна характеристика поліпротових кислот і послідовні константи іонізації часто відрізняються в рази приблизно від 10 5 до 10 6. Цей набір з трьох реакцій дисоціації може здатися ускладненням розрахунків рівноважних концентрацій у розчині H 3 PO 4. Однак, оскільки послідовні константи іонізації відрізняються на коефіцієнт від 10 5 до 10 6, розрахунки можуть бути розбиті на ряд частин, аналогічних тим, що для дипротових кислот.
Поліпротичні підстави можуть приймати більше одного іона водню в розчині. Карбонатний іон є прикладом дипротовой основи, оскільки він може приймати до двох протонів. Розчини карбонатів лужних металів досить лужні, обумовлені реакціями:
\[\ce{H2O}(l)+\ce{CO3^2-}(aq)⇌\ce{HCO3-}(aq)+\ce{OH-}(aq) \nonumber \]
і
\[\ce{H2O}(l)+\ce{HCO3-}(aq)⇌\ce{H2CO3}(aq)+\ce{OH-}(aq) \nonumber \]
Резюме
Кислота, яка містить більше одного іонізуючого протона, - це поліпротова кислота. Протони цих кислот іонізуються поетапно. Відмінності в константах іонізації кислоти для послідовних іонізацій протонів в поліпротовій кислоті зазвичай варіюються приблизно на п'ять порядків. Поки різниця між послідовними значеннями К а кислоти більше приблизно в 20 разів, доцільно розбити розрахунки концентрацій іонів в розчині на ряд етапів.
Глосарій
- діпротова кислота
- кислота, що містить два іонізуваних атома водню на молекулу. Дипротова кислота іонізується в два етапи
- діпротична основа
- база, здатна приймати два протони. Протони приймаються в два етапи
- монопротова кислота
- кислота, що містить один іонізуючий атом водню на молекулу
- ступінчаста іонізація
- процес, в якому кислота іонізується, втрачаючи протони послідовно
- трипротова кислота
- кислота, яка містить три іонізуваних атома водню на молекулу; іонізація трипротових кислот відбувається в три етапи
