7.3: Водень зв'язування та вода
- Page ID
- 19195
- Визначте три особливі властивості води, які роблять її незвичною для молекули її розміру, і поясніть, як вони виникають внаслідок водневого зв'язку.
- Поясніть, що мається на увазі під водневим зв'язком і молекулярні структурні особливості, які його викликають.
- Опишіть «структуру», як вона є, рідкої води.
- Намалюйте структурні приклади водневого зв'язку в трьох малих молекулах, відмінних від H 2 O.
- Опишіть ролі водневого зв'язку в білках і в ДНК.
Більшість студентів хімії швидко вчаться співвідносити будову молекули з її загальними властивостями. Таким чином, ми зазвичай очікуємо, що малі молекули утворюють гази або рідини, а великі - як тверді речовини в звичайних умовах. І тоді ми підходимо до Н 2 О, і в шоці виявляємо, що багато з прогнозів далеко, і що вода (і, як наслідок, саме життя) навіть не повинна існувати на нашій планеті! У цьому розділі ми дізнаємося, чому ця крихітна комбінація з трьох ядер і десяти електронів має особливі властивості, які роблять його унікальним серед більш ніж 15 мільйонів хімічних видів, які ми зараз знаємо.
У воді кожне водневе ядро ковалентно пов'язане з центральним атомом кисню парою електронів, які діляться між ними. У Н 2 О для цієї мети використовуються лише два з шести електронів кисню зовнішньої оболонки, залишаючи чотири електрони, які організовані в дві незв'язні пари. Чотири електронні пари, що оточують кисень, як правило, розташовуються якомога далі один від одного, щоб мінімізувати відштовхування між цими хмарами негативного заряду. Зазвичай це призведе до чотиригранної геометрії, в якій кут між електронними парами (і, отже, кут зв'язку H-O-H) становить 109,5°. Однак, оскільки дві пари, що не зв'язуються, залишаються ближче до атома кисню, вони надають сильніше відштовхування від двох пар ковалентного зв'язку, ефективно штовхаючи два атоми водню ближче один до одного. Результатом є спотворене чотиригранне розташування, в якому кут H—O—H становить 104,5°.
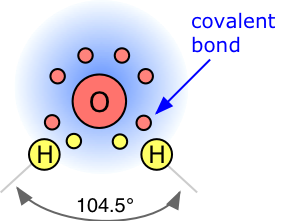
Великий дипольний момент води призводить до водневого зв'язку
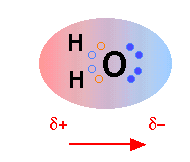
Молекула Н 2 О електрично нейтральна, але позитивний і негативний заряди розподілені не рівномірно. Це ілюструється градацією за кольором на принциповій схемі тут. Електронний (негативний) заряд зосереджений на кисневому кінці молекули, частково завдяки незв'язним електронам (тверді сині кола) та високому ядерному заряду кисню, який надає сильніші притягання до електронів. Це переміщення заряду являє собою електричний диполь, представлений стрілкою внизу; ви можете думати про цей диполь як про електричне «зображення» молекули води.
Протилежні заряди приваблюють, тому не дивно, що негативний кінець однієї молекули води, як правило, орієнтується так, щоб бути близьким до позитивного кінця іншої молекули, яка, як трапляється, знаходиться поруч. Сила цього дипольно-дипольного тяжіння менше, ніж у звичайного хімічного зв'язку, і тому вона повністю перевантажена звичайними тепловими рухами в газовій фазі. Однак, коли молекули Н 2 О переповнені разом в рідині, ці сили привабливості надають дуже помітний ефект, який ми називаємо (дещо оманливо) водневим зв'язком. А при температурах, досить низьких, щоб відключити руйнівний вплив теплових рухів, вода замерзає в лід, в якому водневі зв'язки утворюють жорстку і стійку мережу.
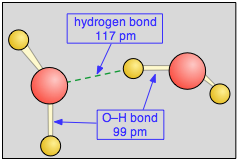
Зверніть увагу, що водневий зв'язок (показаний пунктирною зеленою лінією) дещо довший, ніж ковалентний зв'язок O—H. Він також набагато слабший, близько 23 кДж моль —1 порівняно з міцністю ковалентного зв'язку O—H 492 кДж моль —1.
Сорок одна аномалія води» — деякі з них досить езотеричні.
З давніх-давен відомо, що вода проявляє безліч фізичних властивостей, які відрізняють її від інших дрібних молекул порівнянної маси. Хоча хіміки називають це «аномальними» властивостями води, вони аж ніяк не таємничі; всі цілком передбачувані наслідки того, як розмір і ядерний заряд атома кисню змовляються на спотворення хмар електронного заряду атомів інших елементів, коли вони хімічно зв'язаний з киснем.

Точка кипіння
Найбільш очевидною особливістю води є її дуже висока температура кипіння для такої світлої молекули. Рідкий метан CH 4 (молекулярна маса 16) закипає при -161°С, як видно з цієї діаграми, екстраполяція точок кипіння різних сполук водню групи 16 до Н 2 О свідчить про те, що ця речовина повинна бути газом в нормальних умовах.
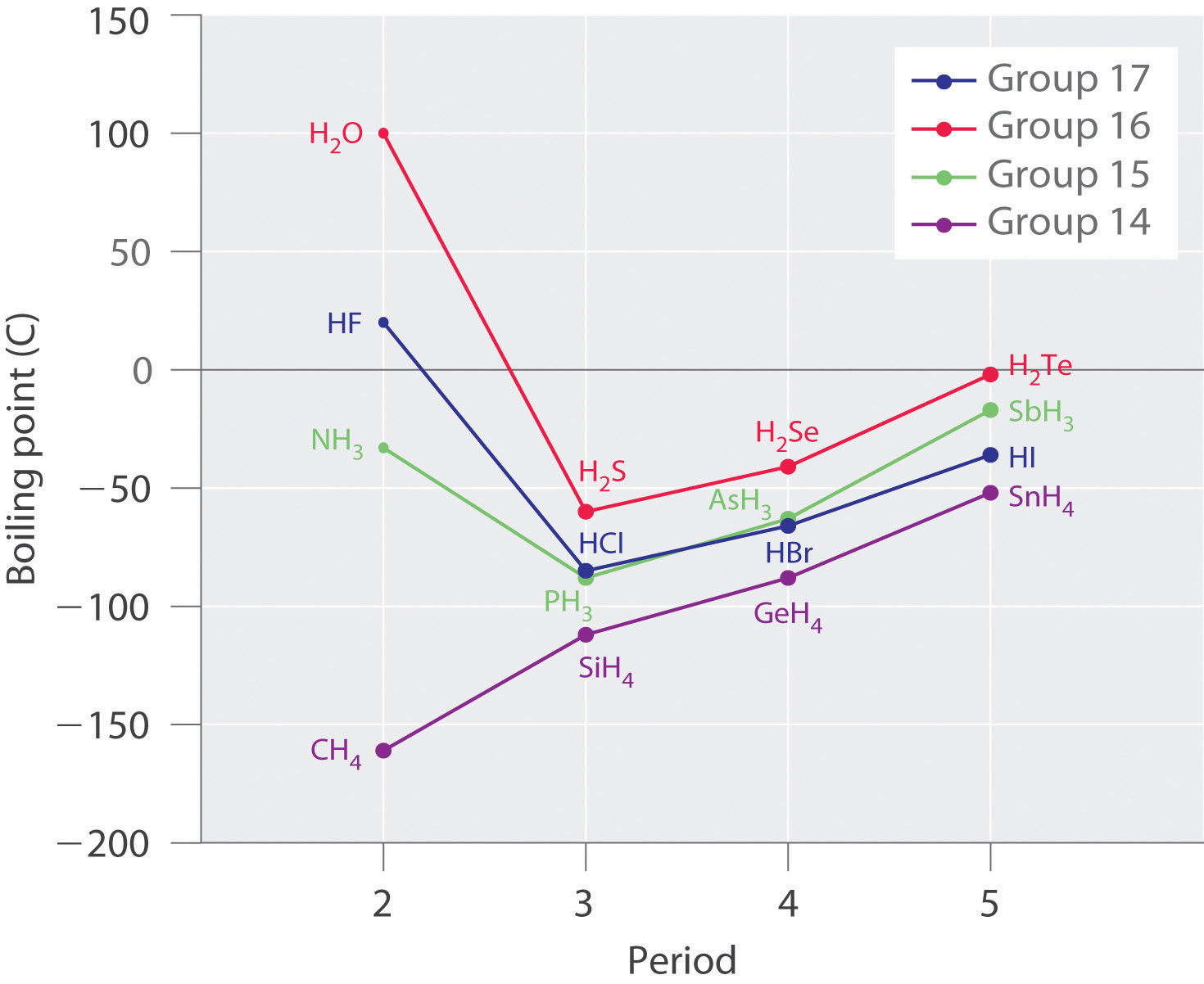
Поверхневий натяг
У порівнянні з більшістю інших рідин вода також має високий поверхневий натяг. Ви коли-небудь спостерігали, як комаха гуляє по поверхні ставка? Водний стридер користується тим, що водна поверхня діє як еластична плівка, яка чинить опір деформації при розміщенні на ній невеликої ваги. (Якщо ви обережні, ви також можете «спливати» невелику скріпку або сталевий штапель на поверхні води в чашці.) Це все завдяки поверхневому натягу води. Молекула в основній масі рідини відчуває притягання до сусідніх молекул у всіх напрямках, але оскільки вони середні до нуля, на молекулу немає чистої сили. Для молекули, яка опиняється на поверхні, ситуація зовсім інша, вона відчуває сили тільки вбік і вниз, і саме це і створює ефект розтягнутої мембрани.

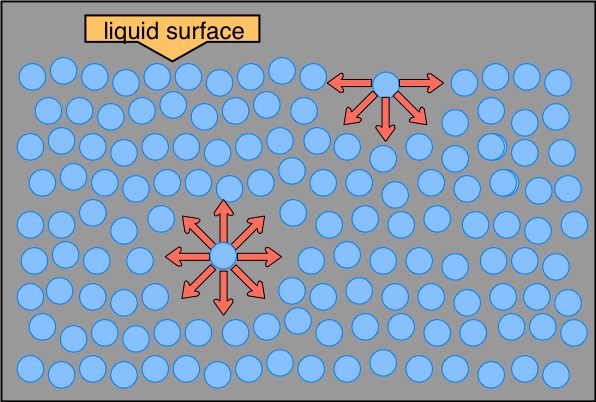
Різниця між молекулами, розташованими на поверхні, і тими, що глибоко всередині, особливо помітна в H 2 O, завдяки сильним силам зв'язку водню. Різниця між силами, які відчуває молекула на поверхні, і одна в об'ємній рідині, породжує поверхневий натяг рідини. Цей малюнок виділяє дві молекули H 2 O, одну на поверхні, а іншу в основній масі рідини. Поверхнева молекула притягується до своїх сусідів знизу та в обидві сторони, але немає пам'яток, що вказують на кут твердого кута 180° над поверхнею. Як наслідок, молекула на поверхні буде прагнути втягуватися в основну частину рідини. Але так як завжди повинна бути якась поверхня, загальний ефект полягає в тому, щоб мінімізувати площу поверхні рідини.
Геометрична форма, яка має найменше відношення площі поверхні до об'єму, - це сфера, тому дуже малі кількості рідин мають тенденцію утворювати сферичні краплі. Коли краплі стають більшими, їх вага деформує їх у типову форму сльози.

Лід плаває на воді
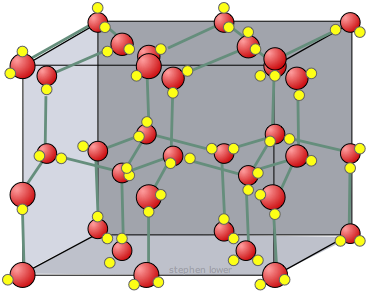
Найбільш енергетично сприятливою конфігурацією молекул Н 2 О є та, в якій кожна молекула пов'язана з воднем з чотирма сусідніми молекулами. Завдяки описаним вище тепловим рухам цей ідеал ніколи не досягається в рідині, але коли вода замерзає до льоду, молекули осідають саме в такому вигляді розташування в кристалі льоду. Це розташування вимагає, щоб молекули були дещо далі один від одного, ніж це було б інакше; як наслідок, лід, в якому водневий зв'язок знаходиться на максимумі, має більш відкриту структуру, і, отже, меншу щільність, ніж вода.
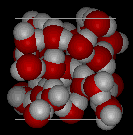
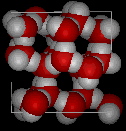
Тут представлені тривимірні види типової місцевої структури води (зліва) і льоду (праворуч.) Зверніть увагу на більшу відкритість структури льоду, яка необхідна для забезпечення найсильнішого ступеня водневого зв'язку в однорідній, розширеній кристалічній решітці. Більш переповнене і переповнене розташування в рідкій воді може бути витримано лише більшою кількістю теплової енергії, доступною вище точки замерзання.
Коли лід тане, більш енергійний тепловий рух порушує більшу частину структури, пов'язаної з воднем, дозволяючи молекулам щільніше упаковувати. Вода, таким чином, є одним з дуже небагатьох речовин, тверда форма яких має меншу щільність, ніж рідина в точці замерзання. Однак локалізовані кластери водневих зв'язків все ще залишаються; вони постійно руйнуються та реформуються, коли теплові рухи коливаються і штовхають окремі молекули. У міру підвищення температури води вище замерзання протяжність і тривалість життя цих скупчень зменшуються, тому щільність води збільшується.
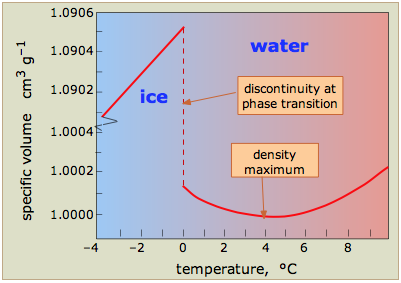
При більш високих температурах починає домінувати інший ефект, загальний для всіх речовин: зі збільшенням температури зростає і амплітуда теплових рухів. Це більш енергійне штовхання призводить до збільшення середньої відстані між молекулами, зменшуючи щільність рідини; це звичайне теплове розширення.
Оскільки два конкуруючі ефекти (водневе зв'язування при низьких температурах і теплове розширення при більш високих температурах) обидва призводять до зменшення щільності, з цього випливає, що повинна бути певна температура, при якій щільність води проходить максимум. Ця температура становить 4° C; це температура води, яку ви знайдете на дні покритого льодом озера, в якому ця найщільніша з усіх вод витіснила холоднішу воду і підштовхнула її ближче до поверхні.
Структура рідкої води
Природа рідкої води і те, як організовані і взаємодіють молекули H 2 O всередині неї - це питання, які викликають інтерес хіміків протягом багатьох років. Напевно, немає рідини, яка отримала більш інтенсивне вивчення, і зараз існує величезна література на цю тему. Добре встановлені такі факти:
- Молекули H 2 O притягують один одного за допомогою особливого типу дипольно-дипольної взаємодії, відомого як водневий зв'язок
- водневий скупчення, в якому чотири H 2 Os розташовані по кутах уявного тетраедра є особливо сприятливою (низькопотенційної енергії) конфігурації, але...
- молекули зазнають швидких теплових рухів за часовою шкалою пікосекунд (10-12 секунд), тому термін служби будь-якої конкретної кластерної конфігурації буде швидким.
Різноманітні методи, включаючи інфрачервоне поглинання, розсіювання нейтронів та ядерний магнітний резонанс, були використані для зондування мікроскопічної структури води. Інформація, отримана в результаті цих експериментів та теоретичних розрахунків, призвела до розробки близько двадцяти «моделей», які намагаються пояснити структуру та поведінку води. Зовсім недавно для вивчення того, наскільки добре ці моделі здатні передбачати спостережувані фізичні властивості води, були використані комп'ютерне моделювання різного роду.
Ця робота призвела до поступового уточнення наших поглядів на структуру рідкої води, але вона не дала жодної остаточної відповіді. Цьому є кілька причин, але головна з них полягає в тому, що саме поняття «будова» (і водних «скупчень») залежить як від розглянутих часових рамок, так і від обсягу. Таким чином, до сих пір відкриті питання наступних видів:
- Як відрізнити члени «скупчення» від сусідніх молекул, яких немає в цьому кластері?
- Оскільки окремі водневі зв'язки постійно розриваються та формуються за пікосекундною шкалою часу, чи мають водні кластери значуще існування протягом більш тривалих періодів часу? Іншими словами, кластери є перехідними, тоді як «структура» передбачає молекулярне розташування, яке є більш міцним. Чи можемо ми тоді законно використовувати термін «кластери» при описі структури води?
- Можливі місця розташування сусідніх молекул навколо даного H 2 O обмежені енергійними та геометричними міркуваннями, що породжує певну кількість «структури» в межах будь-якого елемента малого обсягу. Незрозуміло, однак, в якій мірі ці структури взаємодіють у міру збільшення розміру об'ємного елемента. І як уже згадувалося вище, в якій мірі ці структури підтримуються протягом періодів довше декількох пікосекунд?
У 1950-х роках передбачалося, що рідка вода складається з суміші пов'язаних з воднем кластерів (H 2 O) n, в яких n може мати найрізноманітніші значення, але мало доказів існування таких агрегатів ніколи не було знайдено. Нинішній погляд, підтримуваний комп'ютерним моделюванням та спектроскопією, полягає в тому, що за дуже коротких часових масштабів вода більше схожа на «гель», що складається з одного величезного скупчення, пов'язаного з воднем. За шкалою часу 10-12 -10 -9 сек обертання та інші теплові рухи призводять до розриву та повторного формування окремих водневих зв'язків у нових конфігураціях, викликаючи постійно мінливі локальні розриви, ступінь та вплив яких залежать від температури та тиску.
Лід
Лід, як і всі тверді речовини, має чітко визначену структуру; кожна молекула води оточена чотирма сусідніми Н 2 Os. два з них пов'язані з атомом кисню на центральній молекулі H 2 O, і кожен з двох атомів водню аналогічно пов'язаний з іншим сусіднім Н 2 О.
Лід утворює кристали, що мають гексагональну гратчасту структуру, які в повному розвитку мають тенденцію утворювати гексагональні призми, дуже схожі на ті, які іноді спостерігаються в кварці. Це іноді трапляється, і кожен, хто зробив багато зимового альпінізму, швидше за все, бачив іглоподібні призми кристалів льоду, що плавають у повітрі. Однак у більшості умов кристали сніжинки, які ми бачимо, сплющуються в красиві фрактальні гексагональні структури, які зазвичай спостерігаються.
Сніжинки
Молекули H 2 O, що складають верхню і нижню площину граней призми, упаковані дуже тісно і пов'язані (через водневий зв'язок) з молекулами всередині. На відміну від цього, молекули, що складають сторони призми, і особливо ті, що знаходяться в гексагональних кутах, набагато більш оголені, так що атмосферні молекули H 2 O, які контактують з більшістю місць на поверхні кристалів, прикріплюються дуже вільно і мігрують уздовж неї, поки не зможуть утворювати водородні кріплення до цих кутів, тим самим стаючи частиною твердого тіла і розширюючи конструкцію вздовж цих шести напрямків. Цей процес увічнює себе, оскільки нові розширення самі набувають шестикутну структуру.
Чому лід слизький?
При температурі до 200 К поверхня льоду сильно невпорядкована і схожа на воду. Коли температура наближається до точки замерзання, ця область розладу поширюється далі вниз від поверхні і діє як мастило.
Ілюстрація взята зі статті у випуску C&EN від 7 квітня 2008 року на честь фізичного хіміка Габора Соморджая, який став першопрохідцем сучасних методів дослідження поверхонь.
«Чиста» вода
Для хіміка термін «чистий» має значення тільки в контексті конкретного застосування або процесу. Дистильована або деіонізована вода, яку ми використовуємо в лабораторії, містить розчинені атмосферні гази та іноді деяку кількість кремнезему, але їх невелика кількість та відносна інертність роблять ці домішки незначними для більшості цілей. Коли вода найвищої досяжної чистоти потрібна для певних типів вимогливих вимірювань, її зазвичай фільтрують, деіонізують та дистилюють з потрійним вакуумом. Але навіть ця «хімічно чиста» вода є сумішшю ізотопних видів: існує два стабільних ізотопу як водню (Н 1 і Н 2, останній часто позначається D), так і кисню (О 16 і О 18), які породжують такі комбінації, як H 2 O 18 , HDO 16 тощо, всі з яких легко ідентифікуються в інфрачервоних спектрах водяної пари. І на довершення цього два атоми водню у воді містять протони, магнітні моменти яких можуть бути паралельними або антипаралельними, що породжує орто- та пара-воду відповідно. Дві форми, як правило, присутні в o/p співвідношенні 3:1.
Кількість рідкісних ізотопів кисню і водню у воді досить варіюється від місця до місця, що тепер можна визначити вік і джерело конкретного зразка води з певною точністю. Ці відмінності відображаються в ізотопних профілі H і O організмів. Таким чином, ізотопний аналіз людського волосся може бути корисним інструментом для розслідувань злочинів та антропологічних досліджень.
Детальніше про водневе зв'язування
Водневі зв'язки утворюються, коли електронна хмара атома водню, який прикріплений до одного з більш електронегативних атомів, спотворюється цим атомом, залишаючи частковий позитивний заряд на водні. Завдяки дуже малим розмірам атома водню щільність цього часткового заряду досить велика, щоб дозволити йому взаємодіяти з електронами однієї пари на сусідньому електронегативному атомі. Хоча водневий зв'язок зазвичай описується як форма дипольно-дипольного тяжіння, тепер зрозуміло, що воно передбачає певну міру обміну електронів (між зовнішніми незв'язними електронами та воднем), тому ці зв'язки мають певний ковалентний характер.
Водневі зв'язки довші, ніж звичайні ковалентні зв'язки, і вони також слабкіші. Експериментальні докази водневого зв'язку зазвичай походять від рентгенівських дифракційних досліджень на твердих тілах, які виявляють менші, ніж нормальні відстані між воднем та іншими атомами.
Водень зв'язку в малих молекулах
Наступні приклади показують щось із широкого спектру водневого зв'язку в молекулах.
| Аміак (mp -78, bp -33°C) пов'язаний з воднем у рідкому і твердому станах. | |
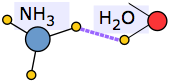 |
Водневий зв'язок відповідає за надзвичайно високу розчинність аміаку у воді. |
| Багато органічні (карбонові) кислоти утворюють водневі димери в твердому стані. | |
| Тут акцептором водневого зв'язку є π електронна хмара бензольного кільця. Цей тип взаємодії важливий в підтримці форми білків. | |
|
Фтористий водень (mp —92, bp 33°C) - ще одна поширена речовина, яка сильно пов'язана з воднем у конденсованих фазах. |
|
| Біфторидний іон (для якого не може бути записана належна структура Льюїса) можна розглядати як складний іон, що утримується найміцнішим водневим зв'язком, відомим: близько 155 кДж моль —1. | |
Водневе зв'язування в біополімерах
Водневе зв'язування відіграє важливу роль у природних полімерах біологічного походження двома способами:
- водневий зв'язок між сусідніми полімерними ланцюгами (міжмолекулярне склеювання);
- Водневий зв'язок між різними частинами одного ланцюга (внутрішньомолекулярне склеювання);
- Водневе зв'язування молекул води з —OH групами на полімерному ланцюзі («зв'язана вода»), що допомагає підтримувати форму полімеру.
Наступні приклади є репрезентативними для декількох типів біополімерів.
Целюлоза
Целюлоза - лінійний полімер глюкози (див. Вище), що містить від 300 до понад 10 000 одиниць, залежно від джерела. Як основний структурний компонент рослин (поряд з лігніном на деревах), клітковина є найбільш поширеною органічною речовиною на землі. Роль водневого зв'язку полягає в тому, щоб зшивати окремі молекули для створення аркушів, як показано тут. Ці листи, ніж складаються в шаховому масиві, що утримуються воєдино ван дер Ваальса сил. Подальше водневе склеювання сусідніх штабелів зв'язує їх між собою в більш міцну і жорстку конструкцію.
Білки
Ці полімери, виготовлені з амінокислот R—CH (NH 2) COOH, залежать від внутрішньомолекулярного водневого зв'язку для підтримки їх форми (вторинної та третинної структури), що є важливим для їх важливої функції як біологічних каталізаторів (ферментів). Вбудовані в білок молекули води, пов'язані з воднем, також важливі для їх структурної цілісності.
Основний водневий зв'язок в білках знаходиться між -N—H групами «аміно» частин з -C=O групами «кислотних» частин. Ці взаємодії породжують два основних типи вторинної структури, яка стосується розташування амінокислотного полімерного ланцюга:
альфа-спіраль[зображення] |
бета-аркуш |
Хоча вуглець зазвичай не вважається особливо електронегативним, водневі зв'язки C—H—X тепер також відомі як значні в білках.
ДНК (дезоксирибонуклеїнова кислота)
Хто ви є, повністю залежить від водневих зв'язків! ДНК, як ви, напевно, знаєте, є найвідомішим з біополімерів завдяки своїй центральній ролі у визначенні структури та функції всіх живих організмів. Кожна нитка ДНК побудована з послідовності чотирьох різних нуклеотидних мономерів, що складаються з дезоксирибозного цукру, фосфатних груп і азотистої основи, умовно ідентифікованої буквами A, T, C і G. сама ДНК складається з двох з них полінуклеотидні ланцюги, які згорнуті навколо загальної осі в конфігурації щось на зразок білкової альфа-спіралі, зображеної вище. Цукрово-фосфатні магістралі знаходяться зовні так, що нуклеотидні основи знаходяться зсередини і звернені один до одного. Дві нитки утримуються разом водневими зв'язками, які пов'язують атом азоту нуклеотиду в одному ланцюжку з азотом або киснем на нуклеотиді, який знаходиться навпроти нього на іншому ланцюгу.

Ефективне водневе з'єднання в цій конфігурації може відбуватися лише між парами A-T та C-G, тому ці дві взаємодоповнюючі пари складають «алфавіт», який кодує генетичну інформацію, яка транскрибується щоразу, коли будуються нові білкові молекули. Молекули води, пов'язані з воднем із зовнішніми частинами спіралі ДНК, допомагають стабілізувати її.
