17.1: Прелюдія до електрохімії
- Page ID
- 23730
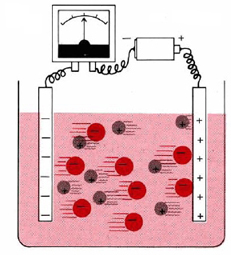
Також можливе вироблення потоку електрики в результаті спонтанної хімічної реакції. Хімічна система, яка може спричинити потік струму таким чином, називається гальванічним елементом або вольтаїчним елементом. Прикладом гальванічного елемента, з яким ви майже напевно знайомі, є акумуляторний ліхтар. Оскільки електричний струм - це потік електронів або інших заряджених частинок, не повинно дивуватися, що як електролітичні, так і гальванічні елементи включають окислювально-відновні реакції.
В електролітичній комірці електрична енергія, що подається від зовнішнього джерела, викликає неспонтанну реакцію. Гальванічний (або вольтаїчний) елемент, з іншого боку. використовує спонтанну реакцію для вироблення електричного струму. У будь-якому виді осередків електрод, при якому відбувається окислення, називається анодом, а електрод, при якому відбувається відновлення, - катодом.
Електролітичні клітини мають численні комерційні застосування. Хлор, гідроксид натрію, водень, алюміній, магній, натрій, кальцій та мідь високої чистоти є одними з найважливіших хімічних речовин, що утворюються електролізом. Гальванічне покриття металів, таких як хром, срібло, нікель, цинк та олово, також є досить важливим. У будь-якій реакції електролізу кількість споживаної або виробленої речовини може бути пов'язане з електричним зарядом, який проходить через комірку за допомогою постійної Фарадея F, яка дорівнює 9,649 × 10 4 С моль —1.
Гальванічний елемент може бути представлений скороченим позначенням, таким як
\[ \text{Zn}│\text{Zn}^{2+} (1\; M)║ \text{Ag}^{2+}(1\; M)│\text{Ag} \label{1} \]
Коли комірка записується таким чином,\( \dfrac{1}{2} \) завжди передбачається, що лівий електрод є анодом і там відбувається напіврівняння окислення. Потім правий електрод повинен бути прийнятий за катод, і передбачається, що там відбувається зменшення напіврівняння. Реакція клітини - це сума цих двох піврівнянь. Якщо він спонтанний, наші припущення про аноді зліва і катоді праворуч були правильними. Електрони будуть вимушені у зовнішній ланцюг зліва, а ЕРС клітини приймається позитивною. Якщо реакція клітини, написана за вищевказаною конвенцією, виявиться неспонтанною, то її зворотний буде спонтанним. Наші припущення про те, який електрод є анодом, а який катод теж повинен бути зворотним, а ЕРС осередку дається негативний знак.
\(\ref{1}\)Рівняння - це дуже весело. Оскільки значення ЕРС клітини вказують на те, чи є процес спонтанним, вони є досить корисними. Вони є адитивними і умовно повідомляються як стандартні електродні потенціали. Вони відносяться до ЕРС комірки з газовоневим електродом зліва і електрода, потенціал якого повідомляється праворуч. Стандартний електродний потенціал безпосередньо пов'язаний зі стандартною зміною вільної енергії для реакції, що дозволяє безпосередньо визначити Δ G°.
Багато гальванічні елементи мають комерційне значення. До них відносяться сухі клітини, ртутні клітини, акумуляторні батареї Ni-Cd та свинцеві акумулятори. Паливні елементи, в які подається безперервна подача як окислювача, так і відновника, з часом можуть стати важливими через їх високу ефективність.
