6.4: Сили в рішеннях
- Дізнайтеся деяку термінологію, що включає рішення.
- Поясніть значимість висловлювання «подібне розчиняється як».
- Поясніть, чому ті чи інші речовини розчиняються в інших речовині.
Розчин - ще одна назва однорідної суміші. Суміш як матеріал, що складається з двох і більше речовин. У рішенні комбінація настільки інтимна, що

різні речовини неможливо диференціювати по зору, навіть за допомогою мікроскопа. Порівняйте, наприклад, суміш солі і перцю і іншу суміш, що складається з солі і води. У першій суміші ми можемо легко побачити окремі крупинки солі і цятки перцю. Суміш солі і перцю - це не розчин. Однак у другій суміші, як би уважно ми не дивилися, ми не можемо побачити двох різних речовин. Сіль, розчинена у воді, є розчином.
Основний компонент розчину, який називається розчинником, зазвичай є тією ж фазою, що і сам розчин. Кожен незначний компонент розчину (а їх може бути більше одного) називається розчиненою речовиною. У більшості рішень, які ми опишемо в цьому підручнику, не буде двозначності щодо того, чи є компонент розчинником або розчиненою речовиною.) Наприклад, в розчині солі у воді розчиненою речовиною є сіль, а розчинник - вода Рис6.4.1.
Розчини надходять у всіх фазах, і розчинник і розчинена речовина не повинні перебувати в одній фазі, щоб утворити розчин (наприклад, сіль і вода). Наприклад, повітря являє собою газоподібний розчин приблизно 80% азоту і близько 20% кисню, при цьому деякі інші гази присутні в набагато менших кількостях. Сплав являє собою твердий розчин, що складається з металу (як заліза) з розчиненими в ньому деякими іншими металами або неметалами. Сталь, сплав заліза і вуглецю і невеликі кількості інших металів, є прикладом твердого розчину. У таблиці6.4.1 наведено деякі поширені типи рішень, з прикладами кожного.
| Фаза розчинника | Розчинена фаза | Приклад |
|---|---|---|
| газ | газ | повітря |
| рідкий | газ | газовані напої |
| рідкий | рідкий | етанол (C 2 H 5 OH) в H 2 O (алкогольні напої) |
| рідкий | твердий | солона вода |
| твердий | газ | H 2 газ поглинається металом Pd |
| твердий | рідкий | Hg () в зубних пломбах |
| твердий | твердий | сталеві сплави |
Розчин роблять шляхом розчинення 1,00 г сахарози (C12H22O11) в 100,0 г рідкої води. Визначте розчинник і розчинений в отриманому розчині.
Рішення
Або за масою, або по родимках очевидним незначним компонентом є сахароза, тому вона є розчиненою речовиною. Вода - основна складова - це розчинник. Той факт, що отриманий розчин є тією ж фазою, що і вода, також говорить про те, що розчинником є вода.
Розчин виготовляють шляхом розчинення 3,33 гHCl(g) в 40,0 г рідкого метилового спирту (CH3OH). Визначте розчинник і розчинений в отриманому розчині.
- Відповідь
-
розчинна речовина: HCl (г); розчинник: СН 3 ОН
Як розчиняється, як
Простим способом передбачити, які сполуки будуть розчинятися в інших сполуках, є фраза «як розчиняється, як». Це означає, що полярні сполуки розчиняють полярні сполуки, неполярні сполуки розчиняють неполярні сполуки, але полярні і неполярні не розчиняються один в одному.
Навіть деякі неполярні речовини розчиняються у воді, але лише в обмеженій мірі. Ви коли-небудь замислювалися, чому риби здатні дихати? Кисневий газ, неполярні молекули, розчиняються у воді, і саме цей кисень риби приймають через свої зябра. Або ще один приклад неполярної сполуки, яка розчиняється у воді, є причиною того, що ми можемо насолоджуватися газованими газованими напоями. Пепсі-кола і всі інші газовані напої мають вуглекислий газCO2, неполярне з'єднання, розчинене в цукрово-водному розчині. При цьому, щоб зберегти якомога більше газу в розчині, газовані напої витримують під тиском.
Ця загальна тенденція «як розчиняється, як» узагальнена в наступній таблиці:
| Розчинена речовина | Розчинник | Чи формується розчин? |
|---|---|---|
| Полярний ковалентний | Полярний | так |
| неполярний ковалентний | неполярний | так |
| Полярний ковалентний | неполярний | ні |
| неполярний ковалентний | Полярний | ні |
| Іонні | Полярний | так |
| Іонні | неполярний | ні |
Зверніть увагу, що кожен раз при змішуванні заряджених частинок (іонних сполук або полярних речовин) утворюється розчин. Коли частинки без зарядів (неполярні сполуки) змішуються, вони утворюють розчин. Однак якщо речовини з зарядами змішуються з іншими речовинами без зарядів, розчин не утворюється.
Коли іонна сполука вважається «нерозчинною», це не обов'язково означає, що сполука повністю недоторкана водою. Всі іонні сполуки в тій чи іншій мірі розчиняються. Нерозчинна сполука просто не розчиняється в будь-якій помітній або помітній кількості.
Що це робить розчинену речовину розчинною в одних розчинниках, але не в інших?
Відповідь - міжмолекулярні взаємодії. Міжмолекулярні взаємодії включають лондонські сили дисперсії, дипольно-дипольні взаємодії та водневий зв'язок (як описано в

попередній розділ). З експериментальних досліджень було визначено, що якщо молекули розчиненої речовини відчувають ті ж міжмолекулярні сили, що і розчинник, розчинена речовина, швидше за все, розчиняється в цьому розчиннику. Отже, NaCl - дуже полярна речовина, оскільки вона складається з іонів - розчиняється у воді, яка є дуже полярною, але не в олії, яка, як правило, неполярна. Неполярний віск розчиняється в неполярному гексані, але не в полярній воді. Рідини, які розчиняються одна в одній у всіх пропорціях, кажуть, що змішуються. Рідини, які не розчиняються одна в одній, називаються незмішуваними.
Малюнок6.4.2 Вода (прозора рідина) і масло (жовта) не утворюють рідких розчинів. (CC BY-SA 1.0 Generic; Віктор Блакус)
Чи був би я 2 більш розчинний у cCl 4 або H 2 O? Поясніть свою відповідь.
Рішення
I 2 неполярний. З двох розчинників cCl 4 є неполярним, а H 2 O є полярним, тому I 2, як очікується, буде більш розчинним у cCl 4.
Чи буде C 3 H 7 OH більш розчинний в CCl 4 або H 2 O? Поясніть свою відповідь.
- Відповідь
-
H 2 O, тому що обидва відчувають водневий зв'язок
Вода вважається полярним розчинником. Які речовини повинні розчинятися у воді?
- метанол (СН 3 ОН)
- сульфат натрію (Na 2 SO 4)
- октан (С 8 Н 18)
Рішення
Оскільки вода полярна, речовини, які є полярними або іонними, розчиняться в ній.
- Через групу OH в метанолі ми очікуємо, що його молекули будуть полярними. Таким чином, ми очікуємо, що він буде розчинний у воді. Оскільки і вода, і метанол є рідинами, слово miscible можна використовувати замість розчинних.
- Сульфат натрію є іонною сполукою, тому ми очікуємо, що він буде розчинний у воді.
- Як і інші вуглеводні, октан неполярний, тому ми очікуємо, що він не буде розчинний у воді.
Толуол (C 6 H 5 CH 3) широко використовується в промисловості як неполярний розчинник. Які речовини повинні розчинятися в толуолі?
- вода (Н 2 О)
- сульфат натрію (Na 2 SO 4)
- октан (С 8 Н 18)
- Відповідь
-
октан (С 8 Н 18) розчиниться. Він також неполярний.
Процес розчинення
Вода зазвичай розчиняє більшість іонних сполук і полярних молекул. Неполярні молекули, такі як ті, що містяться в жирі або олії, не розчиняються у воді. Спочатку ми розглянемо процес, який відбувається, коли іонна сполука, наприклад кухонна сіль (хлорид натрію), розчиняється у воді.
Молекули води рухаються приблизно безперервно за рахунок своєї кінетичної енергії. Коли кристал хлориду натрію поміщається в воду, молекули води стикаються з кристалічною решіткою. Нагадаємо, що кристалічна решітка складається з чергуються позитивних і негативних іонів. Воду приваблює кристал хлориду натрію, оскільки вода полярна; вона має як позитивний, так і негативний кінець. Позитивно заряджені іони натрію в кристалі притягують кисневий кінець молекул води, оскільки вони частково негативні. Негативно заряджені іони хлориду в кристалі притягують водневий кінець молекул води, оскільки вони частково позитивні. Дія полярних молекул води розбирає кристалічну решітку (див. Малюнок нижче).
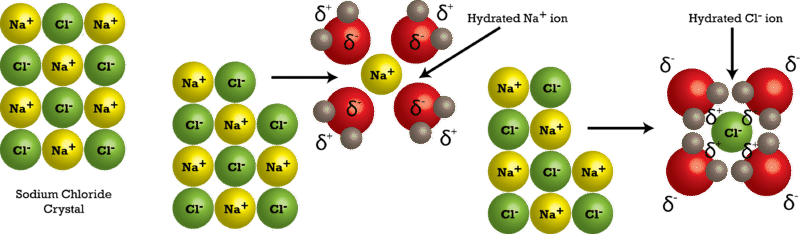
Після виходу з кристала окремі іони потім оточені частинками розчинника в процесі, який називається сольвацією. Зверніть увагу на малюнку вище, що окреміNa+ іони оточені молекулами води з атомом кисню, орієнтованим поблизу позитивного іона. Так само іони хлориду оточені молекулами води з протилежною орієнтацією. Таким чином, утворюються численні іонно-дипольні взаємодії. Гідратація - це процес розчинених частинок, оточених молекулами води, розташованими певним чином. Гідратація допомагає стабілізувати водні розчини, запобігаючи поверненню позитивних і негативних іонів і утворюючи осад.
Столовий цукор виготовляється з молекулярної сполуки сахарози(C12H22O11). Твердий цукор складається з окремих молекул цукру, скріплених між собою міжмолекулярними силами притягування. Коли вода розчиняє цукор, вона відокремлює окремі молекули цукру, порушуючи сили притягання, але не порушує ковалентні зв'язки між атомами вуглецю, водню та кисню. Розчинені молекули цукру також гідратовані. Гідратаційна оболонка навколо молекули сахарози влаштована так, що її частково негативні атоми кисню знаходяться поблизу частково позитивних атомів водню в розчиннику, і навпаки.
Резюме
- Розчини складаються з розчинника (основного компонента) і розчиненої речовини (другорядного компонента).
- «Як розчиняється, як» - це корисне правило для прийняття рішення про те, чи буде розчинена речовина в розчиннику.
- Рідини, які розчиняються одна в одній у всіх пропорціях, кажуть, що змішуються.
- Рідини, які не розчиняються одна в одній, називаються незмішуваними.
- Іонно-дипольні взаємодії утворюються при розчиненні іонних сполук у воді.
Автори та атрибуція
- Template:ContribAgnewM
- Template:ContribAgnewH
- Libretext: Chemistry for Allied Health (Soult)
- Libretext: The Basics of GOB Chemistry (Ball et al.)