3.3: Молекули та хімічна номенклатура
- Page ID
- 22518
- Визначте молекулу.
- Назвіть прості молекули на основі їх формул.
- Визначте формулу молекули виходячи з її назви.
Існує багато речовин, які існують у вигляді двох або більше атомів, з'єднаних між собою настільки сильно, що вони поводяться як одна частинка. Ці багатоатомні комбінації називаються молекулами. Молекула - це найменша частина речовини, яка має фізичні та хімічні властивості цієї речовини. У деяких відношеннях молекула схожа на атом. Однак молекула складається з більш ніж одного атома.
| Водень (1\(\ce{H2}\)) | Кисень (\(\ce{O2}\)) | Азот (\(\ce{N2}\)) | Фтор (1\(\ce{F2}\)) |
|---|---|---|---|
| \ (\ ce {H2}\)) ">Хлор (\(\ce{Cl2}\)) | \ (\ ce {O2}\)) ">Бром (\(\ce{Br2}\)) | \ (\ ce {N2}\)) ">Йод (\(\ce{I2}\)) | \ (\ ce {F2}\)) "> |
Деякі елементи існують природним шляхом у вигляді молекул. Наприклад, водень і кисень існують у вигляді двоатомних молекул. Інші елементи також існують природним шляхом у вигляді двоатомних молекул (табл.\(\PageIndex{1}\)). Як і будь-яка молекула, ці елементи позначені молекулярною формулою, формальним переліком того, що і скільки атомів знаходиться в молекулі. (Іноді використовується тільки формула слова, і його значення виводиться з контексту.) Наприклад, молекулярна формула елементарного водню - H 2, причому H є символом водню, а індекс 2 означає, що в молекулі є два атоми цього елемента. Інші двохатомні елементи мають аналогічні формули: O 2 , N 2 і так далі. Інші елементи існують як молекули - наприклад, сірка зазвичай існує як восьмиатомна молекула, S 8, тоді як фосфор існує як молекула чотирьох атомів, P 4 (рис.\(\PageIndex{1}\)). В іншому випадку ми будемо вважати, що елементи існують як окремі атоми, а не молекули. Передбачається, що у формулі є лише один атом, якщо в правій частині символу елемента немає числового індексу.
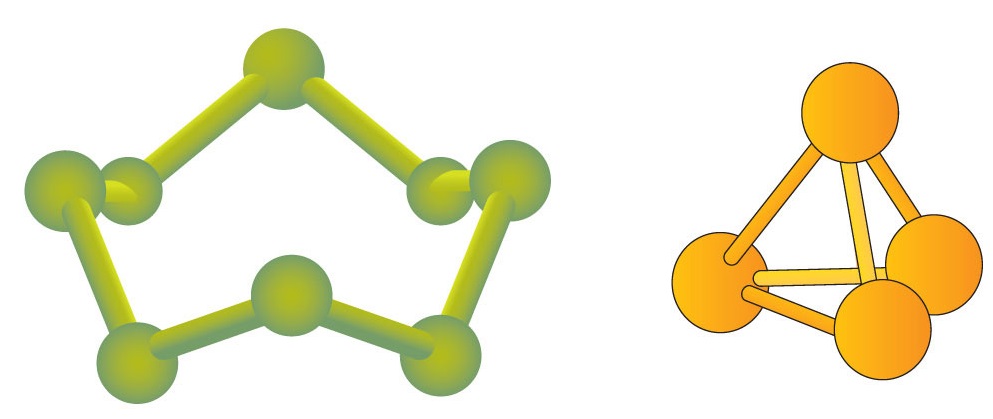
\(\PageIndex{1}\)На малюнку показано два приклади того, як ми будемо представляти молекули в цьому тексті. Атом представлений невеликою кулькою або сферою, яка, як правило, вказує, де знаходиться ядро в молекулі. Циліндрична лінія, що з'єднує кулі, являє собою зв'язок між атомами, які роблять цю колекцію атомів молекулою. Цей зв'язок називається хімічним зв'язком і є зв'язком між двома атомами в молекулі.
Багато сполук існують у вигляді молекул. Зокрема, коли неметали з'єднуються з іншими неметалами, сполуки зазвичай існують як молекули. (Сполуки між металом і неметалом різні і будуть розглянуті в розділі 3.4.) У деяких випадках існує багато різних видів молекул, які можуть утворюватися між будь-якими заданими елементами, причому всі різні молекули мають різні хімічні та фізичні властивості. Як ми їх розмежовуємо?
Відповіддю є дуже специфічна система іменування з'єднань, звана хімічною номенклатурою. Дотримуючись правил номенклатури, кожне з'єднання має свою унікальну назву, і кожне ім'я відноситься до одного і тільки одного з'єднання. Тут ми почнемо з відносно простих молекул, які мають в собі всього два елементи, так звані бінарні сполуки:
- Визначте елементи в молекулі по її формулі.
- Починайте ім'я з імені елемента першого елемента. Якщо в молекулярній формулі більше одного атома цього елемента, використовуйте числовий префікс для позначення кількості атомів, як зазначено в табл\(\PageIndex{2}\). Не використовуйте приставку mono-, якщо є тільки один атом першого елемента.
- Назвіть другий елемент за допомогою трьох частин:
- числовий префікс, що вказує кількість атомів другого елемента, плюс
- стовбур назви елемента (наприклад, коробка для кисню, хлор для хлору тощо), плюс
- суфікс -ide
- Об'єднайте два слова, залишивши між ними пробіл.
| Кількість атомів елемента | Префікс |
|---|---|
| 1 | моно- |
| 2 | ді- |
| 3 | три- |
| 4 | тетра- |
| 5 | пента- |
| 6 | гекса- |
| 7 | гепта- |
| 8 | окта- |
| 9 | нона- |
| 10 | дека- |
Давайте подивимося, як ці кроки працюють для молекули, молекулярна формула якої SO 2, яка має один атом сірки та два атоми кисню - це завершено крок 1. Відповідно до кроку 2, ми починаємо з назви першого елемента—сірки. Пам'ятайте, ми не використовуємо моно- префікс для першого елемента. Тепер для кроку 3 ми об'єднаємо числовий префікс di- (див. Таблицю\(\PageIndex{2}\)) зі стовбуровим биком- і суфіксом -ide, щоб зробити діоксид. Об'єднавши ці два слова разом, ми маємо унікальну назву цієї сполуки - діоксид сірки.
Чому вся ця біда? Існує ще одне поширене з'єднання, що складається з сірки і кисню, молекулярна формула якого - SO 3, тому сполуки потрібно розрізняти. SO 3 має три атоми кисню в ньому, тому це різна сполука з різними хімічними та фізичними властивостями. Система хімічної номенклатури покликана дати цьому з'єднанню свою унікальну назву. Його назва, якщо пройти всі етапи, - триоксид сірки. Різні сполуки мають різні назви.
У деяких випадках, коли префікс закінчується на a або o; а ім'я елемента починається з o, ми скидаємо a або o на префікс. Таким чином, ми бачимо монооксид або пентоксид, а не монооксид або пентаоксид в назвах молекул.
Назвіть кожну молекулу.
- ПФ 3
- СО
- Се 2 Бер 2
Рішення
- Молекула з одним атомом фосфору і трьома атомами фтору називається трифторидом фосфору.
- З'єднання з одним атомом вуглецю і одним атомом кисню правильно називають чадним газом, а не монооксидом вуглецю.
- Є два атоми кожного елемента, селен і бром. Згідно з правилами, власне назва тут - дибромід диселену.
Назвіть кожну молекулу.
- СФ 4
- П 2 С 5
- Відповідь на
-
тетрафторид сірки
- Відповідь б
-
дифосфор пентасульфід
Одна чудова річ про цю систему полягає в тому, що вона працює в обох напрямках. З назви з'єднання слід вміти визначати його молекулярну формулу. Просто перерахуйте символи елемента з числовим індексом, якщо є більше одного атома цього елемента, у порядку імені (ми не використовуємо індекс 1, якщо присутній лише один атом елемента; мається на увазі 1). З назви трихлорид азоту ви повинні мати можливість отримати NCl 3 як формулу для цієї молекули. З назви п'ятитоксид дифосфору ви повинні мати можливість отримати формулу P 2 O 5 (зверніть увагу на числовий префікс на першому елементі, що вказує на наявність у формулі більше одного атома фосфору).
Дайте формулу для кожної молекули.
- чотирихлористий вуглець
- діоксид кремнію
- трикремнію тетранітрид
Рішення
- Назва чотирихлористого вуглецю має на увазі один атом вуглецю і чотири атоми хлору, тому формула CcL 4.
- Назва діоксиду кремнію має на увазі один атом кремнію і два атома кисню, тому формула SiO 2.
- У нас є ім'я, яке має числові префікси на обох елементах. Tri- означає три, а тетра- означає чотири, тому формула цього з'єднання Si 3 N 4.
Дайте формулу для кожної молекули.
- дифторид дісірки
- пентабромід йоду
- Відповідь на
-
\(\ce{S2F2 }\)
- Відповідь б
-
\(\ce{IBr5}\)
Деякі прості молекули мають загальні назви, які ми використовуємо як частину формальної системи хімічної номенклатури. Наприклад, Н 2 О дається назва вода, а не дигідроксид. NH 3 називається аміаком, тоді як CH 4 називається метаном. Ми іноді побачимо інші молекули, які мають спільні назви; ми вкажемо на них, як вони відбуваються.
Ключові виноси
- Молекули - це групи атомів, які поводяться як єдина одиниця.
- Деякі елементи існують у вигляді молекул: водень, кисень, сірка тощо.
- Існують правила, які можуть виражати унікальну назву для будь-якої заданої молекули, і унікальну формулу для будь-якої заданої назви.
