5.1: Хімічні рівняння
- Page ID
- 22142
Цілі навчання
- Визначити хімічну реакцію.
- Зрозумійте закон збереження матерії
Вода (H 2 O) складається з водню і кисню. Припустимо, ми уявляємо процес, в якому ми приймаємо елементарний водень (H 2) та елементарний кисень (O 2) і дозволяємо їм реагувати, щоб зробити воду. Заява
«водень і кисень реагують, щоб зробити воду»
це один із способів уявити цей процес, який називається хімічною реакцією. \(\PageIndex{1}\)На малюнку показаний досить драматичний приклад цієї самої реакції.

Щоб спростити написання реакцій, ми використовуємо формули замість імен, коли описуємо реакцію. Ми також можемо використовувати символи для представлення інших слів у реакції. Знак плюса з'єднує вихідні речовини (і кінцеві речовини, якщо їх більше одного), а стрілка (→) являє собою хімічну зміну:
\[\ce{H_2 + O_2 \rightarrow H_2O} \label{Eq1}\]
Це твердження є одним із прикладів хімічного рівняння, скороченого способу використання символів для представлення хімічної зміни. Речовини з лівого боку стрілки називаються реагентами, а речовини з правого боку стрілки називаються продуктами. Не рідкість включати мітку фази з кожною формулою— (s) для твердої речовини, () для рідини, (g) для газу та (aq) для речовини, розчиненої у воді, також відомої як водний розчин. Якби ми включили фазові етикетки для реагентів та продуктів, при нормальних умовах навколишнього середовища реакція буде такою:
\[\ce{H2(g) + O2(g) \rightarrow H2O (ℓ)} \label{Eq2}\]
Це рівняння все ще не є повним, оскільки воно не задовольняє закону збереження речовини. Підрахуйте кількість атомів кожного елемента з кожного боку стрілки. На стороні реагенту є два атоми Н і два атоми O; на стороні продукту є два атоми Н і лише один атом кисню. Рівняння не збалансоване, оскільки кількість атомів кисню з кожного боку не однакове (рис.\(\PageIndex{2}\)).
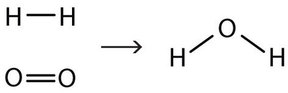
Щоб це хімічне рівняння відповідало закону збереження речовини, ми повинні переглянути кількість реагентів та продуктів, необхідних, щоб отримати однакову кількість атомів даного елемента з кожного боку. Оскільки кожна речовина має характерну хімічну формулу, ми не можемо змінювати хімічні формули окремих речовин. Наприклад, ми не можемо змінити формулу елементарного кисню на O. Однак можна припустити, що може бути задіяна різна кількість молекул реагентів або молекул продукту. Наприклад, можливо, утворюються дві молекули води, а не лише одна:
\[\ce{H2(g) + O2 (g) \rightarrow 2H2O (ℓ)} \label{Eq3}\]
2, що передує формулі для води, називається коефіцієнтом. Він має на увазі, що утворюються дві молекули води. Зараз на кожній стороні рівняння є два атоми кисню.
Цей момент настільки важливий, що ми повинні його повторити. Ви не можете змінити формулу хімічної речовини, щоб збалансувати хімічну реакцію! Необхідно використовувати правильну хімічну формулу речовини.
На жаль, вставивши коефіцієнт 2 перед формулою для води, ми також змінили кількість атомів водню на стороні продукту. В результаті у нас більше немає однакової кількості атомів водню з кожного боку. Однак це можна легко виправити, поставивши коефіцієнт 2 перед двоатомним водневим реагентом:
\[\ce{2H2(g) + O2(g) \rightarrow 2H2O (ℓ)} \label{Eq4}\]
Тепер у нас є чотири атоми водню і два атоми кисню з кожного боку рівняння. Закон збереження речовини задовольняється тому, що тепер ми маємо однакову кількість атомів кожного елемента в реагентах і в продуктах. Ми говоримо, що реакція тепер збалансована (рис.\(\PageIndex{3}\)). Примітка: Двохатомний кисень має коефіцієнт 1, який зазвичай не записується, але приймається в збалансованих хімічних рівняннях.
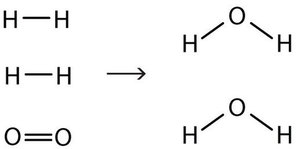
Правильні хімічні рівняння повинні бути збалансованими. Написання збалансованих реакцій - це хімічний спосіб визнання закону збереження речовини.
Приклад\(\PageIndex{1}\)
Чи збалансовано кожне хімічне рівняння?
- 2На (и) + О 2 (г) → 2На 2 О (и)
- СН 4 (г) + 2О 2 (г) → СО 2 (г) + 2Н 2 О ()
- Гано (3 ккал) + 2ККл (ак) → Гакл (и) + КНО (3 кв)
Рішення
- Підрахувавши, ми знаходимо два атоми натрію і два атоми кисню в реагентах і чотири атоми натрію і два атоми кисню в продуктах. Це рівняння не збалансоване.
- Реагенти мають один атом вуглецю, чотири атоми водню та чотири атоми кисню. Продукти мають один атом вуглецю, чотири атоми водню і чотири атоми кисню. Це рівняння збалансоване.
- Реагенти мають один атом срібла, один атом азоту, три атоми кисню, два атоми калію та два атоми хлору. Продукти мають один атом срібла, один атом хлору, один атом калію, один атом азоту та три атоми кисню. Оскільки існує різна кількість атомів хлору та калію, це рівняння не збалансоване.
Вправа\(\PageIndex{1}\)
Чи збалансовано кожне хімічне рівняння?
- \(2Hg_{(ℓ)} + O_{2(g)} \rightarrow Hg_2O_{2(s)}\)
- \(C_2H_{4(g)} + 2O_{2(g)} \rightarrow 2CO_{2(g)} + 2H_2O_{(ℓ)}\)
- \(Mg(NO_3)_{2(s)} + 2Li_{(s)} \rightarrow Mg_{(s)} + 2LiNO_{3(s)}\).
- Відповідь:
-
врівноважений
- Відповідь б:
-
O не врівноважений; 4 атоми кисню зліва не балансують з 6 атомами кисню праворуч
- Відповідь c:
-
врівноважений