6.1: Що таке кислота і основа?
- Page ID
- 25516
Загальні властивості кислот і підстав
Ми зазвичай стикаємося з кислотами і основами в наших продуктах харчування - деякі продукти кислі, а інші - основні (лужні), як показано на рис. 6.1.1.
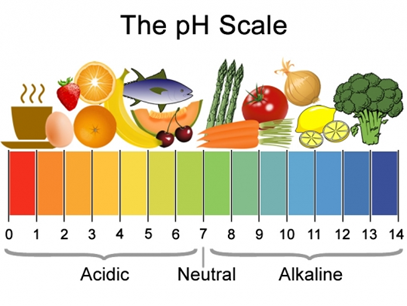
Загальні властивості кислот і підстав наступні.
- Кислоти на смак кислий, наприклад, цитрусові фрукти джерело смаку через цитрусової кислоти і аскорбінової кислоти, тобто вітаміну С, в них. Основні (лужні) речовини, навпаки, гіркий смак.
- Основні (лужні) речовини відчувають себе соковитими, в той час як кислі речовини можуть жалити.
- Кислоти стають синім лакмусовим папером для читання, але не змінюють колір червоного лакмусового паперу. Бази стають червоними лакмусовими паперами синього кольору, але не змінюють колір блакитного лакмусового паперу, як показано на рис. 6.1.2.
- Індикатор фенолфталеїну стає безбарвним в кислоті і стає рожевим в базовому розчині, як показано на рис. 6.1.3.
- Кислоти і основи нейтралізують один одного. У шлунку міститься соляна кислота, яка допомагає травленню. Надлишок соляної кислоти може спричинити кислотні опіки - антациди, такі як молоко магнезії, є основами, які допомагають нейтралізувати надлишок кислоти в шлунку.


Визначення Арренія кислот і підстав
Найбільш раннє визначення кислот і підстав - це визначення Арреніуса, яке стверджує, що:
- Кислота - це речовина, яка при розчиненні у воді утворює іони водню Н +, і
- Основою є речовина, що утворює гідроксид-іони ОН - при розчиненні у воді.
Наприклад, соляна кислота - це кислота, оскільки вона утворює Н +, коли розчиняється у воді.
\[\mathrm{HCl}(\mathrm{g}) \stackrel{\text { Water }}{\longrightarrow} \mathrm{H}^{+}(\mathrm{aq})+\mathrm{Cl}^{-}(\mathrm{aq})\nonumber\]
Аналогічно, NaOH є основою, оскільки він утворює OH - коли розчиняється у воді.
\[\mathrm{NaOH}(\mathrm{s}) \stackrel{\text { Water }}{\longrightarrow} \mathrm{Na}^{+}(\mathrm{aq})+\mathrm{OH}^{-}(\mathrm{aq})\nonumber\]
Зауважимо, що іон водню Н + не існує в реальності. Він зв'язується з молекулами води і існує у вигляді іона гідронію H 3 O + (aq).
\[\mathrm{H}^{+}(\mathrm{aq})+\mathrm{H}_{2} \mathrm{O} \rightarrow \mathrm{H}_{3} \mathrm{O}^{+}(\mathrm{aq})\nonumber\]
Однак Н + (aq) часто пишуть на місці (H 3 O + (aq).
Найменування арренієвих кислот і основ
У таблиці 1 наведені назви і формули деяких поширених кислот і їх аніонів.
- Назви закінчуються словом «кислота».
- Якщо аніон не є оксианіоном, то додайте приставку hydro- до назви аніона і змініть останній склад назви аніона на —ic. Наприклад, Cl - це хлорид-іон, а HCl - соляна кислота.
- Якщо аніон є оксианіоном з останнім складом —їли, змініть останній склад на —ic. Не використовуйте приставку гідро-, а додайте останнє слово «кислота». Якщо в назві оксианіона присутній префікс пер-, збережіть приставку в назві кислоти. Наприклад, NO 3 - це нітрат, а HNO 3 - азотна кислота. Інший приклад, ClO 4 - це перхлорат, а HClO 3 - хлорна кислота.
- Якщо аніон є оксианіоном з останнім складом —ite, змініть останній склад на —ous. Не використовуйте приставку гідро-, а додайте останнє слово «кислота». Якщо в назві оксианіона є приставка гіпо-, збережіть приставку в назві кислоти. Наприклад, NO 2 - це нітрит, а HNO 2 - азотна кислота. Інший приклад, ClO - це гіпохлорит, а HClO - хлорноватиста кислота.
|
Кислотна формула |
назва кислоти |
Аніон |
Аніон ім'я |
|---|---|---|---|
|
HCl |
Соляна кислота |
Кл - |
Хлорид |
|
HBr |
Бромна кислота |
Бр - |
Бромід |
|
ПРИВІТ |
Кислота воднева |
Я - |
йодид |
|
HCN |
Синильна кислота |
CN - |
Ціанід |
|
HNO 3 |
Азотна кислота |
№ 3 - |
Нітрат |
|
HNO 2 |
Азотна кислота |
№ 2 - |
Нітрити |
|
Н 2 ТАК 4 |
Сірчана кислота |
ТАК 4 2 - |
Сульфат |
|
Н 2 ТАК 3 |
Сірчиста кислота |
ТАК 3 2 - |
Сульфіт |
|
Н 2 СО 3 |
Вугільна кислота |
СО 3 - |
Карбонат |
|
СН 3 СООН |
оцтова кислота |
СН 3 СОО - |
ацетат |
|
Н 3 ПОЗ 4 |
Фосфорна кислота |
ПО 4 3 - |
Фосфат |
|
Н 3 ПОЗ 3 |
фосфорна кислота |
ПО 3 3 - |
Фосфіт |
|
ХЛО 4 |
хлорну кислоту |
КЛО 4 - |
Перхлорат |
|
ХЛО 3 |
Хлорна кислота |
КЛО 3 - |
Хлорат |
|
ХЛО 2 |
хлорнуватиста кислота |
КЛО 2 - |
Хлорит |
|
ХКЛО |
Гіпокалорозна кислота |
КЛО - |
Гіпохлорит |
У таблиці 2 наведено назви та формули деяких поширених основ Арреніуса.
Підстави Арренія - це іонні сполуки металу і гідроксид-іона, і їх назва починається з назви металевого елемента, за яким слідує назва аніона, тобто гідроксиду. Наприклад, NaOH - це гідроксид натрію.
|
Формула |
Ім'я |
|---|---|
|
ЛеО |
гідроксид літію |
|
NaOH |
Гідроксид натрію |
|
КОНХ |
Гідроксид калію |
|
Са (ОН) 2 |
Гідроксид кальцію |
|
Ср (ОН) 2 |
гідроксид стронцію |
|
Ба (ОН) 2 |
Гідроксид барію |
