1.6: Рівняння та графіки
- Page ID
- 25461
Рівності, де обидві сторони мають єдиний термін, тобто мономіальний, призводять до коефіцієнтів перетворення. Якщо одна або обидві сторони рівності мають більше одного члена, тобто полінома, це призводить до формули, яка виконує ту саму роботу, тобто перетворювати одиниці. Рівняння перетворення температури та рівняння ідеального газу та процедура маніпулювання цими рівняннями описані нижче як приклади того, як маніпулювати питаннями, необхідними для проведення розрахунків.
Рівняння перетворення температури
Існує три температурні шкали загального користування: Цельсія (o C), Кельвін (K) та Фаренгейт (o F), проілюстровані на рис. 1.6.1.
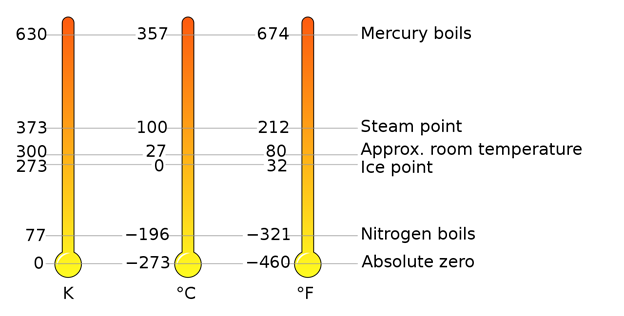
Цельсія (o C)
Шкала Цельсія має O O C при температурі замерзання води і 100 o C при температурі кипіння води. Цельсія є базовою одиницею температури в метричній системі.
шкала Кельвіна
Кельвін є базовою одиницею температури в СІ. Температура замерзання води становить 273,15 К, а температура кипіння води 373,15 К. Для більшості практичних цілей температура замерзання води повідомляється як 273 К і температура кипіння 373 К, тобто з точністю до трьох значущих цифр. Одиниці шкали Цельсія мають однаковий розмір, але зміщені вгору на 273 порівняно зі шкалою Кельвіна. Отже, відносини між Кельвіном і Цельсієм такі:
\ begin {рівняння}
T_ {K} = T_ {C} +273,\ nonumber
\ end {рівняння}
де T K - температура в Кельвіні, а T C - температура в градусах Цельсія. Це рівняння перетворює температуру в Кельвіні в температуру за Цельсієм.
A 0 K, також званий абсолютним нулем, - це температура речовини, при якій жодна енергія не може бути видалена як тепло з речовини. Від'ємної температури за шкалою Кельвіна немає.
Фаренгейт (o F)
Фаренгейт є базовою одиницею англійської системи, з 32 o F в точці замерзання води і 212 o F при температурі кипіння води. Фаренгейт в\(\frac{5}{9}\) рази коротший і зміщений вгору на 32, ніж за Цельсієм. Отже, відносини між ними такі:
\ begin {рівняння}
T_ {F} =\ frac {9} {5}\ раз T_ {C} +32,\ nonumber
\ end {рівняння}
де T F - температура в градусах за Фаренгейтом, а T C - температура в градусах Цельсія. Це рівняння перетворює температуру за Цельсієм в температуру за Фаренгейтом.
Маніпулювання рівняннями перетворення температури
Рівняння для перетворення Цельсія в Фаренгейта таке:
\ begin {рівняння}
T_ {F} =\ frac {9} {5}\ раз T_ {C} +32,\ nonumber
\ end {рівняння}
Додавання або віднімання одного і того ж числа з двох сторін рівняння не змінює рівності. Віднімання 32 з обох сторін вищевказаного рівняння призводить до:
\ begin {рівняння}
T_ {F} -32=\ frac {9} {5}\ раз T_ {C}\ скасувати {+32}\ скасувати {-32},\ nonumber
\ end {рівняння}
\ begin {рівняння}
T_ {F} -32=\ frac {9} {5}\ раз T_ {C}. \ nonumber
\ end {рівняння}
Множення або ділення на одне і те ж число по обидва боки рівняння не змінює рівності. Пам'ятайте, що множення або ділення повинні застосовуватися до кожного члена по обидва боки рівності. Закріпіть сторону з більш ніж одним членом у маленькі дужки, а потім виконайте операцію множення ділення так, щоб вона застосовувалася до кожного члена в дужці. Множення обох сторін вищевказаного рівняння\(\frac{5}{9}\) призводить до:
\ begin {рівняння}
\ гідророзриву {5} {9}\ раз\ ліворуч (T_ {F} -32\ праворуч) =\ скасувати {\ frac {5} {9}}\ раз\ скасувати {\ frac {9} {5}}\ раз T_ {C}\ nonumber
\ end {рівняння}
\ begin {рівняння}
\ frac {5} {9}\ раз\ ліворуч (T_ {F} -32\ праворуч) =T_ {C}\ nonumber
\ end {рівняння}
Зміна сторін рівняння не змінює рівності. Поміняючи місцями сторони у наведеному вище рівнянні, щоб привести T C вліво:
\ begin {рівняння}
T_ {C} =\ frac {5} {9}\ раз\ ліворуч (T_ {F} -32\ праворуч)\ nonumber
\ end {рівняння}
Це рівняння для перетворення Фаренгейта в Цельсія.
Процедура перестановки рівняння, описаного вище, застосовується до всіх алгебраїчних рівнянь. Наприклад, почніть з відносин, які перетворюють Цельсія в Кельвіна:
\ begin {рівняння}
T_ {K} = T_ {C} +273,\ nonumber
\ end {рівняння}
відніміть 273 з обох сторін:
\ begin {рівняння}
T_ {K} -273= T_ {C}\ скасувати {+273}\ скасувати {-273},\ nonumber
\ end {рівняння}
\ begin {рівняння}
T_ {K} -273= T_ {C},\ nonumber
\ end {рівняння}
і, нарешті, поміняти місцями ліву і праву сторону, щоб привести T C вліво:
\ begin {рівняння}
T_ {C} =T_ {K} -273. \ nonumber
\ end {рівняння}
Це рівняння для перетворення Кельвіна в Цельсія.
Рівняння ідеального газу
Ідеальне рівняння газу пов'язує більше двох змінних:
\[PV=nRT,\nonumber\]
де P - тиск, V - об'єм, n - кількість газу в молі, T - температура (в К), а R - константа пропорційності, яка називається постійною ідеальної газу. Поділ обох сторін рівняння з V призводить до:
\[P\times\frac{V}{V}=\frac{nRT}{V},\nonumber\]
\[P=\frac{n R T}{V}.\nonumber\]
Він дозволяє обчислити тиск проби газу, якщо відомі кількість в молі, температура в кельвіні, обсяг проби газу разом із значенням постійної R в послідовних одиницях. Аналогічно перестановка рівняння призводить до формул для обчислення, V, T або n проби газу:
\ begin {рівняння} V
=\ frac {n R T} {P},\ квад T=\ гідророзриву {P V} {n R},\ квад\ текст {і}\ квад n=\ frac {P V} {R T}\ nonumber
\ end {рівняння}
Графіки
Графік являє собою наочне уявлення про зв'язок між двома змінними. На рис. 1.6.2 показаний графік, який представляє залежність між об'ємом і тиском заданої кількості газу при постійній температурі, відомий як закон Бойла.
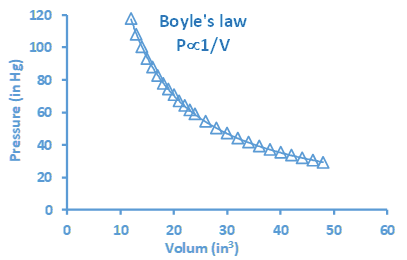
Типовими складовими графіка є наступні.
- Назва, яка розповідає про те, про що йде графік, наприклад, «Закон Бойла:» на графіку рис. 1.6.2.
- Осі: вісь x - це горизонтальна лінія, а вісь y - вертикальна лінія. Осі зазвичай мають рівномірно розподілену шкалу, починаючи з нуля. Вісь x представляє незалежну змінну, а вісь y - залежну змінну. Наприклад, обсяг незалежний, а тиск - залежна змінна на рис.1.6.2.
- Мітки осей, які вказують назву змінної та одиниці виміру. Наприклад, обсяг (в 3) і тиск (в Hg), де в 3 і в Hg - одиниці змінних.
- Символи, що представляють експериментальні точки. Наприклад, Δ символи на рис. 1.6.2, при перетині вертикальної лінії, що починається з експериментальної величини незалежної змінної на осі x і горизонтальної лінії, що починається від відповідного значення залежної змінної на осі y.
- Крива з'єднує експериментальні точки і показує тенденцію в стосунках. Наприклад, затвердіння на рис. 1.6.2 говорить про те, що тиск зменшується в міру збільшення обсягу.
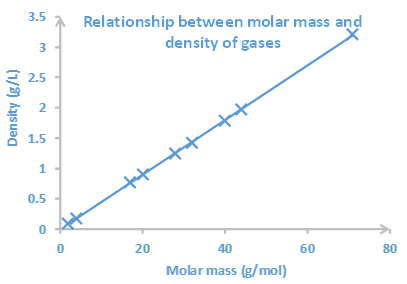
інтерпретація графа
Інтерпретація - це читання тенденції або взаємозв'язку між побудованими змінними. Наприклад, на рис. 1.6.2 видно, що тиск зменшується в міру збільшення обсягу газу. Крива також дозволяє зчитувати значення однієї змінної зі значення іншої. Наприклад, якщо об'єм дорівнює 30 в 3, тиск становитиме ~ 50 в рт. Ст. Читати: намалюйте вертикальну лінію від заданого значення на осі х і горизонтальну лінію від точки, де вертикальна лінія перетинає криву. Потім прочитайте значення, де горизонтальна лінія відповідає осі y. Процес змінюється, коли задане значення є залежною змінною від осі y, а бажаним є відповідне значення незалежної змінної на осі x. Наприклад, якщо тиск дорівнює 40 в рт.ст., обсяг становить близько 35 в 3. Рис. 1.6.3 - ще один приклад графіка, який показує залежність між молярною масою і щільністю газів при постійній температурі. Лікування на цьому графіку говорить про те, що щільність газів збільшується у міру збільшення молярної маси.