23.4: Молекулярно-селективні електродні системи
- Page ID
- 27203
Електроди в главі 23.4 селективні по відношенню до іонів. У цьому розділі ми розглянемо, як ми можемо включити іоноселективний електрод в електрод, який реагує на нейтральні види, такі як летючі аналіти, такі як CO 2 і NH 3, і біохімічно важливі сполуки, такі як амінокислоти та сечовина.
Газочутливі мембранні електроди
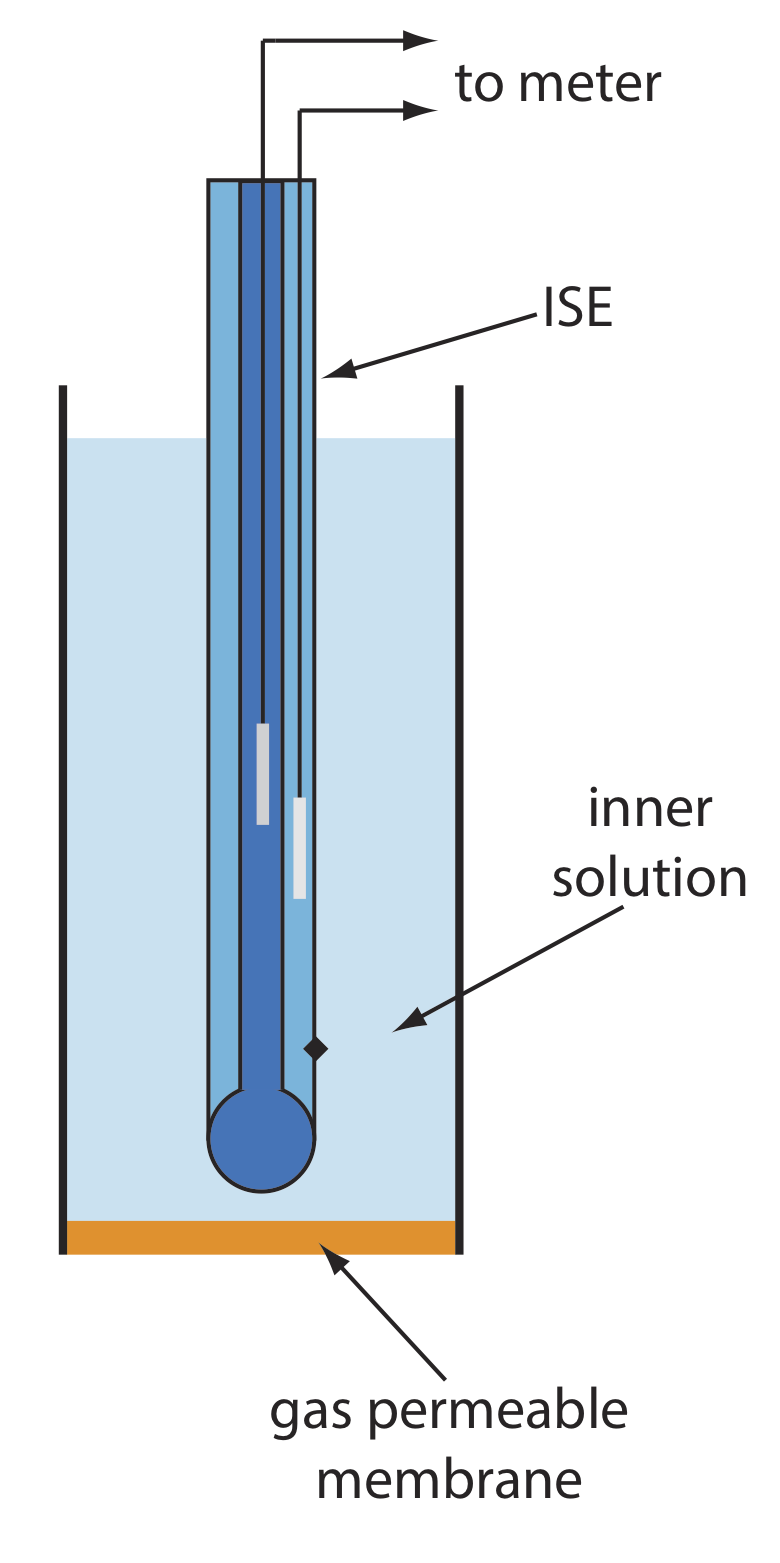
Ряд мембранних електродів реагує на концентрацію розчиненого газу. Основна конструкція газочутливого електрода, як показано на малюнку\(\PageIndex{1}\), складається з тонкої мембрани, яка відокремлює зразок від внутрішнього розчину, який містить іоноселективний електрод. Мембрана проникна для газоподібного аналіту, але непроникна для нелетких компонентів матриці зразка. Газоподібний аналіт проходить через мембрану, де реагує з внутрішнім розчином, утворюючи вид, концентрація якого контролюється іоноселективним електродом. Наприклад, в електроді СО 2 CO 2 дифузує по мембрані, де він реагує у внутрішньому розчині з утворенням H 3 O +.
\[\mathrm{CO}_{2}(a q)+2 \mathrm{H}_{2} \mathrm{O}(l)\rightleftharpoons\text{ HCO}_{3}^{-}(a q)+\text{ H}_{3} \mathrm{O}^{+}(a q) \label{gas1} \]
Зміна активності Н 3 О + у внутрішньому розчині контролюють за допомогою pH-електрода, для чого потенціал клітини, з глави 23.3, дорівнює
\[E_\text{cell} = K + 0.09516 \log a_{\ce{H+}} \label{gas2} \]
Щоб знайти зв'язок між активністю H 3 O + у внутрішньому розчині та активністю СО 2 у внутрішньому розчині, ми переставили вираз константи рівноваги для реакції\ ref {gas1}; таким чином
\[a_{\mathrm{H}_{3} \mathrm{O}^{+}}=K_{\mathrm{a}} \times \frac{a_{\mathrm{CO}_{2}}}{a_{\mathrm{HCO}_{3}^{-}}} \label{gas3} \]
де K a - постійна рівноваги. Якщо активність\(\text{HCO}_3^-\) у внутрішньому розчині досить велика, то на його активність не впливає невелика кількість СО 2, що проходить через мембрану. Підставляючи рівняння\ ref {gas3} в рівняння\ ref {gas2} дає
\[E_{\mathrm{cell}}=K^{\prime}+0.05916 \log a_{\mathrm{co}_{2}} \label{gas4} \]
де K′ - константа, яка включає постійну для pH-електрода, постійну рівноваги для реакції\ ref {gas1} і активність\(\text{HCO}_3^-\) у внутрішньому розчині.
У таблиці\(\PageIndex{1}\) наведені властивості декількох газочутливих електродів. Склад внутрішнього розчину з використанням змінюється, і внутрішній розчин, і мембрану необхідно періодично замінювати. Газочутливі електроди зберігаються в розчині, подібному до внутрішнього розчину, щоб мінімізувати їх вплив атмосферних газів.
Біокаталітичні мембранні електроди
Підхід до розробки газочутливих електродів може бути модифікований для створення потенціометричних електродів, які реагують на біохімічно важливий вид. Найпоширенішим класом потенціометричних біосенсорів є ферментні електроди, в яких ми затримуємо або знерухомлюємо фермент на поверхні потенціометричного електрода. Реакція аналіта з ферментом виробляє продукт, концентрація якого контролюється потенціометричним електродом. Потенціометричні біосенсори також були розроблені навколо інших біологічно активних видів, включаючи антитіла, бактеріальні частинки, тканини та рецептори гормонів.
Одним із прикладів ферментного електрода є електрод сечовини, в основі якого лежить каталітичний гідроліз сечовини уреазою.
\[\mathrm{CO}\left(\mathrm{NH}_{2}\right)_{2}(a q)+2 \mathrm{H}_{2} \mathrm{O}(l)\rightleftharpoons 2 \mathrm{NH}_{4}^{+}(a q)+\text{ CO}_{3}^{-}(a q) \label{bio1} \]
\(\PageIndex{2}\)На малюнку показана одна версія електрода сечовини, яка модифікує газочутливий електрод NH 3, додаючи діалізну мембрану, яка затримує pH 7,0 буферний розчин уреази між діалізною мембраною та газопроникною мембраною [(a) Papastathopoulos, D.S.; Rechnitz, G A. Анальний. Чим. Акт 1975, 79, 17—26; (б) Ріхель, Т. Едук. 1984, 61, 640—642]. Електрод NH 3, як показано в таблиці\(\PageIndex{1}\), використовує газопроникну мембрану і скляний pH-електрод. NH 3 розсіюється по мембрані, де він змінює рН внутрішнього розчину.
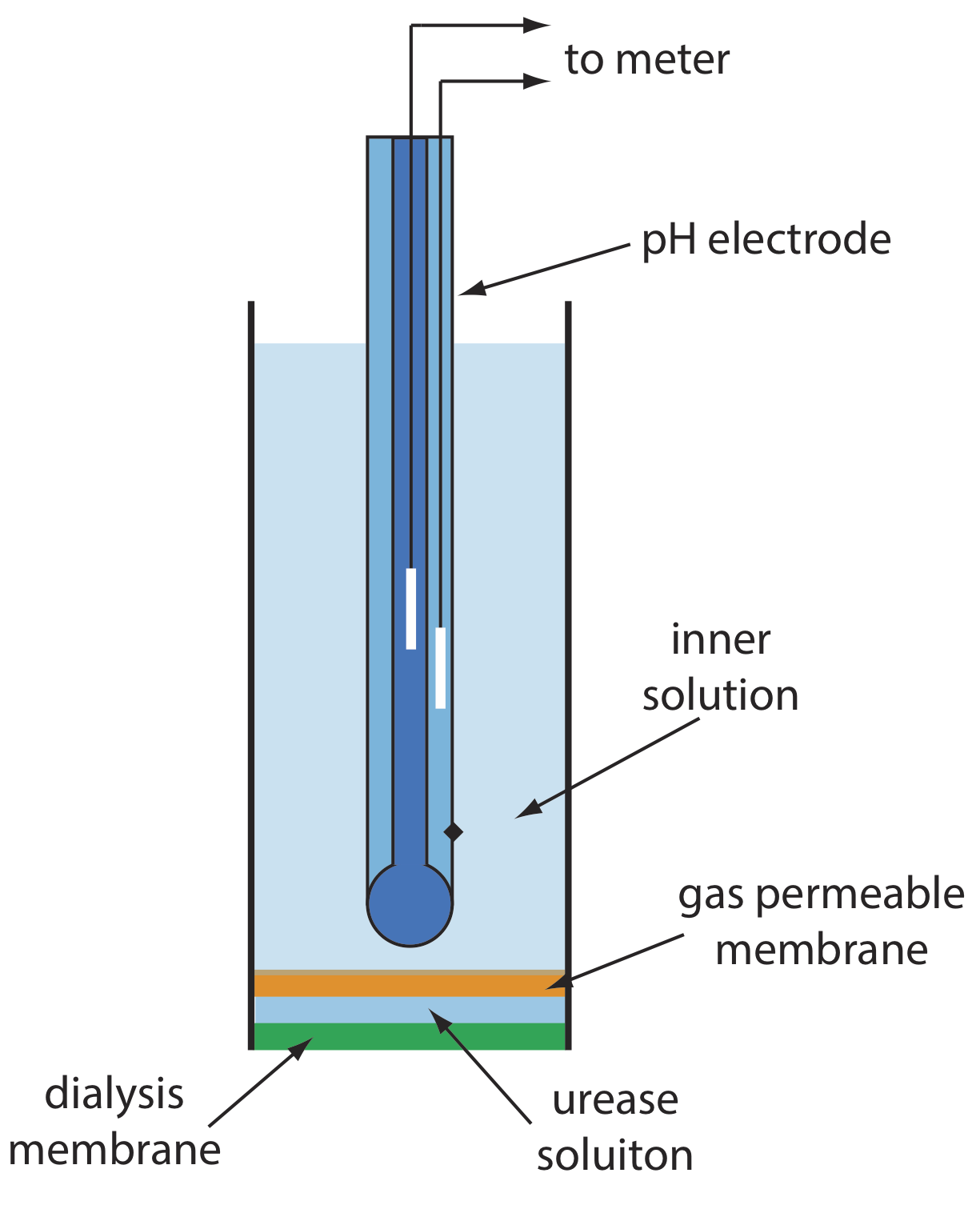
При зануренні в зразок сечовина дифузується через діалізну мембрану, де вона реагує з ферментом уреазою з утворенням іона амонію\(\text{NH}_4^+\), який знаходиться в рівновазі з NH 3.
\[\mathrm{NH}_{4}^{+}(a q)+\mathrm{H}_{2} \mathrm{O}(l ) \rightleftharpoons \text{ H}_{3} \mathrm{O}^{+}(a q)+\text{ NH}_{3}(a q) \label{bio2} \]
NH 3, в свою чергу, дифундує через газопроникну мембрану, де електрод рН вимірює результуючу зміну рН. Реакція електрода на концентрацію сечовини є
\[E_{\text {cell }}=K-0.05916 \log a_{\text {urea }} \label{bio3} \]
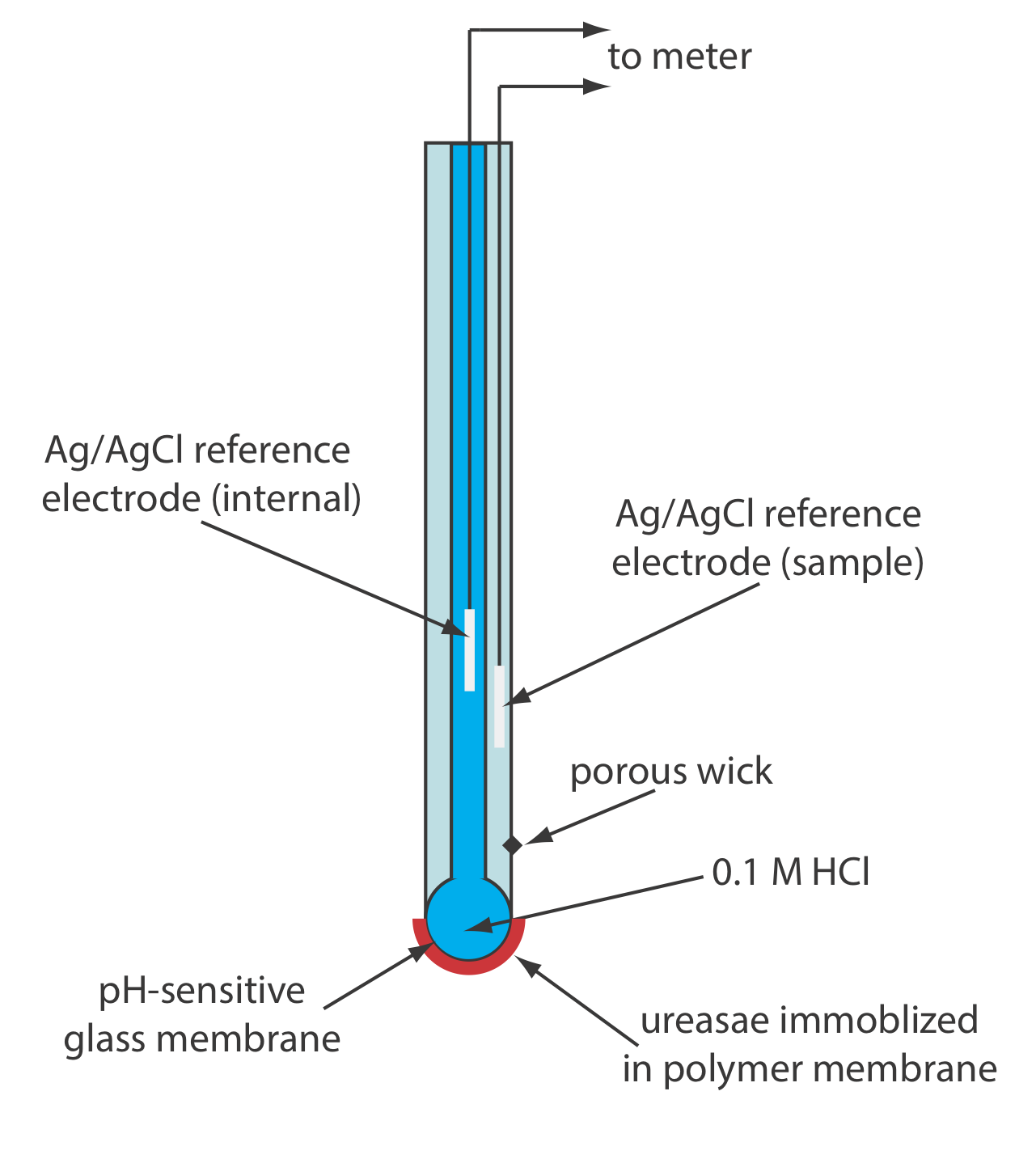
Інший варіант електрода сечовини (рис.\(\PageIndex{3}\)) іммобілізує фермент уреазу в полімерній мембрані, утвореної безпосередньо на кінчику скляного pH-електрода [Tor, R.; Freeman, A. Хім. 1986, 58, 1042—1046]. У цьому випадку реакція електрода дорівнює
\[\mathrm{pH}=K a_{\mathrm{urea}} \label{bio4} \]
Мало потенціометричних біосенсорів доступні у продажу. Однак\(\PageIndex{3}\), як показано на малюнку\(\PageIndex{2}\) та малюнку, можна перетворити іоноселективний електрод або газочутливий електрод в біосенсор. Кілька репрезентативних прикладів описано в таблиці\(\PageIndex{2}\), а додаткові приклади можна знайти в додаткових ресурсах цього розділу.
| аналіт | біологічно активна фаза | речовина визначається |
|---|---|---|
| \(5^{\prime}\)-ПІДСИЛЮВАЧ | AMP-деаміназа (Е) | NH 3 |
| L-аргінін | аргінін і уреаза (Е) | NH 3 |
| аспарагін | аспарагиназа (Е) | \(\text{NH}_4^+\) |
| L-цистеїн | Протей органічний (B) | Н 2 С |
| L-глутамат | жовтий сквош (Т) | СО 2 |
| L-глютамин | Сарцина флава (B) | NH 3 |
| оксалат | оксалатна декарбоксилаза (Е) | СО 2 |
| пеніцилін | пенікліназа (Е) | Н 3 О + |
| L-фенілаланін | L-амінокислотна оксидаза/пероксидаза хрону (Е) | Я — |
| цукри | бактерії з зубного нальоту (B) | Н 3 О + |
| сечовина | уреаза (Е) | NH 3 або Н 3 О + |
|
Джерело: Підписано від Cammann, K. робота з іонно-селективними електродами, Springer-Verlag: Берлін, 1977 і Lunte, C. E.; Heineman, W.R. «Електрохімічні методи в біоаналізі», в Steckham, E. Теми сучасної хімії, Том 143, Спрінгер-Верлаг: Берлін, 1988, с.8. Скорочення біологічно активної фази: Е = фермент; B = бактеріальна частинка; T = тканина. |
||
