20.1: Спектри молекулярних мас
- Page ID
- 27100
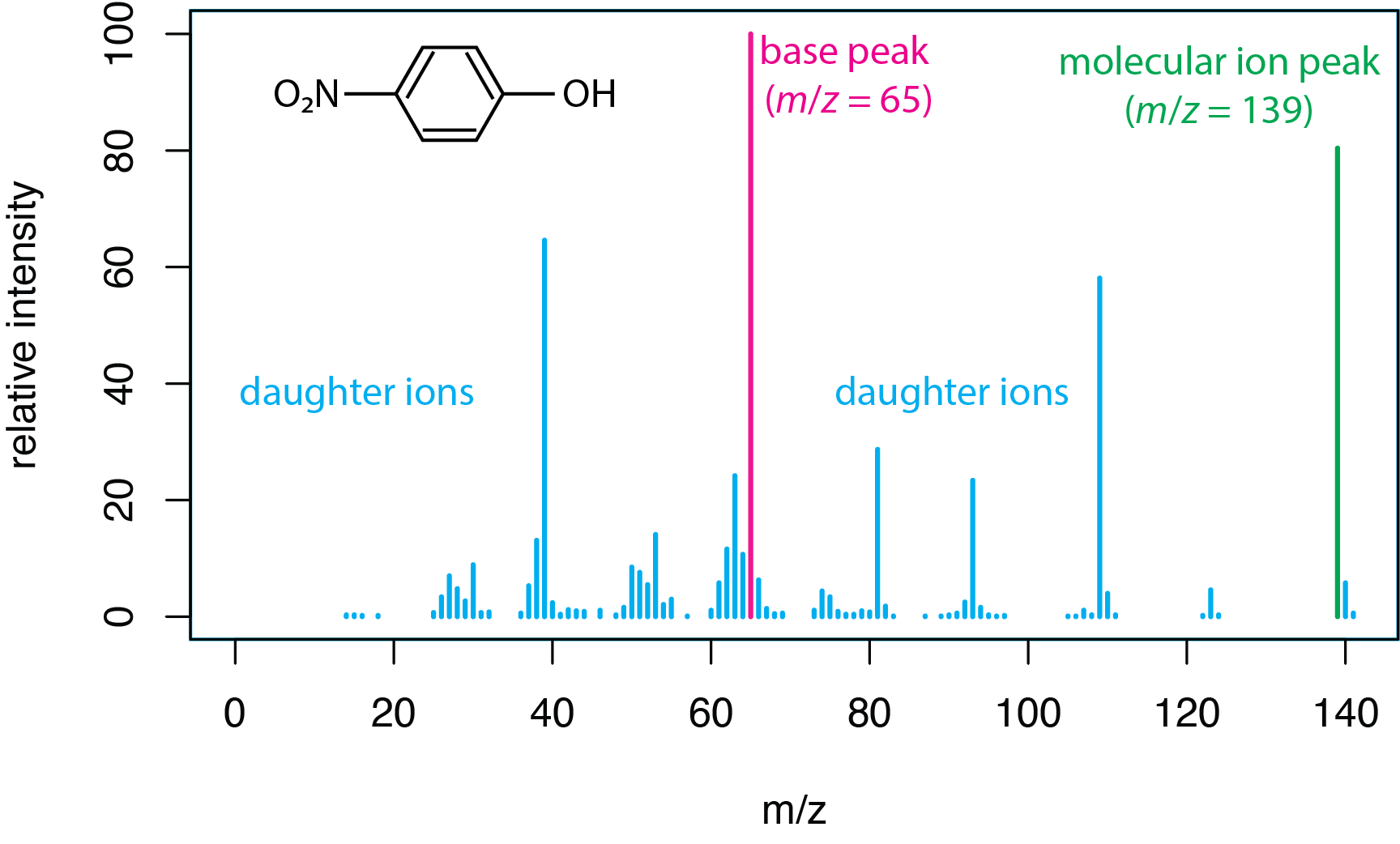
\(\PageIndex{1}\)На малюнку показаний масовий спектр для р -нітрофенолу, C 6 H 5 NO 3, який має номінальну (цілу) масу 139 дальтон. Якщо направити пучок енергетичних електронів через зразок газової фази р -нітрофенолу, він втрачає електрон, який ми запишемо як реакцію
\[\ce{C6H5NO3} + e^{-} \rightarrow \ce{C6H5NO3^{+•}} + 2e^{-} \label{pnp1} \]
де продукт є радикальним катіоном, який має заряд\(+1\) і який зберігає номінальну масу 139 дальтон. Ми називаємо це молекулярним іоном, виділеним тут зеленим кольором, і він має відношення маси до заряду (м/z) 139.
Деякі термінології в цьому розділі були висвітлені раніше в главі 11 про атомну мас-спектрометрію. Дивіться перший розділ цієї глави для обговорення одиниць атомної маси (amu) та дальтонів (Da) та співвідношення маси до заряду.
Якщо реакція\ ref {pnp1} - це все, що відбувається, коли р -нітрофенол взаємодіє з енергійним електроном, то вона не надасть багато корисної інформації. Радикальний катіон\(\ce{C6H5NO3^{+•}}\), однак, зберігає достатню надлишкову енергію від початкового зіткнення електрон-молекули, що вона знаходиться в збудженому стані. Повертаючись до свого основного стану, молекулярний іон зазнає ряд фрагментацій, які призводять до утворення іонів - званих дочірніми іонами - з різним співвідношенням маси до заряду. Ділянка, яка показує відносну інтенсивність цих іонів як функцію їх співвідношення маси до заряду, називається масовим спектром. Найбільш поширений фрагмент у спектрі, показаний тут червоним кольором і який називається базовим піком, присвоюється відносна інтенсивність 100; інтенсивність всіх інших іонів повідомляється відносно базового перка.
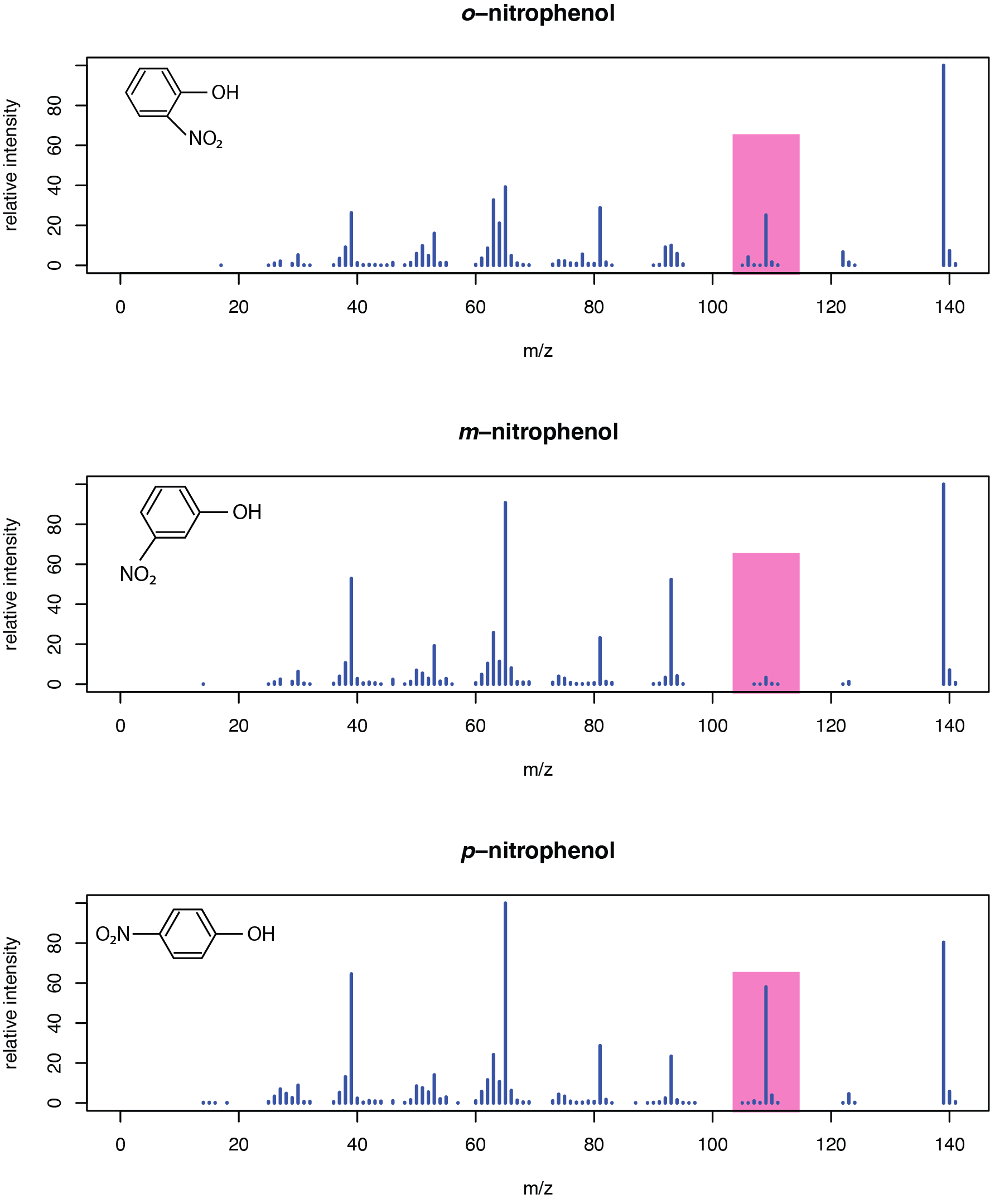
Шаблони фрагментації молекули дають багату інформацію про її структуру. На малюнку\(\PageIndex{2}\) порівнюються масові спектри для o -нітрофенолу, m -нітрофенолу і р -нітрофенолу. Всі три молекули мають кластери фрагментних іонів при однакових співвідношеннях маси до заряду, але відносна кількість іонів у цих кластерах досить сильно змінюється від молекули до молекули. Наприклад, рожевий прямокутник в кожному спектрі виділяє піки з співвідношенням маси до заряду від приблизно 104 м/z до 115 м/z. Всі три молекули мають властивість виробляти іони фрагментів при цих співвідношеннях маси до заряду; відносна кількість іонів фрагмента, однак, істотно варіюється між трьома молекулами з o -нітрофенолом і р -нітрофенолом, що мають великий пік на рівні 109 м/ z, але м -нітрофенол показує не більше сліду піку при 109 м/з. Ми повернемося до використання мас-спектрометрії для визначення структурної інформації далі в цьому розділі.