2.3: Екстрахромосомні елементи, плазміди, селекційні маркери
- Page ID
- 7556
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \) \( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)\(\newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\) \( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\) \( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\) \( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\) \( \newcommand{\Span}{\mathrm{span}}\) \(\newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\) \( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\) \( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\) \( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\) \( \newcommand{\Span}{\mathrm{span}}\)
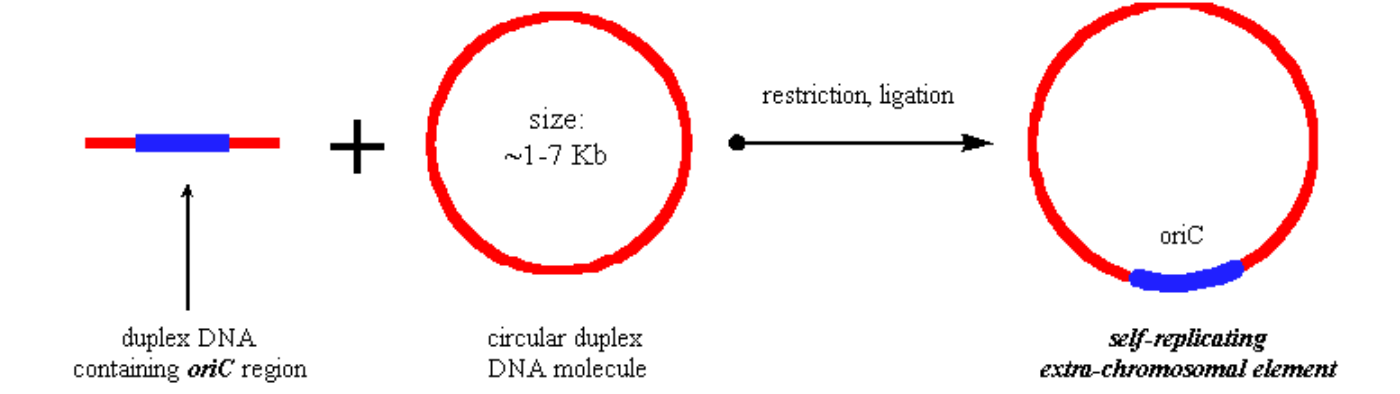
- Включення походження реплікації (тобто E. coli orIC області) у кругову молекулу ДНК є механізмом мати екстрахромосомний елемент у прокаріотичній клітині.
.png)
Малюнок 2.3.1: OriC Екстрахромосомний елемент
- Такий екстрахромосомний елемент називається плазмідою, або вектором
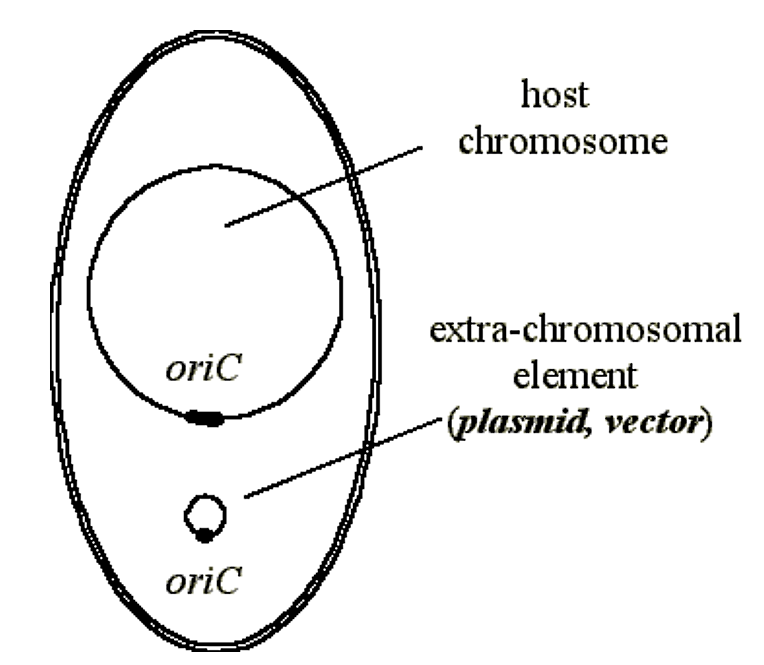
- Плазміда використовує механізми клітини-господаря (тобто полімерази, хелікази, dNtP тощо) для прямої реплікації.
.png)
Малюнок 2.3.2: Вектор/плазміда
- Однак, оскільки додаткова робота по реплікації екстрахромосомного елемента є навантаженням на клітину, вона буде переповнена іншими клітинами, які не містять плазміду.
- Оскільки в прокаріотичних клітині сегрегація плазмід є випадковою подією, можуть виникати дочірні клітини, які не містять плазміди, і вони ростуть швидше (поза конкуренцією) батьківської клітини.
- Іншими словами, за відсутності інших тисків, через певний проміжок часу популяція клітин в культурі буде тими, які «втратили» плазміду.
.png)
Малюнок 2.3.3: Втрата плазміди
- У організмах з більш ніж однією хромосомою (еукаріоти) існують різноманітні механізми, що забезпечують належну сегрегацію хромосом, тобто переконатися, що дочірні клітини містять рівні числа всіх хромосом.
- Одним з основних механізмів є те, що кожна хромосома містить необхідні гени, і якщо вони втрачені, клітина не може вижити.
Стійкість до лікарських засобів
- На сьогоднішній день найпоширенішим підходом до підтримки плазмід є включення генів резистентності до ліків.
- Вони також відомі як маркери, які можна вибрати, тобто ми можемо вибрати для їх присутності, включивши антибіотики в середовищі росту.
Ампіцилін
- Ампіцилін зв'язується і пригнічує ряд ферментів в бактеріальній мембрані, які беруть участь в синтезі грамнегативної клітинної стінки.
- Тому правильна реплікація клітин не може відбуватися в присутності ампіциліну.
- Ген стійкості до ампіциліну (amp r) кодує фермент (b -лактамазу), який секретується в периплазматичний простір бактерії, де він каталізує гідроліз b -лактамного кільця ампіциліну.
- Таким чином, генний продукт гена amp r руйнує антибіотик.
- З часом ампіцилін в культуральному середовищі або тарілці Петрі може бути істотно знищений b -лактамазою.
- Коли це відбувається, можуть виникнути клітинні популяції, які «втратили» плазміду.
.png)
Малюнок 2.3.4: Резистентність до ампіциліну
Тетрациклін
- Тетрациклін зв'язується з білком 30S субодиниці рибосоми і пригнічує рибосомну транслокацію вздовж месенджерної РНК, яка кодує білок (тобто препарат перешкоджає нормальному трансляції або виробленню білків).
- Ген резистентності до тетрацикліну (tet r) кодує 399 амінокислотний зовнішній мембранний асоційований білок грамнегативних клітин, що запобігає потраплянню антибіотика в клітину.
- Таким чином, цей ген резистентності до ліків не руйнує антибіотик. Тиск буде підтримуватися протягом усього процесу культури клітин, щоб зберегти плазміду, що містить ген, стійкий до препарату.
хлорамфенікол
- Хлорамфенікол зв'язується з рибосомальної субодиницею 50S і пригнічує синтез білка.
- Ген стійкості до хлорамфеніколу (Cm r) кодує білок, відомий у котячого білка.
- Котячий білок - це тетрамерний цитозольний білок, який у присутності ацетилкоферменту А каталізує утворення гідроксилацетоксипохідних хлорамфеніколу, які не здатні зв'язуватися з рибосомою.
- Як і у випадку з ампіциліном , продукт гена Cm r руйнує антибіотик.
- Крім того, на експресію котячого білка впливає (вниз регулюється) присутність глюкози в середовищі.
Канаміцин і неоміцин
- Зв'язується з рибосомними компонентами і пригнічує синтез білка.
- Ген Kan r кодує білок, який секретується в периплазматичний простір і перешкоджає транспортуванню цих антибіотиків в клітину.
- Як і резистентність до тетрацикліну, ген Kan r не руйнує антибіотик.
Коліцин Е1
- Це член загального класу речовин, відомих як бактеріоцини.
- Коліцин Е1 викликає летальні зміни мембрани бактерій.
- Ген резистентності до ліків (CEA) кодує білок, який невідомим чином перешкоджає дії коліцину.
Прокаріотичні плазміди
- Окрім виготовлення плазміди за допомогою E. coli orIC області, існує природна плазміда кишкової палички, яка називається плазмідою Cole1.
- Походження реплікації Cole1 є однонаправленим (на відміну від ORIC)
- Реплікація з області Ori CoLe1 не вимагає асоційованих білків (наприклад, білка ДНК), таких як OriC, (але для цього потрібні специфічні молекули РНК).
- Залежно від точної області походження Cole1, яка вставляється в кругову молекулу ДНК, екстрахромосомний елемент буде підтримуватися з «низьким» або «високим» номером копії
- Ген rop поблизу походження Cole1 бере участь в регуляції реплікації.
- Якщо область Ori Cole1 включає цей ген, то плазміда підтримується середнім номером копії 10-30 плазмід/клітина. Це вважається низьким номером копії.
- Якщо область Ori Cole1 не має гена rop, то отримана плазміда підтримується середнім числом копій 100-200 плазмід/клітина. Це вважається високим типом копії номера плазміди.
- Якщо плазміда містить ген, який кодує білок (як гени резистентності до ліків), номер копії може впливати на кількість такого білка в клітині.
ПБр 322 (4.36 Кб)
- Одна з оригінальних клонуючих плазмід.
- Побудований шляхом лігування разом:
- ген резистентності до тетрацикліну з плазміди PSc101
- Cole1 і область краплі з плазміди Cole1
- ген стійкості до ампіциліну з транспозону Tn3
- Містить як ампіцилін, так і гени резистентності до тетрацикліну (маркери).
- Містить унікальні сайти обмежень всередині і зовні цих маркерів.
- Містить область rop поблизу CoE1 ori, отже, має низьке число копії (10-30)
- Нумерація починається з унікального сайту обмеження eCoR I (GAATTC). Перший 'T' в цій послідовності є базовим числом «1».
.png)
Малюнок 2.3.5: ПБР322
Схема плазміди:
- У центрі - назва плазміди (зазвичай починається з нижнього регістру «p») та розмір у базових парах
- внутрішнє кільце забезпечує кліщі в інтервалах 1 Кілобаза (Кб), щоб дати уявлення про загальне розташування частин плазміди
- стрілки вказують гени, маркери, орі або реплікації, промотори, полілінкери, термінатори транскрипції та інші важливі або функціональні елементи
- зовнішнє кільце зазвичай вказує на розташування унікальних, або обмеженого числа (зазвичай <3), місць обмеження ендонуклеази. Рестрикційні ферменти, які мають більше трьох ділянок, не вказуватимуться. Майте на увазі, що ферменти, які не ріжуться взагалі, теж не будуть перераховані!
ПУК18/19 (2.69 Кб)
- Не вистачає гена rop поблизу області Ori Cole1. Таким чином, ця плазміда має тенденцію накопичуватися у великій кількості копій (100-200).
- Цей вектор містить лише маркер резистентності до ампіциліну.
- Цей вектор містить область полілінкера
- Синтетична послідовність ДНК, яка містить кластеризацію унікальних сайтів розпізнавання рестрикційних ферментів
- Дозволяє вставляти фрагменти ДНК, породжені різноманітними рестрикційними ендонуклеазними розщепленнями, в плазміду
- PuC18 має полілінкер в одній орієнтації
- PuC19 має той же полілінкер, але в протилежній орієнтації
- Таким чином, фрагменти з унікальними місцями обмеження на кожному кінці можуть бути вставлені в певній орієнтації
- Сайт Post I в amp або гені був мутований, щоб видалити його. Сайт eCOR I в позиції (1) був мутований, щоб видалити його. Це було зроблено для того, щоб зробити сайти обмежень в області полілінкера унікальними.
- Цей вектор також містить область промотора транскрипції з лак-оперону, яка дозволяє вставляти та транскрибувати/перекладати чужорідні гени.
- Полілінкерна область знаходиться лише нижче за течією (3') до промоутера лаку
- Вставлені гени можна транскрибувати з цього промотора
.png)
Малюнок 2.3.6: PUC18/19
