5.1: Q-ЯМР для визначення чистоти макролідних антибіотиків еталонних стандартів - Порівняння з методом балансу маси
- Page ID
- 19463
Макролідні антибіотики отримують з мікробних ферментацій. Як клас макролідних антибіотиків містять 14- або 16-членний макроциклічний лактон, що містить аміногрупи і дезоксицукру. Антибактеріальна активність цих сполук виникає внаслідок пригнічення синтезу бактеріального білка. Оскільки макроліди накопичуються всередині лейкоцитів, вони транспортуються до місця зараження. Деякі макроліди також мають імуномодулюючу дію, здатну зменшити запалення. Одним з найвідоміших макролідних антибіотиків є еритроміцин, будова якого показано тут.
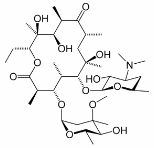
Ця програма вивчає використання кількісних вимірювань ЯМР 1 Н для визначення чистоти макролідних антибіотиків еталонних стандартів. Були протестовані зразки кларитрміцину, рокситроміцину, азитриміцину, диритроміцину та мідекаміцину. Експерименти Q-ЯМР проводилися на частоті 500 МГц з використанням 1,4-динітробензолу як внутрішнього стандарту. Замість визначення часу релаксації T 1, затримка релаксації (64 с) була обрана шляхом порівняння пікової площі для внутрішнього стандарту, використовуючи d 1 затримки 1, 5,10, 20, 32, 64 та 256 с.
Результати Q-ЯМР порівнювали з більш традиційним підходом визначення балансу маси, показаним у таблиці 1 нижче. При визначенні балансу маси вміст обчислюється так, як показано в Рівнянні\(\ref{E1}\).
\[\mathrm{Content\: \% = (1 - impurity\%)(1 - water\% - volatile\: material\: \% - sulfated\: ash\%) \times 100} \label{E1}\]
При цьому визначенні домішка% визначається ВЭЖХ-УФ. Вміст води визначають титруванням Карла Фішера, а залишкові розчинники вимірюють за допомогою газової хроматографії. Кількість сульфатованої золи (перш за все європейське позначення) відповідає кількості залишку, що залишився після займання зразка. Одним з недоліків HPLC-UV для цих вимірювань є відсутність хромофора з характерною довжиною хвилі поглинання. Крім того, загальна проблема такого підходу полягає в тому, що коефіцієнт поглинання УФ кожної домішки різний, і в багатьох випадках невідомий.
Визначення чистоти з використанням ЯМР покладаються на порівняння інтегралів, виміряних для резонансів аналіта (I x) з інтегралом стандарту кількісного визначення (I std). В даному випадку використовувався внутрішній стандарт. Оскільки відомі маси зразка (m x) і внутрішній стандарт (m std), вміст аналіту можна визначити. Зверніть увагу, що основне припущення в цьому методі полягає в тому, що резонанси домішок не перекриваються з резонансами, використовуваними для вимірювання вмісту аналітів. Чистота аналіту, Px, розраховується так, як показано в Рівнянні\(\ref{E2}\):
\[P_x = \dfrac{I_x}{I_{std}} \dfrac{N_{std}}{N_x} \dfrac{M_x}{M_{std}} \dfrac{m_{std}}{m_x} P_{std} \label{E2}\]
де M x і M std - молярні маси аналіта і стандарту, відповідно P std - чистота стандарту, а N std і N x - кількість спінів, що відповідають за інтегрований стандартний і аналітичний сигнали відповідно. Результати вмісту, узагальнені в таблиці 1, для макролідних антибіотиків, отриманих при 1 Н ЯМР та методом балансу маси, добре узгоджуються. Основним джерелом невизначеності в методі Q-ЯМР був у вазі зразка, близько 15 мг в цих експериментах. Використання більшої маси зменшило б невизначеність результатів, але споживало б більшу кількість дейтрованих розчинників. Інформативною особливістю цього звіту є детальний аналіз помилок, який він містить.
| 1 Н Q-ЯМР метод (%) | Метод балансу маси (%) | |||||||
|---|---|---|---|---|---|---|---|---|
| Середній вміст a | ЧЕРВОНИЙ | U розширений | Домішкові/U 1 | Вода/U 2 б | Залишкові розчинники/U 3 b | Сульфатна зола/ч 4 г | Вміст/U розширено | |
| Кларитроміцин | 96.3 | 0,49 | 1.89 | 3,35/0,0299 | 1,4/0,0148 | <0,001/<8,4 х 10 -6 | 0/0 | 95,3/2,64 |
| Рокситроміцин | 95.7 | 0,44 | 1.82 | 2.50/0,0223 | 2,2/0,0233 | <0,001/<8,4 х 10 -6 | 0/0 | 95.4/2,64 |
| азитроміцин | 94.3 | 0,50 | 1.36 | 1,59/0,0142 | 4,5/0,0486 | <0,001/<8,4 х 10 -6 | 0.02/0,0198 | 94.0/2,75 |
| Діритроміцин | 96.9 | 0 | 1.81 | 3,30/0,0295 | 0,6/0,00636 | <0,001/<8,4 х 10 -6 | 0/0 | 96.1/2.67 |
| Мідекаміцин | 97.1 | 2.0 | 1.96 | 3,94/0,0352 | 0,16/0,000035 см | 0/0 | 95.9/1,71 | |
|
||||||||
Довідка
Лю, С.-Ю.; Ху, С.-К. «Порівняльне дослідження невизначеності калібрування еталонних стандартів макролідних антибіотиків з використанням кількісних методів ядерного магнітного резонансу та балансу маси» Анал. Чим. Акт 2007, 602, 114-121.
