2.1: Взаємодія електромагнітного випромінювання та електронів у молекулах
- Page ID
- 25060
Тепер ми розширимо цю ідею від атомів до молекул. Подібно до того, як електрони займають атомні орбіталі в атомах, електрони в молекулах займають молекулярні орбіталі. \[\left. A+hv \rightarrow A^{*}(\text { excited state }) \rightarrow A \text { (ground state }\right)+hv\]
Як і у випадку з атомними орбіталями, електрони на молекулярних орбіталах можуть поглинати або вивільняти фотони певної енергії, коли вони рухаються від однієї молекулярної орбіталі до іншої. Однак існує значна різниця між процесом поглинання/емісії ізольованих атомів (або іонів) та процесом молекул. Коли електрон підвищується до більш високого рівня енергії в атомі, продукт є атомом у збудженому стані - як правило, збуджений атом (або іон) розпадається назад до основного стану, випромінюючи фотон (\(\downarrow\)). Однак, коли електрон всередині молекули збуджується, він рухається (або «просувається») від початкової молекулярної орбіти до іншої. Зараз існує ряд різних наслідків, які можуть виникнути. Наприклад, якщо електрон поглинає фотон і просувається від склеювальної молекулярної орбіти до антізв'язуючої орбіти, результатом буде те, що зв'язок розірветься, оскільки зараз немає загальної стабілізуючої взаємодії. Розглянемо\(\mathrm{H-H}\), яка є найпростішою можливою молекулою. Набір молекулярних орбіталів для водню включає в себе\(\sigma\) (сигма-) зв'язок і\(\sigma^{\star}\) антібондинговую орбіталь. У наземному (або найнижчому енергетичному) стані молекулярний водень має\(\sigma\) зв'язкову орбіталь, що містить обидва електрони молекули. Якщо один із зв'язкових електронів поглинає фотон, який має потрібну кількість енергії (різниця енергії між зв'язком та антізв'язуючою орбіталлю), він буде просуватися і рухатися в дестабілізовану антитілінгову орбітальну, що призведе до розриву зв'язку між атомами, оскільки зараз немає загального зв'язку. взаємодія. Як ви могли собі уявити, якби хімічні зв'язки були схильні до розриву лише шляхом впливу електромагнітного випромінювання низької енергії (наприклад, видимого світла), світ був би іншим (і досить нудним) місцем. Наприклад, життя було б неможливим, оскільки воно залежить від стабільності молекул. Насправді енергія фотонів, необхідних для розриву зв'язків, досить велика. Наприклад, енергія, необхідна для розриву\(\mathrm{H-H}\) зв'язку (енергія зв'язку) є\(436 \mathrm{kJ} / \mathrm{mol} \text {. }\). Якщо обчислити довжину хвилі фотона, який може доставити цю кількість енергії, кількість енергії, необхідної для розриву одного\(\mathrm{H-H}\) зв'язку, буде знаходитися в далекій УФ секції електромагнітного спектра (~ 280 нм). Типово сильний ковалентний\(\sigma\) (або одиночний) зв'язок вимагає досить високоенергетичних фотонів, щоб розірвати їх.
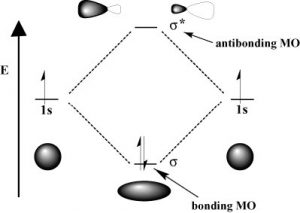
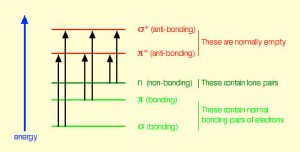
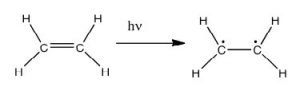
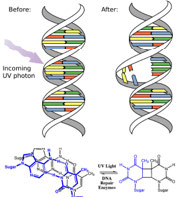
Насправді атмосфера Землі блокує більшість (\(>98 \%\)) високоенергетичних (ультрафіолетових) фотонів, а більшість біологічно важливих молекул не можуть поглинати видиме світло, так що залишає нас питанням про те, навіщо потрібен сонцезахисний крем, який фільтрує УФ-фотони А (400 - 315 нм) та УФ В (315 - 280 нм) . Відповідь полягає в тому, що ряд біологічних молекул містить більше, ніж прості сигма-зв'язки. Наприклад, більшість складних біологічних молекул крім зв'язків містять\(\pi\) (пі) зв'язки і\(\sigma\) незв'язні електрони; можуть спостерігатися переходи між цими орбіталями. Енергетичні проміжки між цими різними орбіталями досить менші, ніж енергетичний зазор\(\sigma-\sigma\) *. Фотони з достатньою енергією, щоб викликати ці електронні переходи, присутні в сонячному світлі. Наприклад, подвійний зв'язок зазвичай включає в себе як\(\sigma\) і\(\pi\) зв'язок. Поглинання фотона, який сприяв би електрону від орбіти\(\pi\) зв'язку до\(\pi^{\star}\) антизв'язкової орбіти, матиме ефект розриву вихідного pi зв'язку. Один із способів представити це показано тут (\(\rightarrow\)). У цьому випадку один з електронів, який був у зв'язці пі, зараз знаходиться в високоенергетичній орбіталі антизв'язування pi* і є набагато більш реактивним. Інший спосіб подумати про це полягає в тому, що електрони зараз непарні, і набагато частіше реагують на формування більш стабільної сутності. [1] Очевидний спосіб відновити стабільність полягає в тому, щоб електрон в\(\pi\) антизв'язній орбіті опустився до рівня енергії зв'язку і випромінював фотон тієї ж енергії, і в більшості випадків це відбувається - врешті-решт не завдаючи шкоди. (Як ми побачимо пізніше, оскільки подвійні зв'язки обмежені обертанням, ще одним можливим явищем є те, що навколо єдиного [\(\sigma\)] зв'язку може бути обертання), а потім реформування\(\pi\) зв'язку, що призводить до ізомеру вихідного алкена). Однак у деяких випадках, якщо поруч є інші потенційно реактивні форми, реакції між молекулами (або у випадку біологічних макромолекул, між різними областями цих молекул) можуть виникнути і спричинити проблеми. Наприклад: більшість з нас знають, що перебування на сонці спричиняє пошкодження шкіри, що може призвести до раку шкіри. Основний механізм відбувається в ДНК, де дві основи тимідину примикають один до одного. УФ-фотон може бути поглинутий pi зв'язком в одній тимінової основі. Цей розірваний пін-зв'язок (і в результаті непарний електрон) дуже реактивний. Він може реагувати з pi зв'язком у сусідньому тиміні, що призводить до нового зв'язку, реакції, яка виробляє чотиричленне вуглецеве кільце, відоме як тиміновий димер. Механізм реплікації ДНК не може точно повторити послідовність, що містить тиміновий димер, що призводить до зміни послідовності ДНК - мутації. Мутації цього типу є поширеним раннім етапом генерації ракових клітин шкіри (карцином) і пігментних клітин (меланом). [2]
Більш доброякісний приклад поглинання фотонів у біологічних системах лежить в основі механізму, за допомогою якого ми (та інші організми) виявляємо світло - саме так ми можемо бачити речі! Хоча спочатку вважалося (принаймні деякими), що бачення включало промені, що випромінюються з очей, [3] ми тепер розуміємо, що для того, щоб побачити, нам потрібно виявити фотони, які відбиваються або випромінюються об'єктами навколо нас. Процес починається, коли фотони світла потрапляють на клітини, відомі як фоторецептори. У наших очах ці клітини розташовані всередині сітківки: аркуш клітин, які вирівнюють внутрішню поверхню ока. У межах підмножини клітин сітківки знаходиться ряд різних типів молекул, які містять pi зв'язки. Ці молекули - це білки, загально відомі як опсіни. Опсин складається з поліпептиду (або апопротеїну), який ковалентно пов'язаний з іншою молекулою, 11-цис-сітківки. [4]
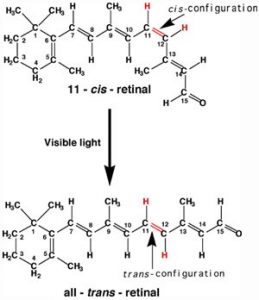
Ця молекула походить від вітаміну А (все-транс-сіткінальний). Комплекс апопротеїну і сітківки - функціональний білок опсін. Існує ряд різних компонентів опсіна, які впливають на довжину хвилі фотонів, поглинених функціональним білком опсін. Коли фотон поглинається, він просуває електрон від однієї з pi зв'язків сітківки до антизв'язуючої орбіти. Замість того, щоб взаємодіяти з іншою молекулою, як тимін, відбувається обертання навколо залишилася одиничної (сигма-) зв'язку, а потім утворення нової pi зв'язку, це призводить до ізомеризації вихідної 11-цис-форми в транс-ізомер. Ця зміна форми сітківки впливає на форму білка опсіна, який ініціює каскад електрохімічних подій, які несуть сигнали до решти мозку (сітківка вважається продовженням мозку), які врешті-решт визнаються візуальним входом.
