5.4: Оптична активність
- Page ID
- 24625
Два енантіомери є дзеркальним відображенням один одного. Вони дуже схожі і мають багато спільних властивостей, як той же B.p., m.p., щільність, колір, розчинність і т.д. насправді, пара енантіомерів мають однакові фізичні властивості, за винятком того, як вони взаємодіють з плоскополяризованим світлом.
При нормальному освітленні електричне поле коливається у всіх напрямках. Коли нормальне світло проходить через поляризаційний фільтр, може пройти лише світло, що коливається в одній площині, а отримане світло, яке коливається в одному єдиному напрямку, називається плоскополяризованим світлом.
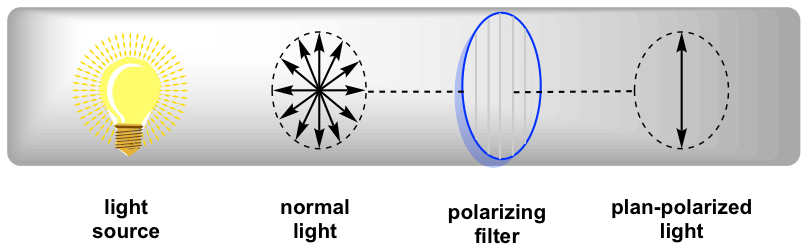
Коли план-поляризоване світло взаємодіє з хіральними молекулами, площина поляризації буде обертатися хіральними речовинами. Вперше Жан-Батістом Бйо було виявлено в 1815 році, що деякі природні органічні речовини, такі як камфора, здатні обертати площину поляризації плоскополяризованого світла. Він також зазначив, що деякі з'єднання обертали площину за годинниковою стрілкою, а інші проти годинникової Подальші дослідження вказують на те, що ротація викликана хиральністю речовин.
Властивість з'єднання, здатного обертати площину поляризації плоскополяризованого світла, називається оптичною активністю, а з'єднання з такою активністю позначається як оптичне активне. Стереоізомер, який є оптичним активним, також називають оптичним ізомером.
Хіральне з'єднання оптично активне. Ахіральне з'єднання оптично неактивне.
Зразок, що містить хіральне з'єднання, обертає площину поляризації плоскополяризованого світла, напрямок і кути обертання залежать від характеру і концентрації хіральних речовин. Кути повороту можна виміряти за допомогою поляриметра (далі в цьому розділі).
Для пари енантіомерів з однаковою концентрацією при тій же умові вони обертають площину поляризації з тими ж кутами, але в протилежному напрямку, один - за годинниковою стрілкою, а інший проти годинникової стрілки.
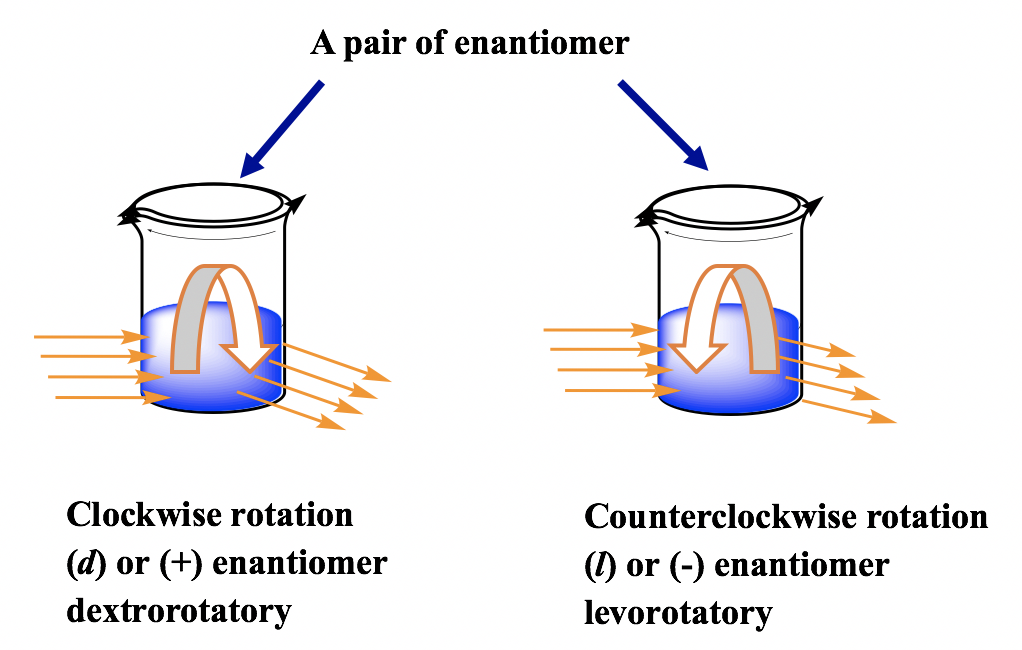
Енантіомер обертає площину поляризації за годинниковою стрілкою, як кажуть, декстроротаторний (латинський, означає праворуч), і позначений префіксом (d) або (+). Енантіомер обертає площину поляризації проти годинникової стрілки, як кажуть, леворотаторний (латинський, означає ліворуч), і позначений префіксом (l) або (—). D/l (або +/-) вказують напрямок, в якому оптична активна сполука обертає площину поляризації план-поляризованого світла, що має бути визначено експериментом для вимірювання оптичного обертання. d/l (або +/ —) символ не має нічого спільного з R/S. R/S вказує на розташування груп навколо центру хиральності, що можна визначити, знаючи точне просторове розташування груп. Це означає, що з'єднання з конфігурацією R може бути або d, або l, а з'єднання з конфігурацією S також може бути d або l. Для наведених нижче прикладів обидві сполуки є S -ізомером, але одне - d (+), а інше - l (-).

Єдине, в чому ми можемо бути впевнені, це те, що для пари енантіомерів, якщо один енантіомер був визначений як d, то інший енантіомер повинен бути l, і навпаки.
Вимірювання оптичного обертання
Поляриметр - прилад, який вимірює напрямок і кути обертання плоскополяризованого світла. Плоскополяризоване світло проходить через пробірку для зразка, що містить розчин зразка, і кут поворотів буде прийнятий і зафіксований аналізатором, як узагальнено на рис. 5.4c.
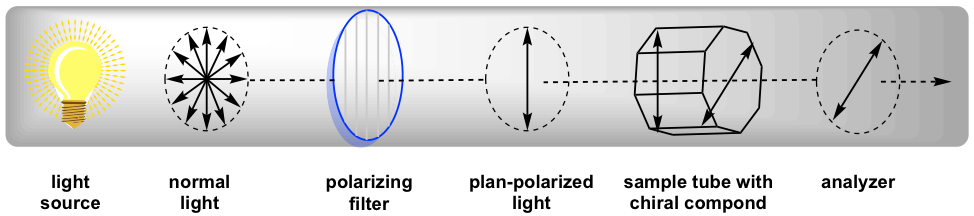
Оскільки результати вимірювань змінюються залежно від довжини хвилі використовуваного світла, для більшості поляриметрів використовується питоме світло атомного спектру натрію з довжиною хвилі 589 нм, який називається D-лінією натрію. Ступінь обертання, виміряна поляриметром, називається спостережуваним обертанням (α), а спостережуване обертання залежить від довжини трубки зразка, концентрації зразка та температури.
Для порівняння оптичного обертання між різними сполуками в узгоджених умовах![]() використовується питоме обертання. Питома ротація - це обертання, викликане розчином з концентрацією 1,0 г/мл у пробірці для зразків довжиною 1,0 дм. Виходячи з цього визначення, питоме обертання можна обчислити за спостережуваним обертанням, застосовуючи формулу:
використовується питоме обертання. Питома ротація - це обертання, викликане розчином з концентрацією 1,0 г/мл у пробірці для зразків довжиною 1,0 дм. Виходячи з цього визначення, питоме обертання можна обчислити за спостережуваним обертанням, застосовуючи формулу:

Зверніть увагу: У цій формулі одиниця концентрації (г/мл) і довжина пробірки для зразка (дм) не є тими одиницями, з якими ми знайомі. Крім того, одиниця питомого обертання знаходиться в градусі (°), не потрібно турбуватися про скасування одиниць в цій формулі.
Приклади: Обчислення питомого обертання
Спостережуване обертання 10,0 г (R) -2-метил-1-бутнаолу в 50 мл розчину в 20-сантиметровій поляриметровій трубці становить+2,3° при 20° C, яке питоме обертання сполуки?
Рішення
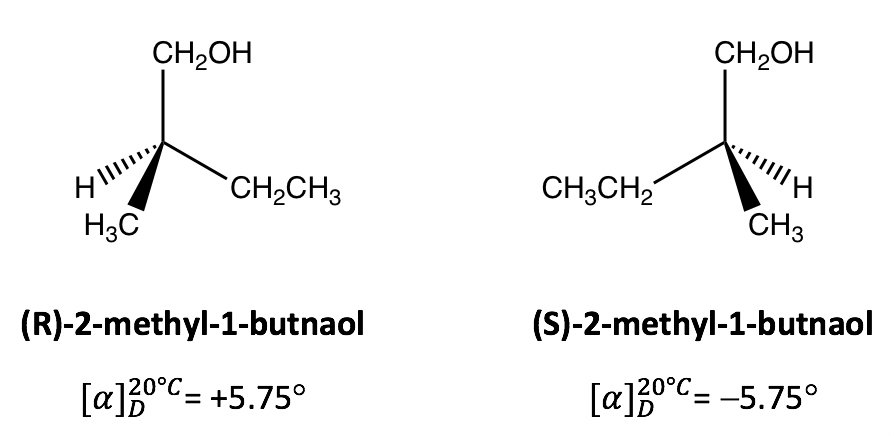
Питоме обертання - характерна властивість оптичного активного з'єднання. Літературні конкретні значення обертання автентичної сполуки можуть бути використані для підтвердження ідентичності невідомої сполуки. Для прикладу тут, якщо було виміряно, що питоме обертання (R) -2-метил-1-бутнаолу становить+5,75 °, то ми можемо сказати, що інший енантіомер (S) -2 -метил-1-бутнаол повинен мати питоме обертання -5,75 °, без подальшого вимірювання необхідного.
Оптична активність різних зразків
Коли вимірюваний зразок містить лише один енантіомер, цей зразок називається енантіомерно чистим, означає, що в зразку присутній лише один енантіомер.
Проба також може складатися з суміші пари енантіомерів. Для такого зразка суміші спостережувані значення обертання суміші разом з інформацією про питому обертанні одного з енантіомерів дозволяють обчислити відсоток (%) кожного енантіомера в суміші. Для проведення такого розрахунку знадобиться поняття надлишку енантіомера (її). Enantiomeric надлишок (ee) говорить про те, скільки надлишок одного енантіомера знаходиться в суміші, і його можна обчислити як:
Ми використаємо низку гіпотетичних прикладів у наступній таблиці для детального пояснення.
| Якщо питоме обертання (+) -енантіомера становить +100 °, то спостерігається обертання наступних зразків (припустимо, що пробірка зразка має довжину 1 дм, а концентрація для кожного зразка становить 1,0 г/мл): | ||
| Номер зразка |
Зразок |
Спостерігається обертання (º) |
| 1 | чистий (+) енантіомер | +100 |
| 2 | Чистий (-) -енантіомер | -100 |
| 3 | Рацемічна суміш 50% (+) -енантіомеру
і 50% (-) -енантіомер |
0 |
| 4 | Суміш 75% (+) -енантіомеру і 25% (-) -енантіомеру |
+50 |
| 4 |
Суміш 20% (+) -енантіомеру і 80% (-) -енантіомеру
|
-60 |
Зразки #1 та #2 прості.
Зразок #3 призначений для суміші з рівною кількістю двох енантіомерів, і така суміш називається рацемічної сумішшю або рацематом. Рацемічні суміші не обертають площину поляризації плоскополяризованого світла, а це означає, що рацемічні суміші є оптично неактивними і мають спостережуване обертання нуля! Це тому, що для кожної молекули в суміші, які обертають площину поляризації в одному напрямку, є молекула енантіомеру, яка обертає план поляризації в протилежному напрямку з тим же кутом, і обертання скасовується. В результаті не спостерігається обертання для загальної рацемической суміші. Символ (±) іноді використовується для позначення суміші рацемічної суміші.
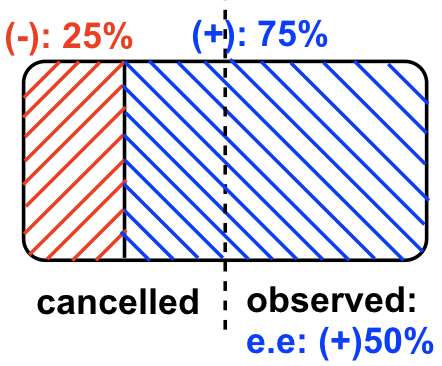
Зразок #4, (+) -енантіомер в надлишку. Оскільки існує 75% (+) -енантіомер і 25% (-) -енантіомер, енантіомерное надлишкове (ee) значення (+) -енантіомеру становить 75% - 25% = 50%, це також можна обчислити за формулою: ee =
У цьому зразку суміші обертання (-) -енантіомеру скасовується обертанням, викликаним частиною (+) -енантіомеру, тому загальна чиста спостережувана обертання залежить від того, наскільки «чиста кількість» (+) -енантіомеру присутній. Це можна показати по наведеній нижче схемі, яка допомагає розібратися.
Зразок #5, (-) -енантіомер в надлишку, і оскільки є 80% (-) -енантіомер і 20% (+) -енантіомер, енантіомерний надлишок (ee) значення (-) -енантіомер становить 80% - 20% = 60%, це також можна обчислити за формулою: ee =
Зверніть увагу: для обчислення значення e.e не потрібно включати знак кута повороту, якщо майте на увазі, що знак (+ або —) спостережуваного обертання вказує на те, який енантіомер є надлишком.
Вправи 5.6
Відповіді на практичні питання Глава 5
Приклади: Розширений рівень обчислення
(+) -енантіомер сполуки має питоме обертання ([α] 20 D) +100°. Для зразка (1 г/мл у клітині 1 дм), який є сумішшю (+) та (-) енантіомерів, спостережуване обертання α становить -45°, який відсоток (+) енантіомеру, присутнього в цьому зразку?
Рішення
Спостережуване обертання знаходиться в «-», тому (-) -енантіомер знаходиться в надлишку.
ee (-) -енантіомеру становить:
Звідси ми побачимо два способи вирішення такого типу питання:
Метод I: розв'язування алгебри
% (-) -енантіомеру встановлюється як «x»;% (+) -енантіомеру встановлюється як «y»
х + у = 100%
х — у = 45%
Вирішити х = 72,5%; у = 27,5%;
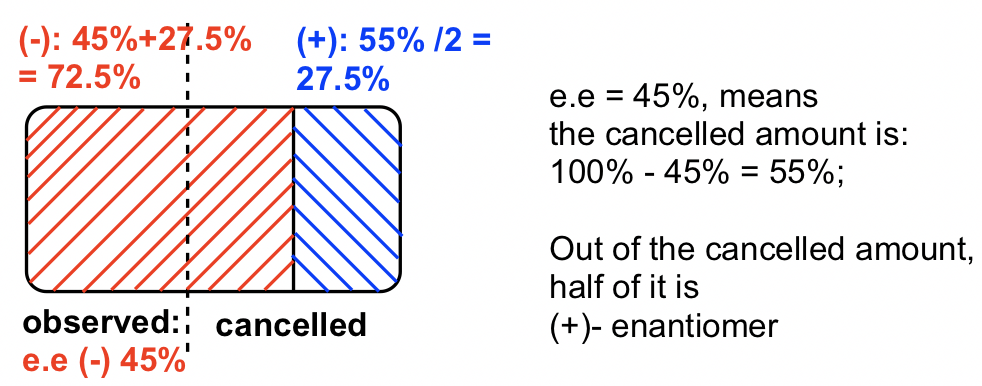
Так у зразку є 72,5% (-) -енантіомер і 27,5% (+) -енантіомеру.
Спосіб II: використовуючи діаграму, відповідь синім кольором, є 27,5% (+) -енантіомеру.
Хіральність і біологічні властивості
Окрім різниці оптичної активності, різні енантіомери хіральної молекули зазвичай виявляють різні властивості при взаємодії з іншими хіральними речовинами. Це можна зрозуміти, використовуючи аналоговий приклад встановлення руки у відповідну рукавичку: права рука вписується лише в праву рукавичку, і вона відчуває себе дивно і незручно, якщо ви носите ліву рукавичку на правій руці. Це тому, що і права рука, і права рукавичка є хіральними. Хіральний об'єкт вписується тільки в певне хіральне середовище.
В організмі людини біологічні функції модулюються безліччю ферментів і рецепторів. Ферменти і рецептори по суті є білками, а білки складаються з амінокислот. Амінокислоти є прикладами природно існуючих хіральних речовин. За загальною формулою, наведеною нижче, група вуглецю з аміно (NH 2) є хіральним (асиметричним) центром для більшості амінокислот, і в природі існує лише один енантіомер (зазвичай S -енантіомер). Кілька прикладів амінокислот наведені нижче із загальною формулою.
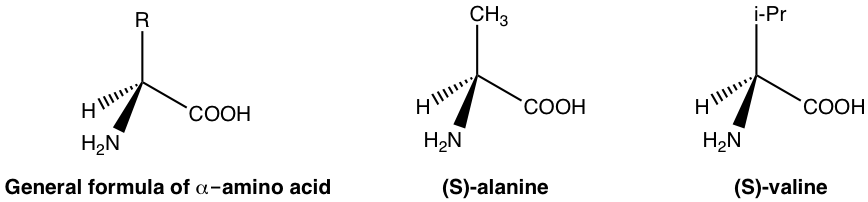
Оскільки амінокислоти є хіральними, білки є хіральними, тому ферменти та рецептори також є хіральними. Таким чином, фермент або рецептор утворюють хіральне середовище в організмі людини, які розрізняють R або S енантіомер. Таку вибірковість можна проілюструвати простою діаграмою нижче.
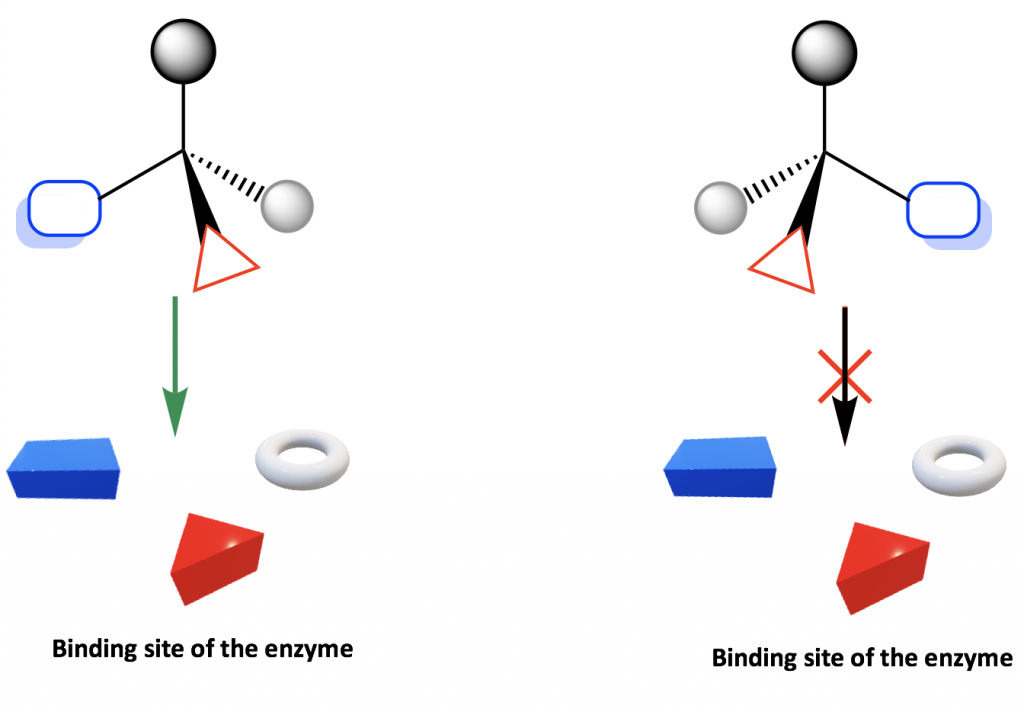
Місце зв'язування ферменту або рецептора є хіральним, тому він зв'язується лише з енантіомером, групи якого знаходяться в належних положеннях, щоб поміститися в місці зв'язування. Як показано на схемі, з ділянкою зв'язується тільки один енантіомер, але не інший енантіомер.
Кілька поширених прикладів для демонстрації такої селективності зв'язування різних енантіомерів можуть включати лімонен і карвон.
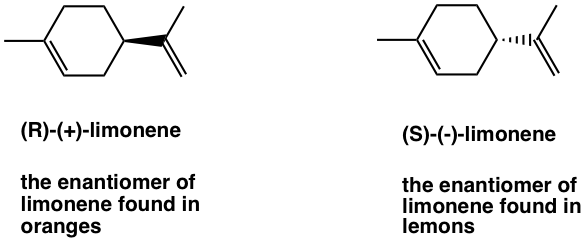
Лімонен має два енантіомери, і вони пахнуть абсолютно по-різному від людини, тому що вони взаємодіють з різними рецепторами, які розташовані на нервових клітині в носі. The (R) - (+) -лімонен відповідає за запах апельсина, а (S) - (-) -лімонен надає трохи запаху лимона.
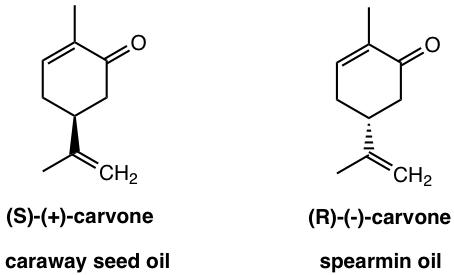
Якщо ви любите кминний хліб, це пов'язано з (S) - (+) -карвоном; а (R) - (-) -карвон, який міститься в олії м'яти, дає набагато інший запах.
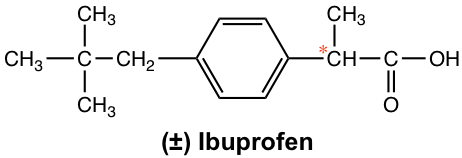
Більш драматичні приклади того, як хіральність відіграє важливу роль в біологічних властивостях, знаходяться в багатьох лікарських засобах. Наприклад, для звичайного протизапального препарату без рецепта ібупрофен (Advil) активний агент є лише (S) -енантіомер, тоді як (R) -енантіомер не має ніякої протизапальної дії. На щастя, (R) -енантіомер не має шкідливого побічного ефекту і повільно перетворюється в (S) -енантіомер в організмі. Ібупрофен продається зазвичай як форма рацемата.
Питання хіральних препаратів (препарат містить єдиний енантіомер, а не як рацемат) не знаходився в центрі уваги галузі відкриття наркотиків до 1960 року. Тоді препарати були затверджені у формі рацемату, якщо задіяний центр хіральності, і подальших досліджень щодо біологічної різниці на різних енантіомерах не проводилося. Все це було змінено трагічним інцидентом талідоміду. Талідомід був препаратом, який продавався у більш ніж 40 країнах, головним чином в Європі, на початку 1960-х років як засіб для сну, а вагітним жінкам - як протиблювотний засіб (препарат, що запобігає блювоті) для боротьби з ранковою нудотою. У той час не було визнано, що властивістю володіє тільки R -енантіомер, в той час як S -енантіомер був тератогеном, що викликає вроджені деформації. Препарат продавався як рацемічна суміш і спричинив пошкодження близько 10 000 дітей, поки він не був вилучений з ринку в листопаді 1961 року. Цей препарат не був схвалений в США, однак, приписується доктору Френсіс О.Келсі, який був лікарем FDA (харчових продуктів і медикаментів) в той час і наполягав на додаткових тестах на деякі побічні ефекти. Тисячі життя врятував доктор Келсі, і вона була нагороджена медаллю президента в 1962 році за запобігання продажу талідоміду.

